¿Alguna vez te has preguntado por qué el agua hierve... Mostrar más
Introducción Básica a la Química










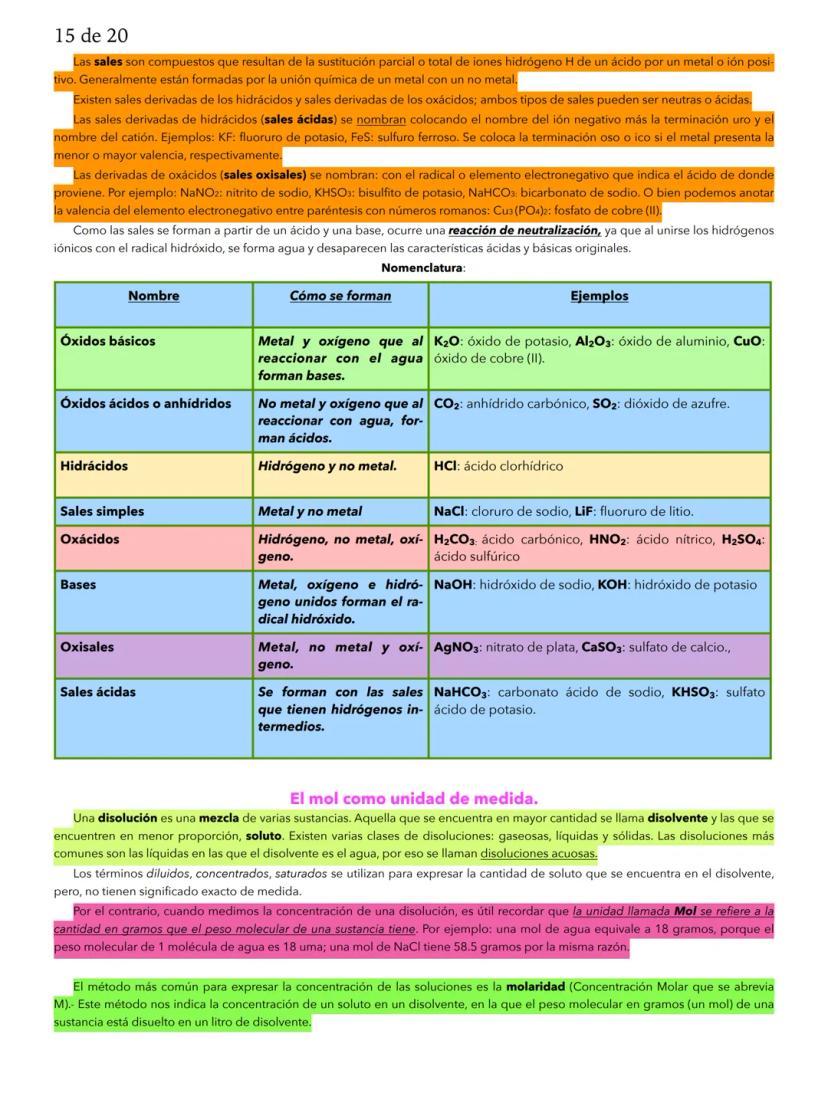



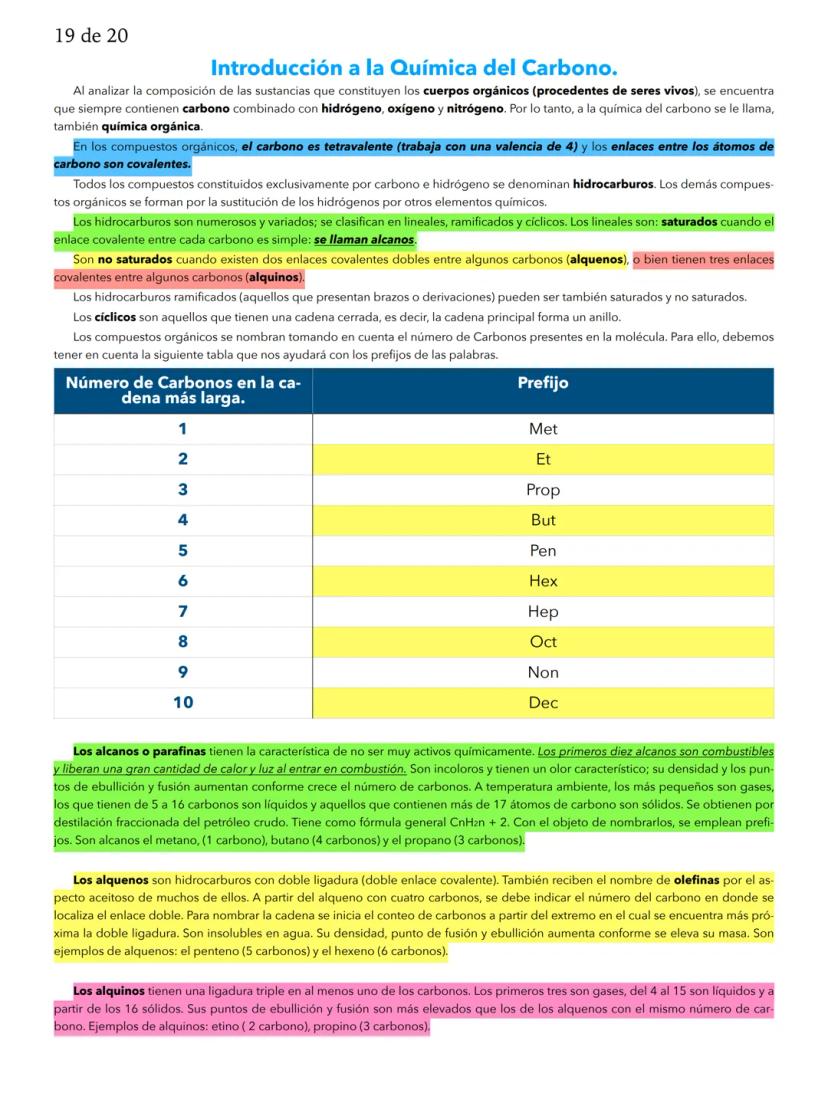
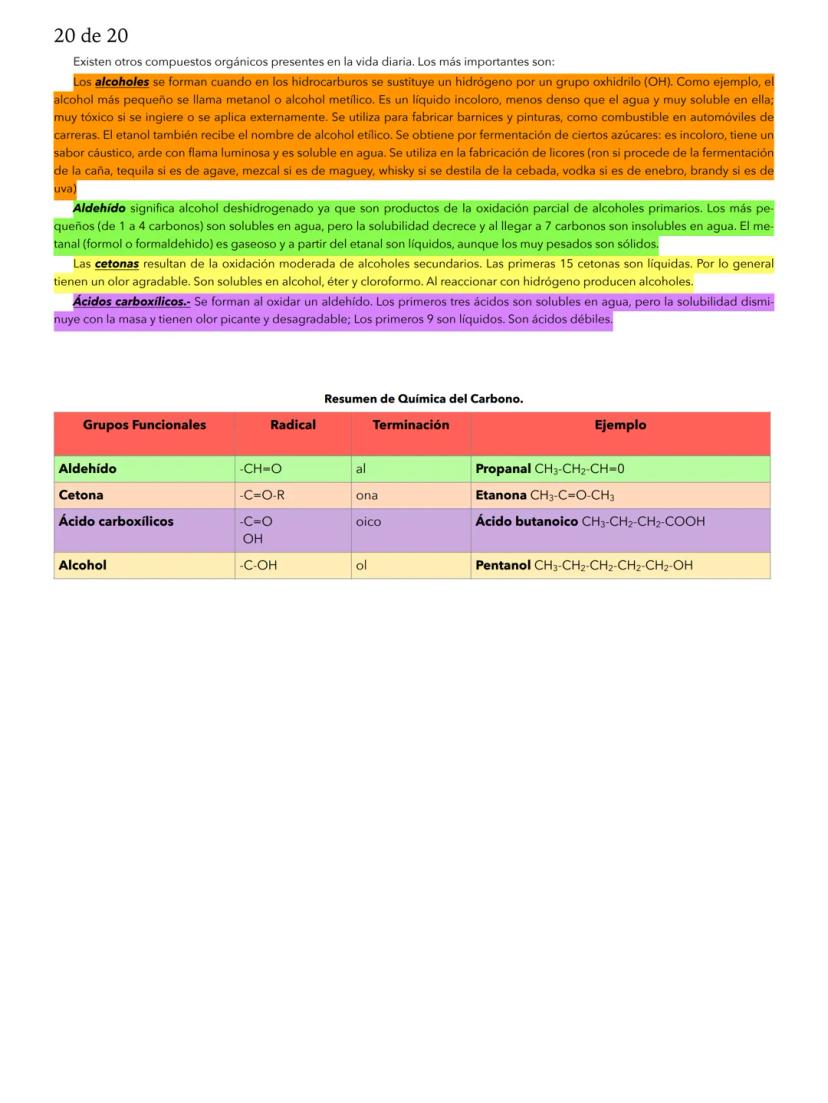

Fundamentos de la Química y Estados de la Materia
La química es la ciencia que estudia la composición, estructura y propiedades de los materiales, así como los cambios que ocurren entre la materia y la energía. Para entender este mundo microscópico, necesitas conocer algunos conceptos básicos que son como el alfabeto de la química.
Un elemento es una sustancia pura formada por átomos iguales que no se puede descomponer en algo más simple. El átomo es la partícula más pequeña de un elemento, como los ladrillos fundamentales de todo lo que existe. Cuando dos o más átomos se unen, forman una molécula.
Los materiales pueden existir en diferentes estados de agregación. Los sólidos tienen sus moléculas muy juntas y casi sin movimiento, manteniendo forma y volumen constantes. Los líquidos se adaptan al recipiente que los contiene pero mantienen su volumen. Los gases no conservan ni forma ni volumen, y se expanden para llenar cualquier espacio.
Dato curioso: Existen dos estados más extremos: el plasma (en las estrellas) y el condensado Bose-Einstein .

Cambios de Estado y Características de los Materiales
Los cambios de estado son transformaciones físicas que ocurren cuando calientas o enfrías una sustancia. La fusión convierte sólidos en líquidos, la vaporización transforma líquidos en gases, y la sublimación pasa directamente de sólido a gas sin ser líquido.
El conocimiento científico en química se basa en observación sistemática, experimentos rigurosos y datos que pueden repetirse. Esto lo diferencia del conocimiento empírico, que se basa solo en experiencias personales.
Las propiedades químicas solo se ven durante reacciones químicas, cuando un material se transforma en otro completamente diferente. La acidez y alcalinidad se miden con la escala de pH: números menores a 7 son ácidos (como el limón), 7 es neutro (agua), y mayores a 7 son básicos (como el jabón).
Otras propiedades importantes incluyen la concentración (cantidad de sustancia disuelta), la solubilidad (cuánto se puede disolver) y el estado de oxidación (electrones ganados o perdidos).
Tip para el examen: Memoriza que el agua tiene pH 7 y es neutra, mientras que la sangre tiene pH entre 7.35-7.45.

Escala de pH y Propiedades Químicas Importantes
El pH es fundamental para entender el comportamiento de las sustancias en tu vida diaria. Los valores van de 0 a 14, donde cada número representa qué tan ácida o básica es una sustancia.
Sustancias ácidas que conoces: jugo de limón , refrescos de cola (pH 2.5), café (pH 5.0). Sustancias básicas: jabón , lejía (pH 11.5). La leche tiene pH 6.5, ligeramente ácido, mientras que el agua de mar es básica con pH 8.2.
La afinidad electrónica mide cuánta energía se libera cuando un átomo atrapa un electrón. Los halógenos (como el cloro y el flúor) son excelentes para esto. La concentración te dice qué tan "fuerte" está una solución - imagina un vaso de agua con una cucharada de azúcar versus uno con diez cucharadas.
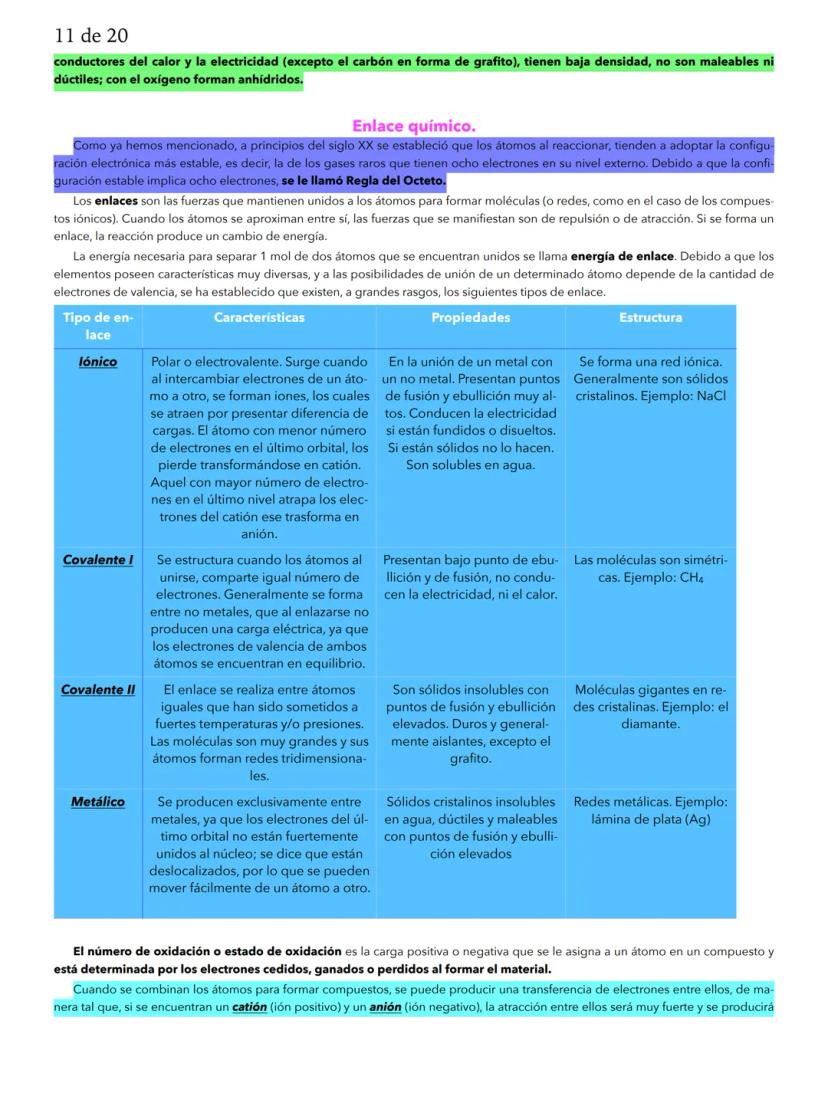
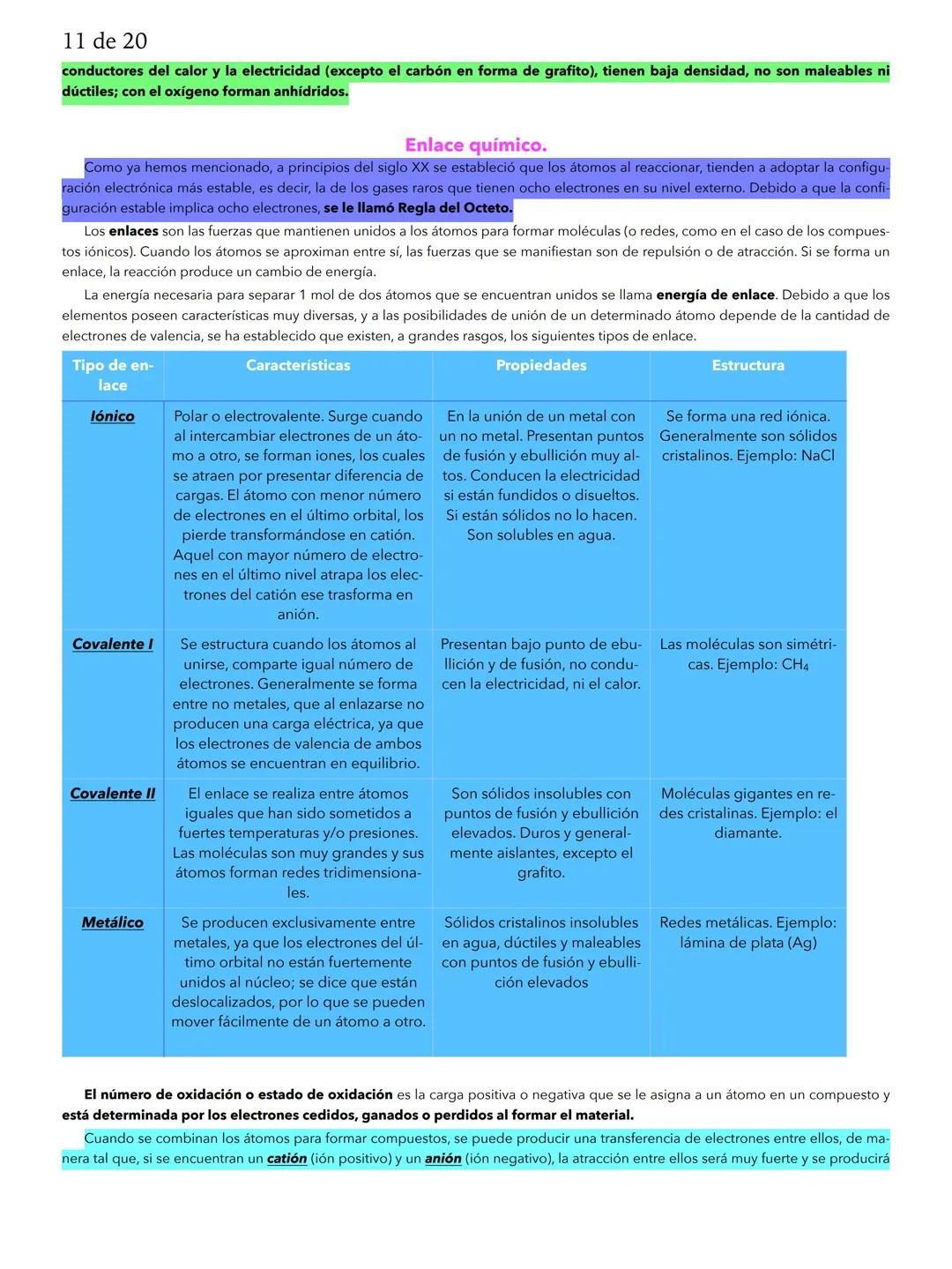
El tipo de enlace químico determina cómo se unen los átomos: pueden compartir electrones (covalente), transferirlos completamente (iónico), o formar una "nube" de electrones (metálico).
Conexión con la vida real: Tu estómago produce ácido gástrico con pH 2.0, ¡casi tan ácido como el limón!
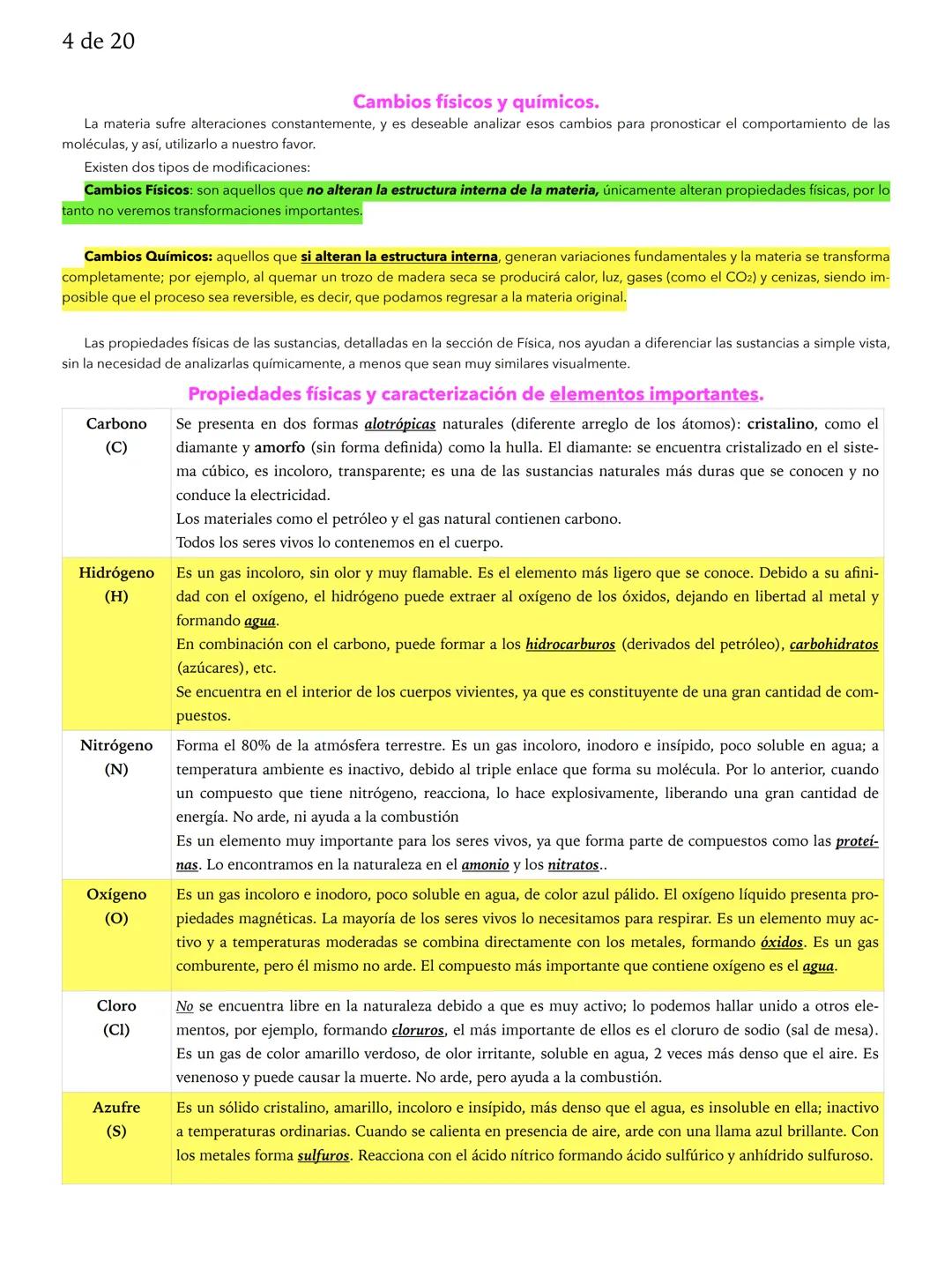
Cambios Físicos vs Químicos y Elementos Importantes
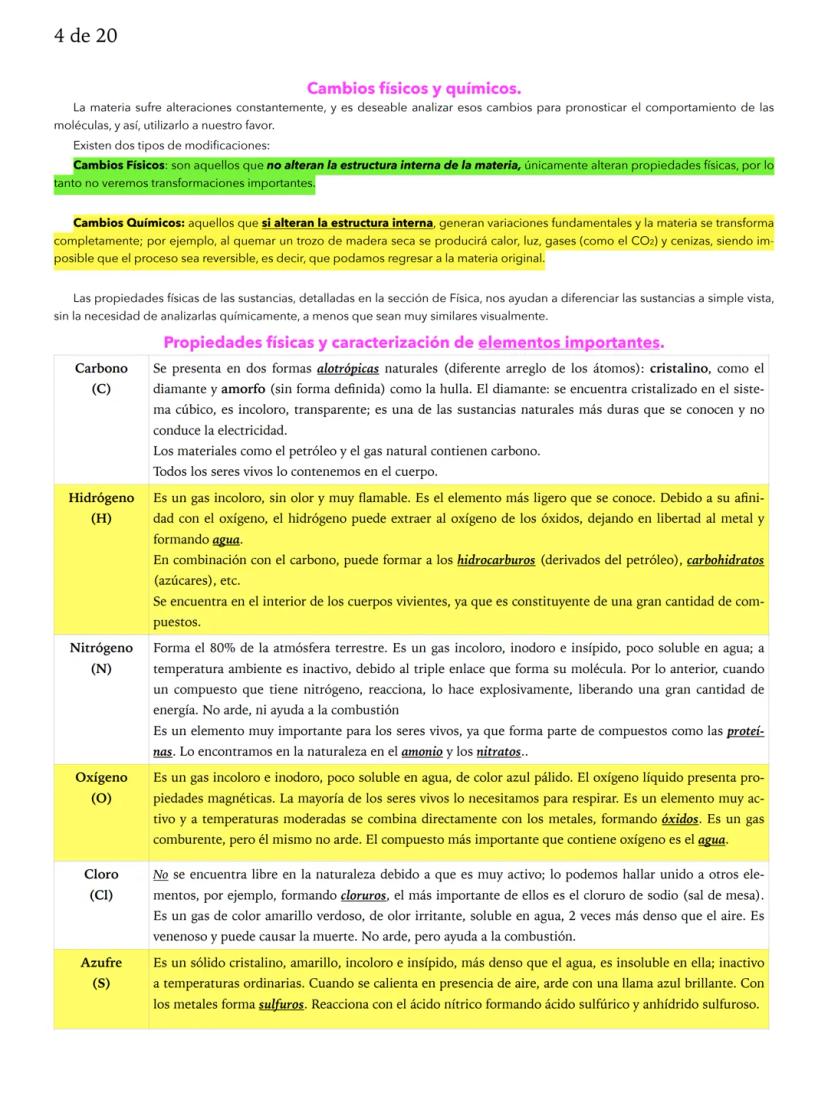
Es crucial distinguir entre cambios físicos y cambios químicos. Los cambios físicos no alteran la estructura interna de la materia (como derretir hielo), mientras que los cambios químicos sí la transforman completamente (como quemar madera).
Ahora conocerás algunos elementos clave. El carbono forma diamantes súper duros y también está en el petróleo y en tu cuerpo. El hidrógeno es el gas más ligero y se combina con oxígeno para formar agua. El nitrógeno forma 80% del aire que respiras pero es muy estable debido a sus enlaces triples.
El oxígeno es esencial para la respiración y ayuda a la combustión, pero él mismo no arde. El cloro es ese gas amarillo-verdoso tóxico que se usa para purificar agua. El azufre es amarillo y arde con llama azul brillante.
En cuanto a metales importantes: el hierro se oxida (se herrumbra) y forma la base del acero. El cobre fue el primer metal que usó la humanidad y conduce muy bien la electricidad. El sodio reacciona violentamente con agua. El aluminio es abundante y se usa en utensilios de cocina.
Dato fascinante: El sodio debe guardarse en queroseno porque reacciona tan rápido con el aire y agua que puede explotar.

Conservación de la Masa y Métodos de Separación
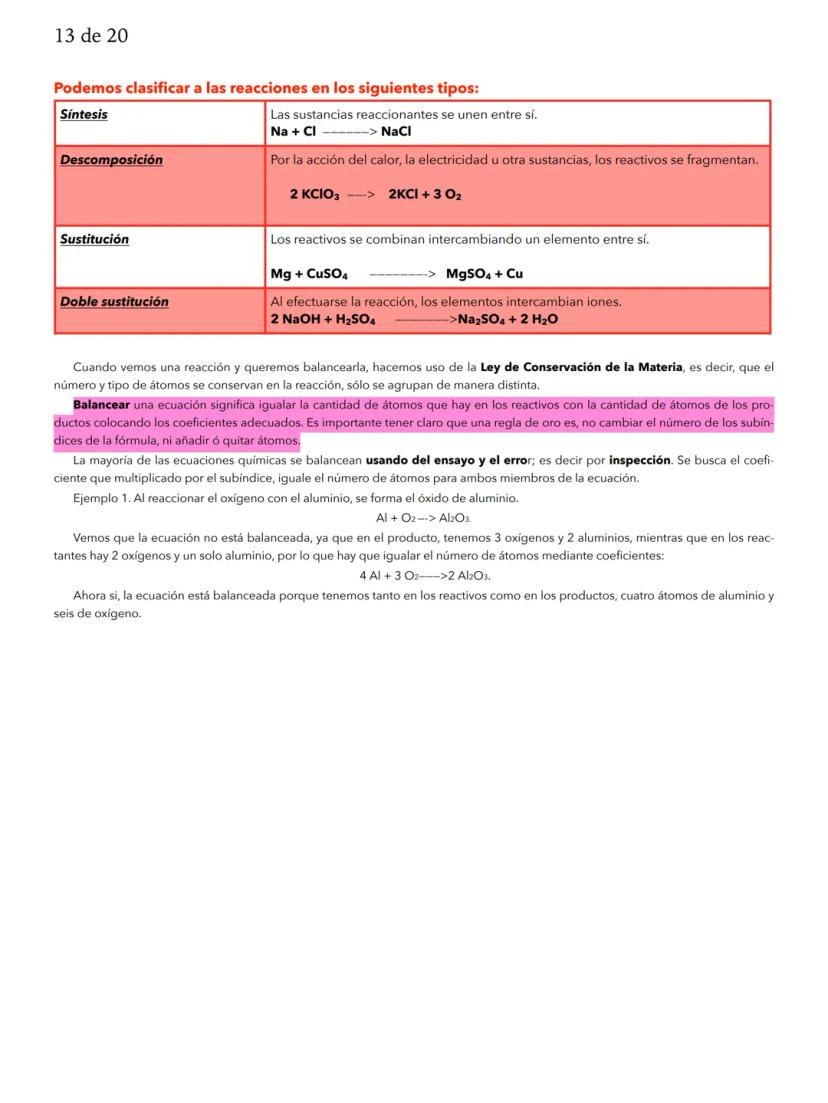
La ley de conservación de la masa de Lavoisier establece que en cualquier reacción química, la masa no se crea ni se destruye, solo se transforma. Si tienes 10 gramos de reactivos, obtienes exactamente 10 gramos de productos.
Las mezclas son uniones físicas (no químicas) de dos o más sustancias que mantienen sus propiedades originales. Las mezclas heterogéneas permiten ver sus componentes a simple vista (como arena y agua), mientras que las homogéneas no (como la leche o el acero).
Para separar mezclas usamos métodos físicos específicos. La decantación usa la gravedad para separar líquidos y sólidos. La filtración emplea papel poroso para retener sólidos. La centrifugación acelera la separación usando fuerza centrífuga.
La evaporación elimina líquidos dejando sólidos, la sublimación separa sustancias que pasan de sólido a gas directamente, y la destilación permite recuperar tanto sólidos como líquidos usando diferentes puntos de ebullición.
Aplicación práctica: Cuando preparas café estás usando filtración, y cuando se evapora agua de mar para obtener sal, es evaporación.

Métodos de Separación y Estados de Agregación
Los métodos de separación son herramientas fundamentales que aprovechan las diferencias en propiedades físicas entre sustancias. Cada método tiene su aplicación específica según el tipo de mezcla que tengas.
La decantación funciona perfectamente cuando tienes aceite y agua, ya que la gravedad separa naturalmente los líquidos de diferente densidad. La centrifugación es como la decantación súper acelerada - imagina cómo funciona una lavadora en el ciclo de centrifugado.
Para separar sólidos de líquidos, la filtración es tu mejor opción. El papel filtro actúa como un colador microscópico que deja pasar el líquido pero retiene las partículas sólidas.
Los métodos que involucran calor son especialmente útiles. La evaporación te permite obtener sal del agua de mar, mientras que la destilación puede separar alcohol del agua porque tienen diferentes puntos de ebullición. La sublimación es perfecta para sustancias especiales como el yodo, que pasa de sólido a gas sin derretirse.
Conexión con tu vida: Cuando tu mamá cuela el café o cuando se seca la ropa al sol, está usando métodos de separación que estudias en química.

Estructura Atómica y Modelos Históricos
Los átomos son los bloques fundamentales de todo lo que existe, compuestos por tres partículas principales. Los protones tienen carga positiva y están en el núcleo, los neutrones no tienen carga y también están en el núcleo, mientras que los electrones con carga negativa giran alrededor del núcleo.
La historia de los modelos atómicos es fascinante. Dalton (1808) imaginó los átomos como esferas sólidas indivisibles. Thomson (1897) descubrió los electrones y propuso el modelo del "pastel con pasas" - electrones incrustados en una masa positiva.
Rutherford (1911) revolucionó todo con sus experimentos disparando partículas contra láminas de oro. Descubrió que los átomos tienen un núcleo diminuto y denso rodeado de mucho espacio vacío. Su modelo planetario mostraba electrones orbitando como planetas alrededor del sol.
Bohr (1913) mejoró el modelo estableciendo que los electrones se mueven en órbitas específicas con niveles de energía definidos: K, L, M, N, O, P, Q. Solo pueden "brincar" entre estos niveles, emitiendo luz en el proceso.
Dato increíble: Si el núcleo fuera del tamaño de una pelota de fútbol, los electrones estarían girando a kilómetros de distancia.

Modelos Atómicos Modernos y Conceptos Fundamentales
Los modelos atómicos evolucionaron hacia conceptos más complejos y precisos. Sommerfeld introdujo las órbitas elípticas, mientras que De Broglie estableció que los electrones se comportan como ondas y partículas al mismo tiempo.
Schrödinger desarrolló el modelo actual basado en probabilidades. Ya no hablamos de órbitas definidas, sino de regiones del espacio donde es más probable encontrar un electrón. Esto llevó a los números cuánticos que describen completamente cada electrón.
El principio de exclusión de Pauli establece que dos electrones en el mismo átomo no pueden tener los cuatro números cuánticos iguales. Es como decir que cada electrón tiene su "dirección" única en el átomo.
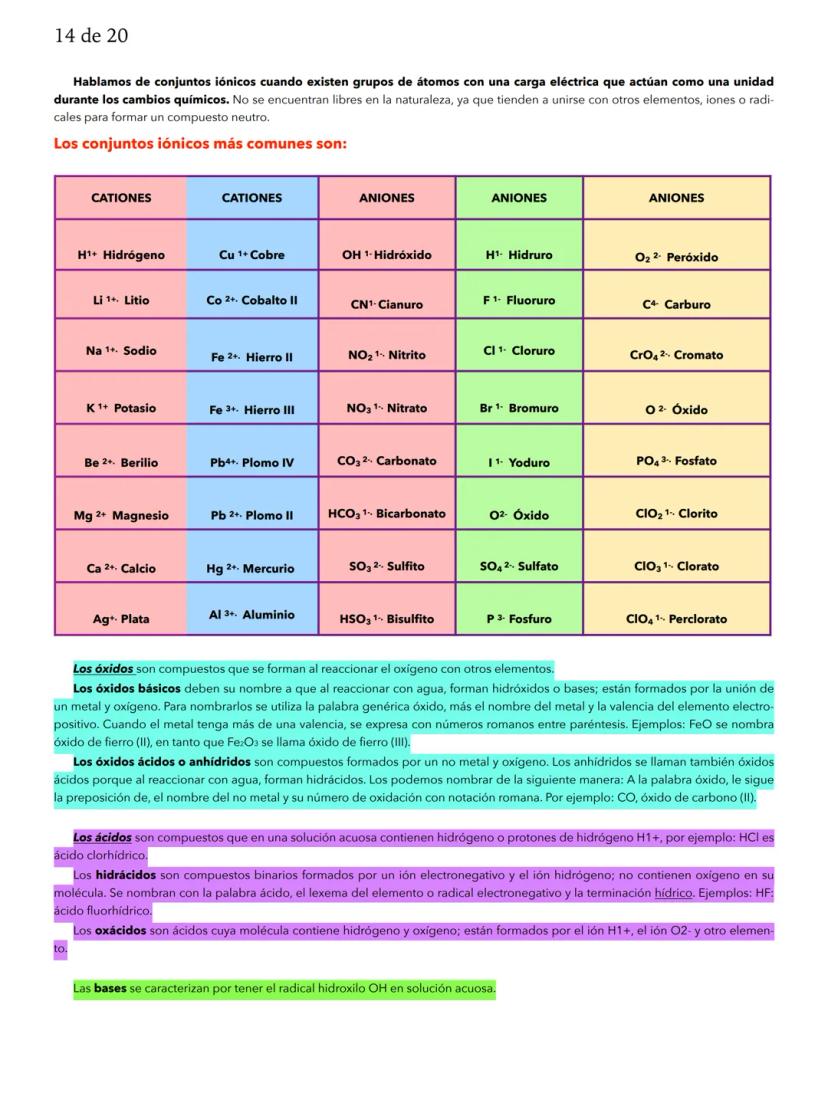
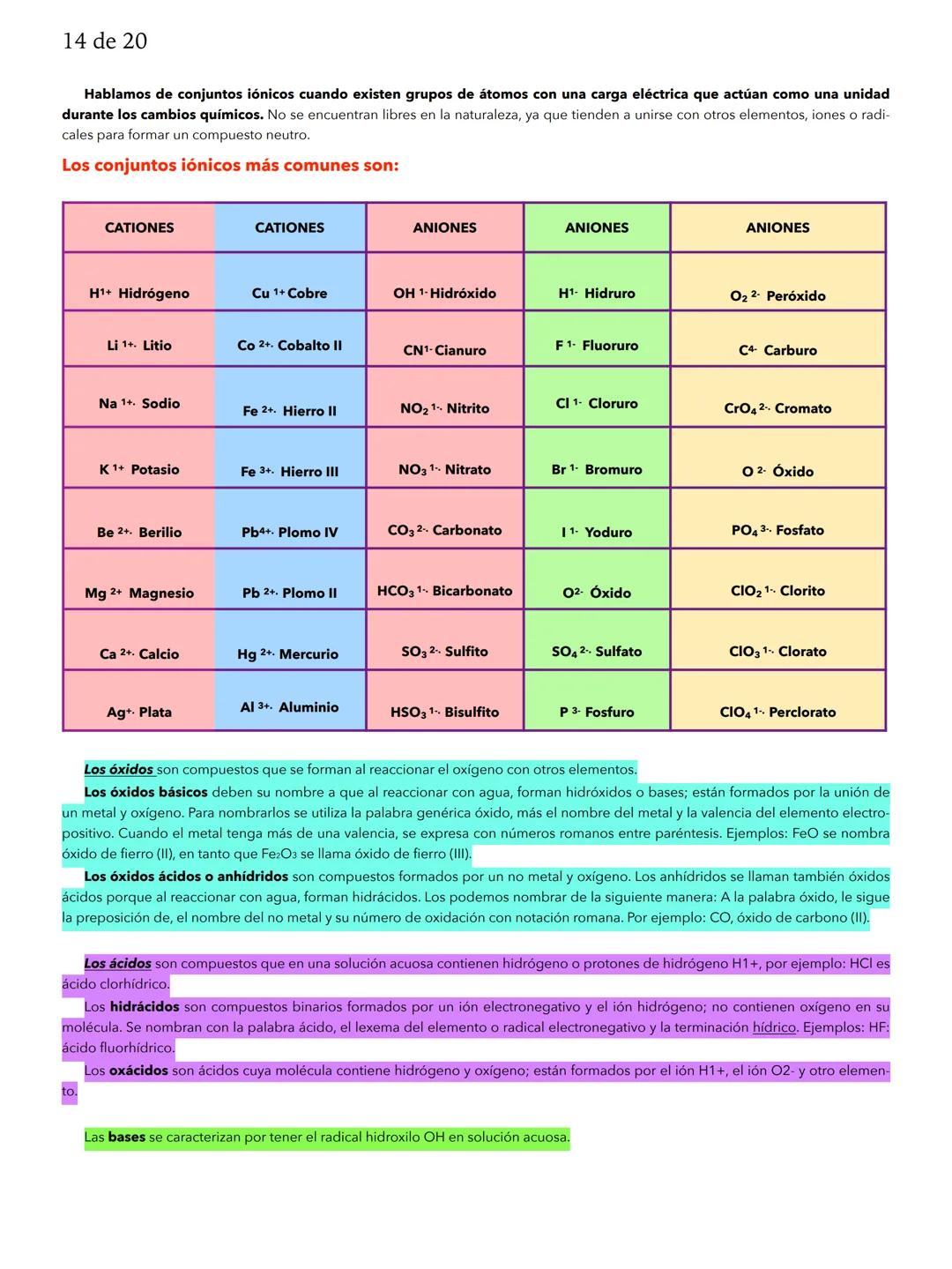
El número atómico (Z) es el número de protones en el núcleo y define qué elemento es. El número de masa (A) suma protones y neutrones. Los iones son átomos que han ganado o perdido electrones: cationes tienen carga positiva, aniones tienen carga negativa.
La valencia es la capacidad de un átomo para combinarse con otros, determinada por los electrones en su nivel externo.
Tip para recordar: Catión = positivo , anión = negativo.

Configuración Electrónica y Estructura de Lewis
Los orbitales son las regiones del espacio donde es más probable encontrar un electrón. Existen diferentes tipos: s (caben 2 electrones), p (caben 6), d (caben 10) y f (caben 14). Los electrones llenan estos orbitales siguiendo un orden específico.
La configuración electrónica te dice cómo están distribuidos los electrones en un átomo. Por ejemplo, el carbono tiene la configuración 1s², 2s², 2p², lo que significa 6 electrones en total. El aluminio tiene 1s², 2s², 2p⁶, 3s², 3p¹ para un total de 13 electrones.
La regla del octeto establece que los átomos tienden a tener 8 electrones en su nivel externo para ser estables (excepto el hidrógeno que solo necesita 2).
La estructura de Lewis es una forma gráfica de representar cómo se enlazan los átomos mostrando los electrones como puntos. En el agua (H₂O), el oxígeno comparte electrones con dos átomos de hidrógeno: H:O:H.
Esta representación te ayuda a visualizar cómo se forman los enlaces químicos y predecir las propiedades de las moléculas.
Truco mnemotécnico: Para recordar el orden de llenado, usa: "1s, 2s, 2p, 3s, 3p, 4s, 3d..." - imagina que subes escalones energéticos.

Tabla Periódica y Clasificación de Elementos
La tabla periódica es el mapa de la química - organiza todos los elementos según sus propiedades y estructura electrónica. Los grupos (columnas verticales) contienen elementos con propiedades similares, mientras que los períodos (filas horizontales) muestran el llenado progresivo de niveles electrónicos.
Los metales alcalinos (Grupo 1: Li, Na, K) son súper reactivos porque tienen un solo electrón en su nivel externo que pierden fácilmente. Los halógenos (Grupo 17: F, Cl, Br, I) son igualmente reactivos pero porque les falta un electrón para completar su octeto.
Los metales ocupan la mayor parte de la tabla (lado izquierdo y centro). Son buenos conductores de electricidad y calor, brillantes cuando se pulen, dúctiles y maleables. Tienden a perder electrones formando cationes.
Los no metales están en el lado derecho de la tabla. Pueden ser sólidos, líquidos o gases, no tienen brillo metálico y son malos conductores. Tienden a ganar electrones formando aniones.
Los metaloides están en la frontera entre metales y no metales, teniendo propiedades intermedias. Son fundamentales en la tecnología moderna, especialmente en semiconductores.
Dato útil: La tabla periódica es como un calendario químico - si sabes la posición de un elemento, puedes predecir muchas de sus propiedades.




Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
Contenidos más populares: Properties of Matter
9Lo principal de la química
¿Que es la Química?
Propiedades Intensivas y Extensivas de la Materia
Describe cuáles son los tipos de propiedades intensivas y extensivas de la materia.
Método científico
Saber información del método científico
Propiedades de la materia
Propiedades de la materia
SUSTANCIAS QUÍMICAS, QUE SON Y SUS CLASIFICACIONES
Descripción de qué son las sustancias quimicas y sus clasificaciones. 💗
Química enlaces químicos
identificar elaces quimicos para relacionar las propiedades de los elementos y su uso enfocado a la aplicación en lso dispositivos eléctricos y electrónicos
quimica general
genral
Propiedades físicas de la materia
Propiedades de la materia, explicación .
Química 1 Bachillerato
Un repasó acerca de los temas de Química 1 a nivel bachillerato para preparación del examen para admisión universidad
Contenidos más populares de Química
9química
química
Mapa metabólico
Mapa metabólico, glucólisis, gluconeogénesis, lípidos, vía de las pentosas, ciclo de krebs
Examen ecoems unam
Estudiar para el examen de ecoems 2026 unam
Quimica ECOEMS(Comipems)
resumen de los temas de quimica que se presentarán en el próximo examen de nivel media superior en la zona metropolitana de el valle de México
Temario y Formulario de Quimica General
Vienen varios conceptos acerca de Quimica General, un apartado de formulas para usarlo de repaso y aplicarlo en ejercicios. Es un resumen de temas relacionados a Quimica General.
LIPIDOS.
RESUMEN
química
propiedades de los elementos, compuestos, reacciones químicas y leyes de la química.
Quimica
Este quiz evalúa tus conocimientos sobre diversos temas de química, desde conceptos básicos hasta reacciones y compuestos.
Método de Tanteo
Balanceo de ecuaciones químicas
Contenidos más populares
9Jerarquía de operaciones
Te enseña la jerarquía de operaciones y también te ecplica que son y como las puedes hacer
química
química
Sistema óseo
Función, tipos, etcétera
Mapa mental - Sistema Nervioso
Mapa mental sobre el sistema nervioso
Célula animal y vegetal
En resumen, este documento te habla sobre qué es, características, diferencias y similitudes de la célula animal y célula vegetal.💗
Matemáticas
matemáticas
Examen mate
matemáticas
Mapa metabólico
Mapa metabólico, glucólisis, gluconeogénesis, lípidos, vía de las pentosas, ciclo de krebs
Historia ECOEMS (Comipems)
Breve resumen de los temas de historia universal del examen del examen de media superior ECOEMS del valle de México
¿No encuentras lo que buscas? Explora otros temas.
Reseñas de nuestros usuarios. Ellos obtuvieron todo lo bueno — y tú también lo harías.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Introducción Básica a la Química
¿Alguna vez te has preguntado por qué el agua hierve o cómo funciona la sal en tu comida? La química es la ciencia que estudia todo lo que nos rodea, desde los materiales más simples hasta las reacciones más complejas.... Mostrar más

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Fundamentos de la Química y Estados de la Materia
La química es la ciencia que estudia la composición, estructura y propiedades de los materiales, así como los cambios que ocurren entre la materia y la energía. Para entender este mundo microscópico, necesitas conocer algunos conceptos básicos que son como el alfabeto de la química.
Un elemento es una sustancia pura formada por átomos iguales que no se puede descomponer en algo más simple. El átomo es la partícula más pequeña de un elemento, como los ladrillos fundamentales de todo lo que existe. Cuando dos o más átomos se unen, forman una molécula.
Los materiales pueden existir en diferentes estados de agregación. Los sólidos tienen sus moléculas muy juntas y casi sin movimiento, manteniendo forma y volumen constantes. Los líquidos se adaptan al recipiente que los contiene pero mantienen su volumen. Los gases no conservan ni forma ni volumen, y se expanden para llenar cualquier espacio.
Dato curioso: Existen dos estados más extremos: el plasma (en las estrellas) y el condensado Bose-Einstein .

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Cambios de Estado y Características de los Materiales
Los cambios de estado son transformaciones físicas que ocurren cuando calientas o enfrías una sustancia. La fusión convierte sólidos en líquidos, la vaporización transforma líquidos en gases, y la sublimación pasa directamente de sólido a gas sin ser líquido.
El conocimiento científico en química se basa en observación sistemática, experimentos rigurosos y datos que pueden repetirse. Esto lo diferencia del conocimiento empírico, que se basa solo en experiencias personales.
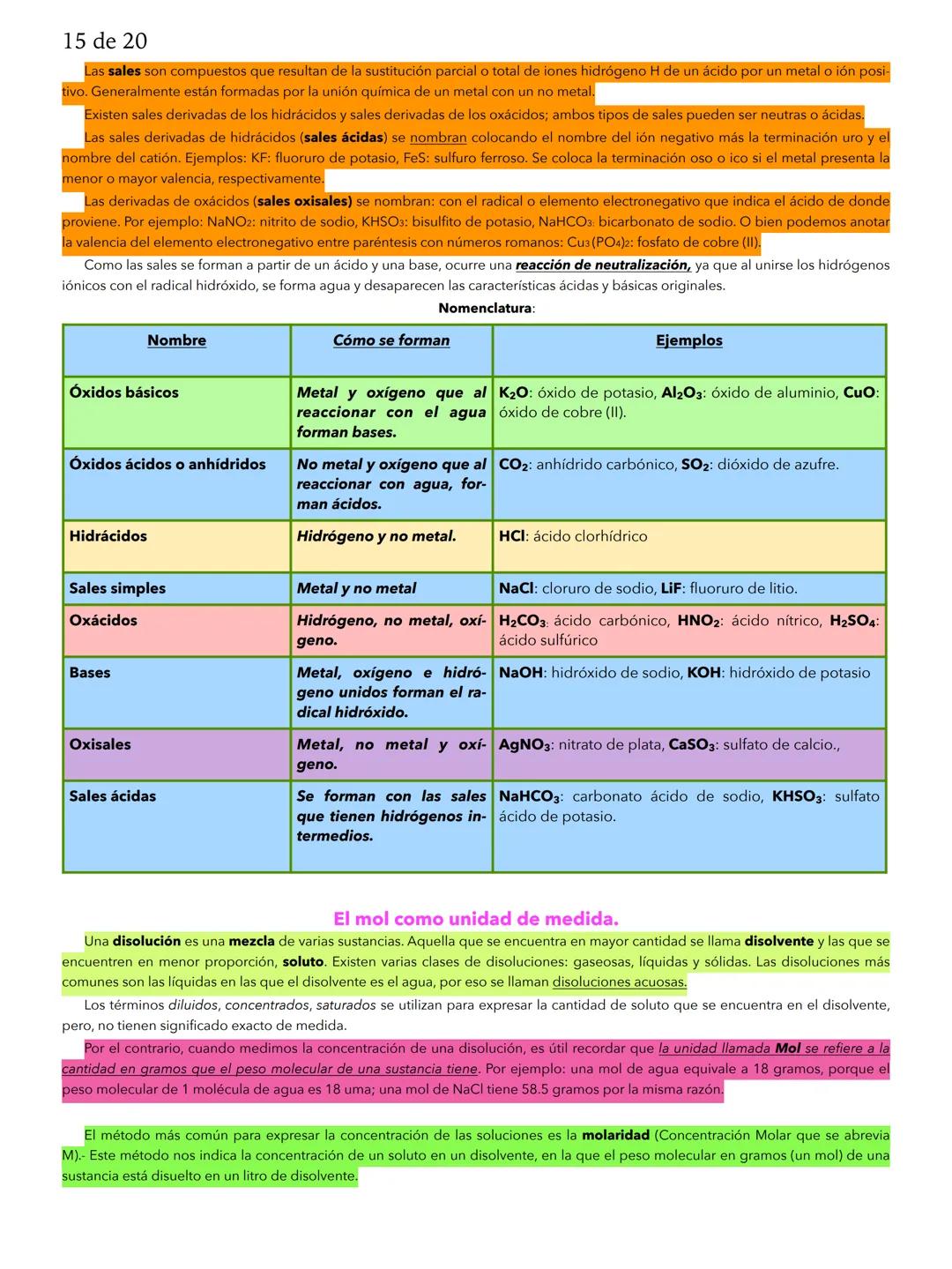
Las propiedades químicas solo se ven durante reacciones químicas, cuando un material se transforma en otro completamente diferente. La acidez y alcalinidad se miden con la escala de pH: números menores a 7 son ácidos (como el limón), 7 es neutro (agua), y mayores a 7 son básicos (como el jabón).
Otras propiedades importantes incluyen la concentración (cantidad de sustancia disuelta), la solubilidad (cuánto se puede disolver) y el estado de oxidación (electrones ganados o perdidos).
Tip para el examen: Memoriza que el agua tiene pH 7 y es neutra, mientras que la sangre tiene pH entre 7.35-7.45.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Escala de pH y Propiedades Químicas Importantes
El pH es fundamental para entender el comportamiento de las sustancias en tu vida diaria. Los valores van de 0 a 14, donde cada número representa qué tan ácida o básica es una sustancia.
Sustancias ácidas que conoces: jugo de limón , refrescos de cola (pH 2.5), café (pH 5.0). Sustancias básicas: jabón , lejía (pH 11.5). La leche tiene pH 6.5, ligeramente ácido, mientras que el agua de mar es básica con pH 8.2.
La afinidad electrónica mide cuánta energía se libera cuando un átomo atrapa un electrón. Los halógenos (como el cloro y el flúor) son excelentes para esto. La concentración te dice qué tan "fuerte" está una solución - imagina un vaso de agua con una cucharada de azúcar versus uno con diez cucharadas.
El tipo de enlace químico determina cómo se unen los átomos: pueden compartir electrones (covalente), transferirlos completamente (iónico), o formar una "nube" de electrones (metálico).
Conexión con la vida real: Tu estómago produce ácido gástrico con pH 2.0, ¡casi tan ácido como el limón!

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Cambios Físicos vs Químicos y Elementos Importantes
Es crucial distinguir entre cambios físicos y cambios químicos. Los cambios físicos no alteran la estructura interna de la materia (como derretir hielo), mientras que los cambios químicos sí la transforman completamente (como quemar madera).
Ahora conocerás algunos elementos clave. El carbono forma diamantes súper duros y también está en el petróleo y en tu cuerpo. El hidrógeno es el gas más ligero y se combina con oxígeno para formar agua. El nitrógeno forma 80% del aire que respiras pero es muy estable debido a sus enlaces triples.
El oxígeno es esencial para la respiración y ayuda a la combustión, pero él mismo no arde. El cloro es ese gas amarillo-verdoso tóxico que se usa para purificar agua. El azufre es amarillo y arde con llama azul brillante.
En cuanto a metales importantes: el hierro se oxida (se herrumbra) y forma la base del acero. El cobre fue el primer metal que usó la humanidad y conduce muy bien la electricidad. El sodio reacciona violentamente con agua. El aluminio es abundante y se usa en utensilios de cocina.
Dato fascinante: El sodio debe guardarse en queroseno porque reacciona tan rápido con el aire y agua que puede explotar.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Conservación de la Masa y Métodos de Separación
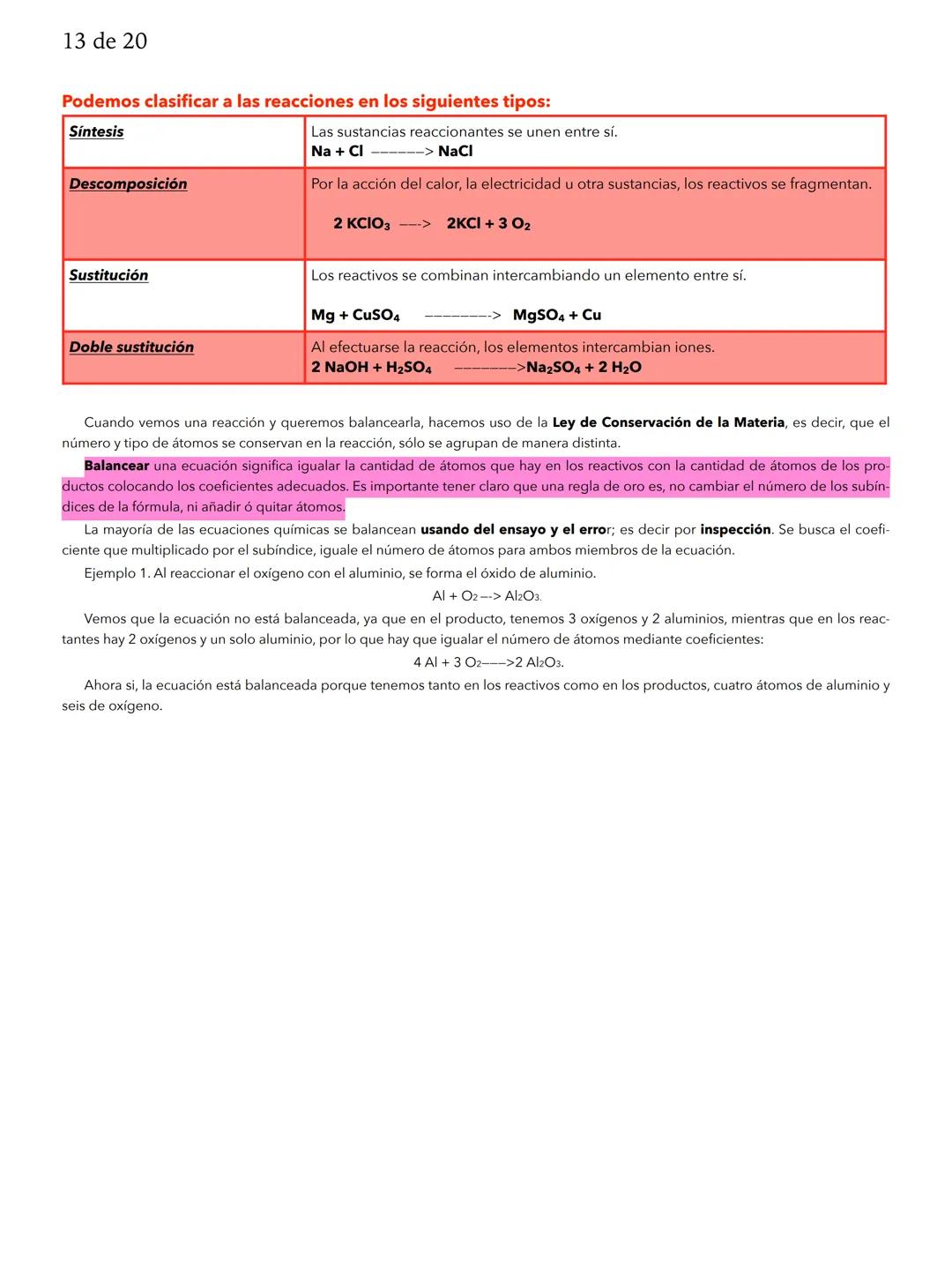
La ley de conservación de la masa de Lavoisier establece que en cualquier reacción química, la masa no se crea ni se destruye, solo se transforma. Si tienes 10 gramos de reactivos, obtienes exactamente 10 gramos de productos.
Las mezclas son uniones físicas (no químicas) de dos o más sustancias que mantienen sus propiedades originales. Las mezclas heterogéneas permiten ver sus componentes a simple vista (como arena y agua), mientras que las homogéneas no (como la leche o el acero).
Para separar mezclas usamos métodos físicos específicos. La decantación usa la gravedad para separar líquidos y sólidos. La filtración emplea papel poroso para retener sólidos. La centrifugación acelera la separación usando fuerza centrífuga.
La evaporación elimina líquidos dejando sólidos, la sublimación separa sustancias que pasan de sólido a gas directamente, y la destilación permite recuperar tanto sólidos como líquidos usando diferentes puntos de ebullición.
Aplicación práctica: Cuando preparas café estás usando filtración, y cuando se evapora agua de mar para obtener sal, es evaporación.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Métodos de Separación y Estados de Agregación
Los métodos de separación son herramientas fundamentales que aprovechan las diferencias en propiedades físicas entre sustancias. Cada método tiene su aplicación específica según el tipo de mezcla que tengas.
La decantación funciona perfectamente cuando tienes aceite y agua, ya que la gravedad separa naturalmente los líquidos de diferente densidad. La centrifugación es como la decantación súper acelerada - imagina cómo funciona una lavadora en el ciclo de centrifugado.
Para separar sólidos de líquidos, la filtración es tu mejor opción. El papel filtro actúa como un colador microscópico que deja pasar el líquido pero retiene las partículas sólidas.
Los métodos que involucran calor son especialmente útiles. La evaporación te permite obtener sal del agua de mar, mientras que la destilación puede separar alcohol del agua porque tienen diferentes puntos de ebullición. La sublimación es perfecta para sustancias especiales como el yodo, que pasa de sólido a gas sin derretirse.
Conexión con tu vida: Cuando tu mamá cuela el café o cuando se seca la ropa al sol, está usando métodos de separación que estudias en química.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Estructura Atómica y Modelos Históricos
Los átomos son los bloques fundamentales de todo lo que existe, compuestos por tres partículas principales. Los protones tienen carga positiva y están en el núcleo, los neutrones no tienen carga y también están en el núcleo, mientras que los electrones con carga negativa giran alrededor del núcleo.
La historia de los modelos atómicos es fascinante. Dalton (1808) imaginó los átomos como esferas sólidas indivisibles. Thomson (1897) descubrió los electrones y propuso el modelo del "pastel con pasas" - electrones incrustados en una masa positiva.
Rutherford (1911) revolucionó todo con sus experimentos disparando partículas contra láminas de oro. Descubrió que los átomos tienen un núcleo diminuto y denso rodeado de mucho espacio vacío. Su modelo planetario mostraba electrones orbitando como planetas alrededor del sol.
Bohr (1913) mejoró el modelo estableciendo que los electrones se mueven en órbitas específicas con niveles de energía definidos: K, L, M, N, O, P, Q. Solo pueden "brincar" entre estos niveles, emitiendo luz en el proceso.
Dato increíble: Si el núcleo fuera del tamaño de una pelota de fútbol, los electrones estarían girando a kilómetros de distancia.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Modelos Atómicos Modernos y Conceptos Fundamentales
Los modelos atómicos evolucionaron hacia conceptos más complejos y precisos. Sommerfeld introdujo las órbitas elípticas, mientras que De Broglie estableció que los electrones se comportan como ondas y partículas al mismo tiempo.
Schrödinger desarrolló el modelo actual basado en probabilidades. Ya no hablamos de órbitas definidas, sino de regiones del espacio donde es más probable encontrar un electrón. Esto llevó a los números cuánticos que describen completamente cada electrón.
El principio de exclusión de Pauli establece que dos electrones en el mismo átomo no pueden tener los cuatro números cuánticos iguales. Es como decir que cada electrón tiene su "dirección" única en el átomo.
El número atómico (Z) es el número de protones en el núcleo y define qué elemento es. El número de masa (A) suma protones y neutrones. Los iones son átomos que han ganado o perdido electrones: cationes tienen carga positiva, aniones tienen carga negativa.
La valencia es la capacidad de un átomo para combinarse con otros, determinada por los electrones en su nivel externo.
Tip para recordar: Catión = positivo , anión = negativo.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Configuración Electrónica y Estructura de Lewis
Los orbitales son las regiones del espacio donde es más probable encontrar un electrón. Existen diferentes tipos: s (caben 2 electrones), p (caben 6), d (caben 10) y f (caben 14). Los electrones llenan estos orbitales siguiendo un orden específico.
La configuración electrónica te dice cómo están distribuidos los electrones en un átomo. Por ejemplo, el carbono tiene la configuración 1s², 2s², 2p², lo que significa 6 electrones en total. El aluminio tiene 1s², 2s², 2p⁶, 3s², 3p¹ para un total de 13 electrones.
La regla del octeto establece que los átomos tienden a tener 8 electrones en su nivel externo para ser estables (excepto el hidrógeno que solo necesita 2).
La estructura de Lewis es una forma gráfica de representar cómo se enlazan los átomos mostrando los electrones como puntos. En el agua (H₂O), el oxígeno comparte electrones con dos átomos de hidrógeno: H:O:H.
Esta representación te ayuda a visualizar cómo se forman los enlaces químicos y predecir las propiedades de las moléculas.
Truco mnemotécnico: Para recordar el orden de llenado, usa: "1s, 2s, 2p, 3s, 3p, 4s, 3d..." - imagina que subes escalones energéticos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Tabla Periódica y Clasificación de Elementos
La tabla periódica es el mapa de la química - organiza todos los elementos según sus propiedades y estructura electrónica. Los grupos (columnas verticales) contienen elementos con propiedades similares, mientras que los períodos (filas horizontales) muestran el llenado progresivo de niveles electrónicos.
Los metales alcalinos (Grupo 1: Li, Na, K) son súper reactivos porque tienen un solo electrón en su nivel externo que pierden fácilmente. Los halógenos (Grupo 17: F, Cl, Br, I) son igualmente reactivos pero porque les falta un electrón para completar su octeto.
Los metales ocupan la mayor parte de la tabla (lado izquierdo y centro). Son buenos conductores de electricidad y calor, brillantes cuando se pulen, dúctiles y maleables. Tienden a perder electrones formando cationes.
Los no metales están en el lado derecho de la tabla. Pueden ser sólidos, líquidos o gases, no tienen brillo metálico y son malos conductores. Tienden a ganar electrones formando aniones.
Los metaloides están en la frontera entre metales y no metales, teniendo propiedades intermedias. Son fundamentales en la tecnología moderna, especialmente en semiconductores.
Dato útil: La tabla periódica es como un calendario químico - si sabes la posición de un elemento, puedes predecir muchas de sus propiedades.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
Contenidos más populares: Properties of Matter
9Lo principal de la química
¿Que es la Química?
Propiedades Intensivas y Extensivas de la Materia
Describe cuáles son los tipos de propiedades intensivas y extensivas de la materia.
Método científico
Saber información del método científico
Propiedades de la materia
Propiedades de la materia
SUSTANCIAS QUÍMICAS, QUE SON Y SUS CLASIFICACIONES
Descripción de qué son las sustancias quimicas y sus clasificaciones. 💗
Química enlaces químicos
identificar elaces quimicos para relacionar las propiedades de los elementos y su uso enfocado a la aplicación en lso dispositivos eléctricos y electrónicos
quimica general
genral
Propiedades físicas de la materia
Propiedades de la materia, explicación .
Química 1 Bachillerato
Un repasó acerca de los temas de Química 1 a nivel bachillerato para preparación del examen para admisión universidad
Contenidos más populares de Química
9química
química
Mapa metabólico
Mapa metabólico, glucólisis, gluconeogénesis, lípidos, vía de las pentosas, ciclo de krebs
Examen ecoems unam
Estudiar para el examen de ecoems 2026 unam
Quimica ECOEMS(Comipems)
resumen de los temas de quimica que se presentarán en el próximo examen de nivel media superior en la zona metropolitana de el valle de México
Temario y Formulario de Quimica General
Vienen varios conceptos acerca de Quimica General, un apartado de formulas para usarlo de repaso y aplicarlo en ejercicios. Es un resumen de temas relacionados a Quimica General.
LIPIDOS.
RESUMEN
química
propiedades de los elementos, compuestos, reacciones químicas y leyes de la química.
Quimica
Este quiz evalúa tus conocimientos sobre diversos temas de química, desde conceptos básicos hasta reacciones y compuestos.
Método de Tanteo
Balanceo de ecuaciones químicas
Contenidos más populares
9Jerarquía de operaciones
Te enseña la jerarquía de operaciones y también te ecplica que son y como las puedes hacer
química
química
Sistema óseo
Función, tipos, etcétera
Mapa mental - Sistema Nervioso
Mapa mental sobre el sistema nervioso
Célula animal y vegetal
En resumen, este documento te habla sobre qué es, características, diferencias y similitudes de la célula animal y célula vegetal.💗
Matemáticas
matemáticas
Examen mate
matemáticas
Mapa metabólico
Mapa metabólico, glucólisis, gluconeogénesis, lípidos, vía de las pentosas, ciclo de krebs
Historia ECOEMS (Comipems)
Breve resumen de los temas de historia universal del examen del examen de media superior ECOEMS del valle de México
¿No encuentras lo que buscas? Explora otros temas.
Reseñas de nuestros usuarios. Ellos obtuvieron todo lo bueno — y tú también lo harías.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.