El agua es mucho más que solo H₂O: es la... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Knowunity AI
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
244
•
Actualizado Mar 30, 2026
•
KAREN GUADALUPE CELEDON SANTANA
@karenguadalupec
El agua es mucho más que solo H₂O: es la... Mostrar más








¿Sabías que una sola gota de agua contiene millones de moléculas que se deslizan unas sobre otras? La molécula de agua (H₂O) está formada por dos átomos de hidrógeno unidos a uno de oxígeno mediante enlaces covalentes.
El agua es conocida como el disolvente universal porque puede disolver más sustancias que cualquier otro líquido. Esto sucede gracias a su carácter polar, que le permite formar puentes de hidrógeno con otras moléculas. Sin embargo, no puede disolver grasas y aceites, que son hidrofóbicas.
Sus propiedades físicas más importantes incluyen: una capacidad calorífica de 1 kcal/kg°C (puede absorber mucho calor), densidad de 1 kg/L, temperatura de ebullición de 100°C y temperatura de fusión de 0°C. Estas características se deben completamente a su estructura molecular única.
💡 Tip de estudio: Recuerda que todas las propiedades del agua se explican por su estructura: dos hidrógenos + un oxígeno = propiedades extraordinarias.
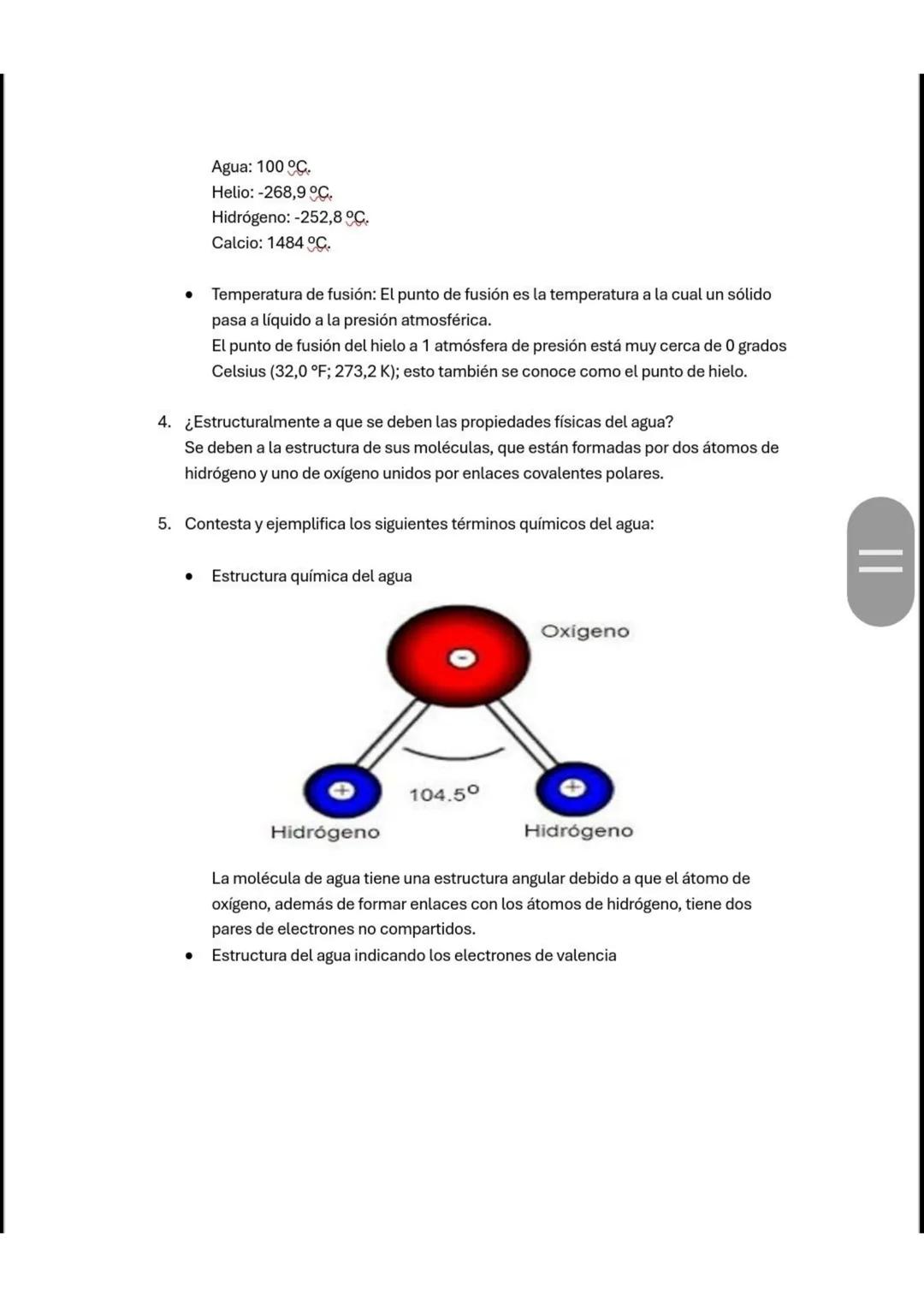
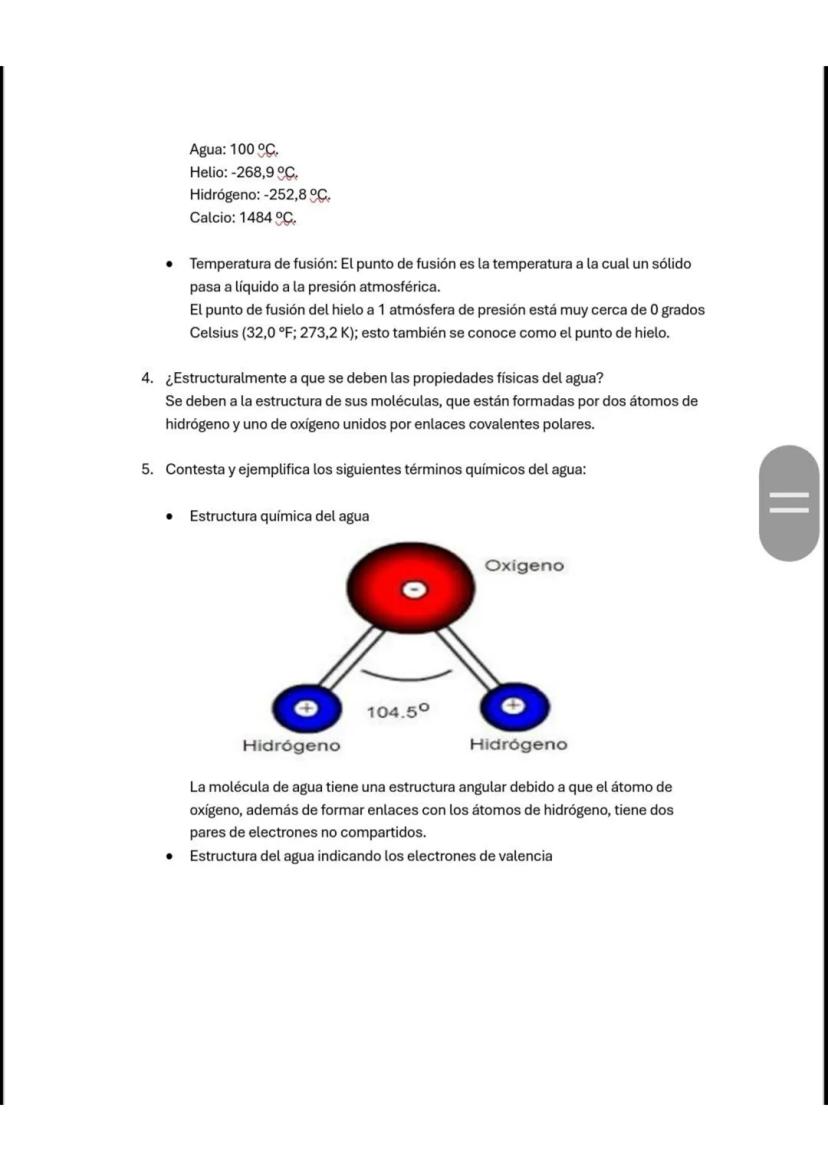
La estructura angular del agua es clave para entender por qué es tan especial. El oxígeno no solo se une a los hidrógenos, sino que también tiene dos pares de electrones no compartidos que crean un ángulo de 104.5°.
Esta forma angular hace que el agua sea un dipolo: tiene un extremo positivo (hidrógenos) y uno negativo (oxígeno). La polarización ocurre porque el oxígeno atrae más fuertemente a los electrones que el hidrógeno, creando cargas parciales.
Los puentes de hidrógeno se forman cuando el lado positivo de una molécula de agua se atrae al lado negativo de otra. Esta es la razón por la cual las moléculas de agua tienden a "pegarse" entre sí, creando las propiedades únicas que conocemos.
💡 Conexión real: Los puentes de hidrógeno explican por qué el agua tiene tensión superficial y por qué algunos insectos pueden caminar sobre ella.

La hidrosolubilidad es la capacidad de una sustancia para disolverse en agua. Se puede medir usando curvas de solubilidad, unidades de concentración como la molaridad, o expresando gramos de soluto por litro de disolvente.
La solvatación es cuando las moléculas de agua rodean completamente a un soluto para disolverlo. Por ejemplo, cuando agregas azúcar al agua, las moléculas de agua envuelven cada molécula de azúcar mediante puentes de hidrógeno.
Los factores que alteran la solvatación son: la temperatura (generalmente aumenta la solubilidad), la presión (afecta principalmente a gases), y la naturaleza del soluto y disolvente (las sustancias pueden ser hidrosolubles o liposolubles).
Las dispersiones incluyen emulsiones (agua y aceite), soles (como la sangre), y suspensiones (partículas sólidas en líquido). Estas son diferentes a las soluciones porque tienen múltiples fases visibles.
💡 Para recordar: "Lo similar disuelve a lo similar" - las sustancias polares se disuelven en agua (polar), las no polares en aceites.

La ósmosis es el movimiento del agua a través de una membrana semipermeable, desde donde hay menos solutos hacia donde hay más. Es como si el agua "quisiera" igualar las concentraciones a ambos lados.
La presión osmótica es la fuerza necesaria para detener este movimiento de agua. La tonicidad describe cómo las soluciones afectan el volumen celular según su concentración de solutos.
Existen tres tipos de soluciones importantes:
Los electrolitos como sodio, potasio y cloruro tienen concentraciones específicas dentro y fuera de las células. El sodio es mayor afuera mientras que el potasio es mayor adentro .
💡 Aplicación médica: Los sueros hospitalarios son isotónicos para no dañar tus células al administrarse.

Un ácido libera iones H⁺ en agua (como el ácido acético del vinagre), mientras que una base acepta estos iones (como el amoniaco). Las sales se forman cuando ácidos y bases se neutralizan (como el cloruro de sodio).
La ionización del agua produce tanto iones H⁺ como OH⁻, lo que permite que el agua actúe como ácido o como base según las circunstancias. Esto se llama comportamiento anfótero.
El pH (potencial de hidrógeno) se mide en una escala de 0 a 14:
La fórmula para calcular pH es: pH = -log[H⁺], donde [H⁺] es la concentración de iones hidrógeno.
💡 Dato curioso: El pH de tu sangre debe mantenerse entre 7.35-7.45. Cambios pequeños pueden ser mortales.

El pH en sistemas biológicos es crítico porque cada órgano funciona solo dentro de rangos específicos. Tu sangre tiene pH 7.4, mientras que el interior celular tiene pH 7.2.
Los amortiguadores biológicos son sustancias que mantienen el pH estable cuando consumes algo ácido o básico. Son como "esponjas" que absorben el exceso de H⁺ u OH⁻ para proteger tus células.
Las alteraciones del pH indican problemas de salud:
El agua representa el 80% de la composición de la mayoría de los organismos e interviene en prácticamente todos los procesos metabólicos de tu cuerpo.
💡 Conexión vital: Mantener el equilibrio del pH es tan importante que tu cuerpo tiene múltiples sistemas trabajando 24/7 para lograrlo.


Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener dificultades para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuario de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser muy difícil reunir toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis notas y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuario de Android
Siempre estaba estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a manejar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZZES Y FLASHCARDS SON SÚPER ÚTILES Y AMO Knowunity AI. TAMBIÉN ES LITERALMENTE COMO CHATGPT PERO MÁS INTELIGENTE!! ME AYUDÓ CON MIS PROBLEMAS DE RÍMEL TAMBIÉN!! Y CON MIS MATERIAS REALES OBVIO! 😍😁😲🤑💗✨🎀😮
Sarah L
usuario de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros – me siento mucho más seguro cuando me preparo para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener dificultades para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuario de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser muy difícil reunir toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis notas y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuario de Android
Siempre estaba estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a manejar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZZES Y FLASHCARDS SON SÚPER ÚTILES Y AMO Knowunity AI. TAMBIÉN ES LITERALMENTE COMO CHATGPT PERO MÁS INTELIGENTE!! ME AYUDÓ CON MIS PROBLEMAS DE RÍMEL TAMBIÉN!! Y CON MIS MATERIAS REALES OBVIO! 😍😁😲🤑💗✨🎀😮
Sarah L
usuario de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros – me siento mucho más seguro cuando me preparo para los exámenes.
Paul T
usuario de iOS
KAREN GUADALUPE CELEDON SANTANA
@karenguadalupec
El agua es mucho más que solo H₂O: es la base de la vida y tiene propiedades únicas que la hacen indispensable para todos los procesos biológicos. Entender su estructura molecular y comportamiento te ayudará a comprender mejor cómo funciona... Mostrar más

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
¿Sabías que una sola gota de agua contiene millones de moléculas que se deslizan unas sobre otras? La molécula de agua (H₂O) está formada por dos átomos de hidrógeno unidos a uno de oxígeno mediante enlaces covalentes.
El agua es conocida como el disolvente universal porque puede disolver más sustancias que cualquier otro líquido. Esto sucede gracias a su carácter polar, que le permite formar puentes de hidrógeno con otras moléculas. Sin embargo, no puede disolver grasas y aceites, que son hidrofóbicas.
Sus propiedades físicas más importantes incluyen: una capacidad calorífica de 1 kcal/kg°C (puede absorber mucho calor), densidad de 1 kg/L, temperatura de ebullición de 100°C y temperatura de fusión de 0°C. Estas características se deben completamente a su estructura molecular única.
💡 Tip de estudio: Recuerda que todas las propiedades del agua se explican por su estructura: dos hidrógenos + un oxígeno = propiedades extraordinarias.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La estructura angular del agua es clave para entender por qué es tan especial. El oxígeno no solo se une a los hidrógenos, sino que también tiene dos pares de electrones no compartidos que crean un ángulo de 104.5°.
Esta forma angular hace que el agua sea un dipolo: tiene un extremo positivo (hidrógenos) y uno negativo (oxígeno). La polarización ocurre porque el oxígeno atrae más fuertemente a los electrones que el hidrógeno, creando cargas parciales.
Los puentes de hidrógeno se forman cuando el lado positivo de una molécula de agua se atrae al lado negativo de otra. Esta es la razón por la cual las moléculas de agua tienden a "pegarse" entre sí, creando las propiedades únicas que conocemos.
💡 Conexión real: Los puentes de hidrógeno explican por qué el agua tiene tensión superficial y por qué algunos insectos pueden caminar sobre ella.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La hidrosolubilidad es la capacidad de una sustancia para disolverse en agua. Se puede medir usando curvas de solubilidad, unidades de concentración como la molaridad, o expresando gramos de soluto por litro de disolvente.
La solvatación es cuando las moléculas de agua rodean completamente a un soluto para disolverlo. Por ejemplo, cuando agregas azúcar al agua, las moléculas de agua envuelven cada molécula de azúcar mediante puentes de hidrógeno.
Los factores que alteran la solvatación son: la temperatura (generalmente aumenta la solubilidad), la presión (afecta principalmente a gases), y la naturaleza del soluto y disolvente (las sustancias pueden ser hidrosolubles o liposolubles).
Las dispersiones incluyen emulsiones (agua y aceite), soles (como la sangre), y suspensiones (partículas sólidas en líquido). Estas son diferentes a las soluciones porque tienen múltiples fases visibles.
💡 Para recordar: "Lo similar disuelve a lo similar" - las sustancias polares se disuelven en agua (polar), las no polares en aceites.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La ósmosis es el movimiento del agua a través de una membrana semipermeable, desde donde hay menos solutos hacia donde hay más. Es como si el agua "quisiera" igualar las concentraciones a ambos lados.
La presión osmótica es la fuerza necesaria para detener este movimiento de agua. La tonicidad describe cómo las soluciones afectan el volumen celular según su concentración de solutos.
Existen tres tipos de soluciones importantes:
Los electrolitos como sodio, potasio y cloruro tienen concentraciones específicas dentro y fuera de las células. El sodio es mayor afuera mientras que el potasio es mayor adentro .
💡 Aplicación médica: Los sueros hospitalarios son isotónicos para no dañar tus células al administrarse.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Un ácido libera iones H⁺ en agua (como el ácido acético del vinagre), mientras que una base acepta estos iones (como el amoniaco). Las sales se forman cuando ácidos y bases se neutralizan (como el cloruro de sodio).
La ionización del agua produce tanto iones H⁺ como OH⁻, lo que permite que el agua actúe como ácido o como base según las circunstancias. Esto se llama comportamiento anfótero.
El pH (potencial de hidrógeno) se mide en una escala de 0 a 14:
La fórmula para calcular pH es: pH = -log[H⁺], donde [H⁺] es la concentración de iones hidrógeno.
💡 Dato curioso: El pH de tu sangre debe mantenerse entre 7.35-7.45. Cambios pequeños pueden ser mortales.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El pH en sistemas biológicos es crítico porque cada órgano funciona solo dentro de rangos específicos. Tu sangre tiene pH 7.4, mientras que el interior celular tiene pH 7.2.
Los amortiguadores biológicos son sustancias que mantienen el pH estable cuando consumes algo ácido o básico. Son como "esponjas" que absorben el exceso de H⁺ u OH⁻ para proteger tus células.
Las alteraciones del pH indican problemas de salud:
El agua representa el 80% de la composición de la mayoría de los organismos e interviene en prácticamente todos los procesos metabólicos de tu cuerpo.
💡 Conexión vital: Mantener el equilibrio del pH es tan importante que tu cuerpo tiene múltiples sistemas trabajando 24/7 para lograrlo.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
2
Herramientas Inteligentes NUEVO
Convierte estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Tarjetas de Estudio Interactivas ✓ Examen Completo de Práctica ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener dificultades para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuario de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser muy difícil reunir toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis notas y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuario de Android
Siempre estaba estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a manejar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZZES Y FLASHCARDS SON SÚPER ÚTILES Y AMO Knowunity AI. TAMBIÉN ES LITERALMENTE COMO CHATGPT PERO MÁS INTELIGENTE!! ME AYUDÓ CON MIS PROBLEMAS DE RÍMEL TAMBIÉN!! Y CON MIS MATERIAS REALES OBVIO! 😍😁😲🤑💗✨🎀😮
Sarah L
usuario de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros – me siento mucho más seguro cuando me preparo para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener dificultades para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuario de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser muy difícil reunir toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis notas y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuario de Android
Siempre estaba estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a manejar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZZES Y FLASHCARDS SON SÚPER ÚTILES Y AMO Knowunity AI. TAMBIÉN ES LITERALMENTE COMO CHATGPT PERO MÁS INTELIGENTE!! ME AYUDÓ CON MIS PROBLEMAS DE RÍMEL TAMBIÉN!! Y CON MIS MATERIAS REALES OBVIO! 😍😁😲🤑💗✨🎀😮
Sarah L
usuario de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros – me siento mucho más seguro cuando me preparo para los exámenes.
Paul T
usuario de iOS