¿Alguna vez te has preguntado de qué están hechas todas... Mostrar más
Guía fácil: Estructura atómica, modelos y enlaces químicos explicados










Fundamentos Atómicos: Las Piezas del Rompecabezas
Imagínate que tienes superpoderes para ver las cosas más pequeñas del universo. Lo primero que encontrarías sería el átomo, la partícula más pequeña de cualquier sustancia que no se puede descomponer químicamente.
Cada átomo es como una mini ciudad con un núcleo en el centro (formado por protones con carga positiva y neutrones sin carga) y electrones con carga negativa girando alrededor. Lo genial es que cada elemento tiene un número único de protones, como si fuera su huella digital.
Los científicos Bohr y Sommerfield nos ayudaron a entender que los electrones no andan perdidos por ahí, sino que viven en niveles energéticos específicos alrededor del núcleo. Es como si cada electrón tuviera su propio carril asignado en una pista de carreras circular o elíptica.
Dato curioso: El sodio (Na) tiene 11 protones, así que también tiene 11 electrones cuando está en equilibrio. ¡Es como un sistema perfectamente balanceado!

Modelos Atómicos en Acción
Los modelos atómicos son como mapas que nos muestran dónde viven los electrones en diferentes elementos. El modelo de Bohr nos dice que los electrones están en niveles específicos, mientras que Sommerfield añadió que pueden moverse en órbitas circulares o elípticas.
Cuando hablamos del electrón, estamos hablando de una partícula súper pequeña con carga negativa que no se puede dividir más. Es uno de los bloques fundamentales de la materia, representado por el símbolo "e⁻".
Para elementos como el hidrógeno (H), que solo tiene un electrón, es fácil visualizar cómo funciona este sistema. Ese electrón único orbita alrededor del núcleo siguiendo las reglas que descubrieron estos científicos.
Tip de estudio: Dibuja los modelos atómicos con colores diferentes para cada nivel energético. Te ayudará a recordar cómo se distribuyen los electrones.

Electrones de Valencia y Formación de Iones
Los electrones de valencia son los electrones VIP del átomo porque viven en el nivel de energía más externo. Estos son los que realmente importan cuando los átomos quieren hacer amigos (formar enlaces químicos).
La capa de valencia es como la "zona de contacto" del átomo. El número de electrones en esta capa determina qué tan sociable será tu átomo y con quién se va a juntar. Es la clave para predecir el comportamiento químico.
Cuando un átomo gana o pierde electrones, se convierte en un ion. Los cationes son iones con carga positiva (perdieron electrones), mientras que los aniones tienen carga negativa (ganaron electrones). Es como si el átomo fuera una persona que puede tener más o menos dinero de lo normal.
Recuerda: Un átomo neutro tiene el mismo número de protones y electrones. ¡Cuando este equilibrio se rompe, nacen los iones!

Enlaces Químicos: Cuando los Átomos se Unen
Los enlaces químicos son las fuerzas invisibles que mantienen unidos a los átomos, como el pegamento molecular que crea todo lo que existe. Sin estos enlaces, no existirían las moléculas ni los compuestos.
El enlace iónico se forma cuando un átomo cede electrones y otro los recibe, creando iones con cargas opuestas que se atraen. Es como el romance entre el sodio (Na⁺) y el cloro (Cl⁻) que forma la sal de mesa (NaCl).
En este tipo de enlace, el metal (como el sodio) pierde electrones y se vuelve catión, mientras que el no metal (como el cloro) gana esos electrones y se convierte en anión. La atracción electrostática entre cargas opuestas los mantiene unidos.
Visualízalo: Imagina que el sodio le regala un electrón al cloro. Ahora el sodio queda positivo y el cloro negativo, ¡y se atraen como imanes opuestos!

Enlaces Covalentes: Compartir es Vivir
El enlace covalente funciona diferente: aquí los átomos comparten electrones en lugar de regalarlos. Es como dos amigos que comparten sus juguetes para que ambos puedan jugar.
En el enlace covalente no polar, los átomos comparten los electrones de manera equitativa. Esto pasa cuando se unen átomos iguales (como H₂) o con electronegatividades muy similares.
El átomo de hidrógeno es el más simple: un protón en el núcleo y un electrón girando alrededor. Cuando dos átomos de hidrógeno se juntan, comparten sus electrones formando H₂, donde cada átomo siente que tiene dos electrones.
Dato interesante: En la molécula H₂, cada átomo de hidrógeno contribuye con un electrón, y ambos comparten ese par equitativamente.

Enlaces Covalentes Polares y el Agua
Los enlaces covalentes polares se forman cuando los átomos no comparten los electrones de manera equitativa. Uno de los átomos "jala" más fuerte a los electrones, creando polos positivo y negativo.
El agua (H₂O) es el ejemplo perfecto de esto. El oxígeno es más "comelón" de electrones que el hidrógeno, así que atrae más hacia él los electrones compartidos. Esto hace que el oxígeno quede ligeramente negativo y los hidrógenos ligeramente positivos.
Este tipo de enlace explica por qué el agua tiene propiedades tan especiales. Los enlaces de hidrógeno se forman cuando el hidrógeno de una molécula se siente atraído hacia átomos electronegativos de otras moléculas.
Aplicación real: Las propiedades únicas del agua (como su punto de ebullición alto) se deben a estos enlaces polares y de hidrógeno.

Enlaces Especiales: Coordinado y Metálico
El enlace covalente coordinado es como un acto de generosidad extrema: un átomo aporta ambos electrones del par compartido, mientras el otro solo ofrece el espacio. Es menos común pero súper importante en ciertos compuestos.
El enlace metálico es exclusivo de los metales y funciona como una "sopa de electrones". Los átomos metálicos liberan sus electrones de valencia, creando un "mar de electrones" que se mueve libremente entre los cationes metálicos.
Este tipo de enlace explica por qué los metales brillan, conducen electricidad y calor, y son maleables. Los electrones libres pueden moverse fácilmente, transmitiendo energía y permitiendo que el metal se deforme sin romperse.
Conexión real: Cuando tocas algo metálico frío, los electrones libres transmiten rápidamente el calor de tu mano, por eso se siente más frío que otros materiales.

Herramientas para Entender los Enlaces
Las estructuras de Lewis son como diagramas que muestran cómo se distribuyen los electrones en las moléculas. Usas puntos para electrones solitarios y líneas para enlaces, creando un mapa visual de la molécula.
La regla del octeto dice que los átomos son más felices cuando tienen 8 electrones en su capa de valencia. Es como si cada átomo quisiera tener su "octet completo" para sentirse estable y seguro.
La electronegatividad mide qué tan "comelón" es un átomo de electrones. Los elementos más electronegativos (como el flúor) atraen fuertemente los electrones, mientras que otros (como el cesio) los ceden fácilmente.
Tip de examen: La electronegatividad aumenta hacia la derecha y hacia arriba en la tabla periódica. ¡El flúor es el más electrónegativo de todos!

Propiedades Periódicas Clave
La afinidad electrónica es la energía que se libera cuando un átomo neutral atrapa un electrón extra. Es como medir qué tan "feliz" se pone un átomo al recibir un electrón adicional.
El radio iónico nos dice qué tan grande es un ion comparado con su átomo original. Los cationes son más pequeños (perdieron electrones) y los aniones son más grandes (ganaron electrones).
El radio atómico es simplemente el tamaño del átomo. Esta propiedad sigue patrones predecibles en la tabla periódica: aumenta hacia abajo y hacia la izquierda.
El número de oxidación indica cuántos electrones puede ganar, perder o compartir un átomo. Es como su "capacidad de negociación" en las reacciones químicas.
Regla práctica: Para encontrar números de oxidación, recuerda que la suma de todos los números de oxidación en un compuesto neutro debe ser cero.
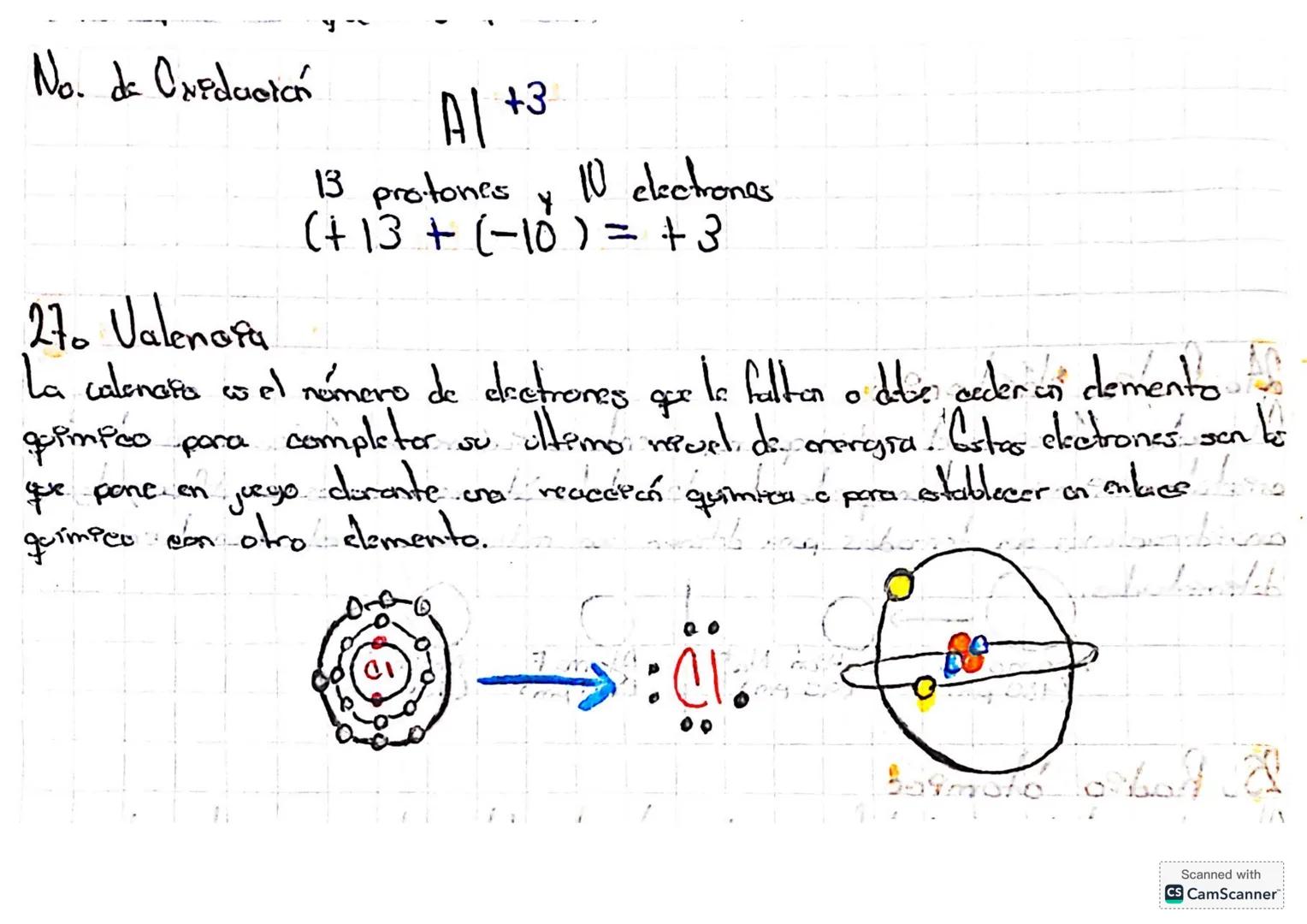
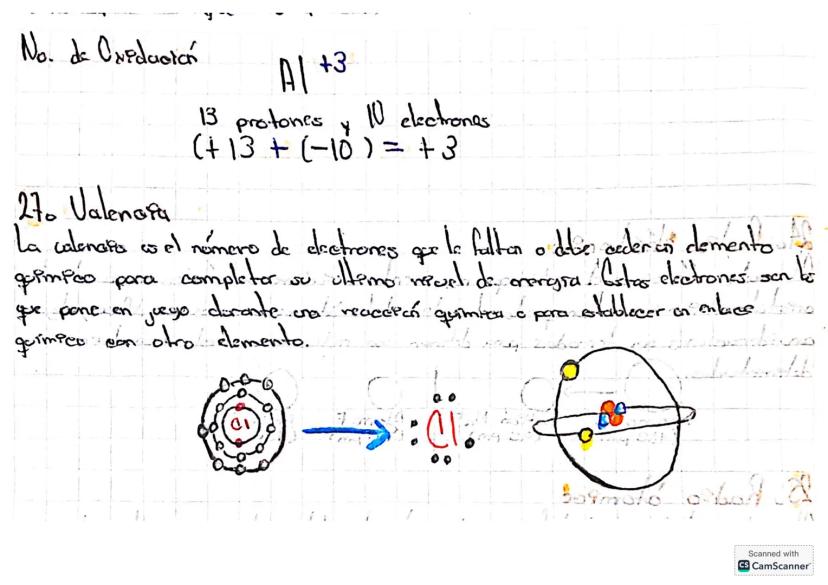
Valencia: La Capacidad de Combinación
La valencia es el número de electrones que un elemento necesita ganar, perder o compartir para completar su capa de valencia. Es como conocer cuántos "asientos vacíos" tiene disponibles para hacer enlaces.
Por ejemplo, el aluminio (Al³⁺) tiene valencia +3 porque puede ceder 3 electrones. Esto significa que tiene 13 protones pero solo 10 electrones, dándole esa carga positiva característica.
Entender la valencia te ayuda a predecir qué tipos de compuestos puede formar cada elemento y en qué proporciones. Es una herramienta súper útil para balancear ecuaciones químicas y entender fórmulas.
Consejo final: Memoriza las valencias más comunes de los elementos que estudias frecuentemente. Te ahorrará mucho tiempo en los exámenes y problemas.
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
Contenidos más populares de Química
9química
química
Mapa metabólico
Mapa metabólico, glucólisis, gluconeogénesis, lípidos, vía de las pentosas, ciclo de krebs
Examen ecoems unam
Estudiar para el examen de ecoems 2026 unam
Quimica ECOEMS(Comipems)
resumen de los temas de quimica que se presentarán en el próximo examen de nivel media superior en la zona metropolitana de el valle de México
Método de Tanteo
Balanceo de ecuaciones químicas
química
propiedades de los elementos, compuestos, reacciones químicas y leyes de la química.
Quimica
Este quiz evalúa tus conocimientos sobre diversos temas de química, desde conceptos básicos hasta reacciones y compuestos.
LIPIDOS.
RESUMEN
Temario y Formulario de Quimica General
Vienen varios conceptos acerca de Quimica General, un apartado de formulas para usarlo de repaso y aplicarlo en ejercicios. Es un resumen de temas relacionados a Quimica General.
Contenidos más populares
9Jerarquía de operaciones
Te enseña la jerarquía de operaciones y también te ecplica que son y como las puedes hacer
química
química
Sistema óseo
Función, tipos, etcétera
Mapa metabólico
Mapa metabólico, glucólisis, gluconeogénesis, lípidos, vía de las pentosas, ciclo de krebs
Célula animal y vegetal
En resumen, este documento te habla sobre qué es, características, diferencias y similitudes de la célula animal y célula vegetal.💗
Matemáticas
matemáticas
Examen mate
matemáticas
Mapa mental - Sistema Nervioso
Mapa mental sobre el sistema nervioso
Historia ECOEMS (Comipems)
Breve resumen de los temas de historia universal del examen del examen de media superior ECOEMS del valle de México
¿No encuentras lo que buscas? Explora otros temas.
Reseñas de nuestros usuarios. Ellos obtuvieron todo lo bueno — y tú también lo harías.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Guía fácil: Estructura atómica, modelos y enlaces químicos explicados
¿Alguna vez te has preguntado de qué están hechas todas las cosas que te rodean? Todo comienza con los átomos, las piezas fundamentales de la materia que se combinan de maneras increíbles para formar desde el agua que bebes hasta... Mostrar más

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Fundamentos Atómicos: Las Piezas del Rompecabezas
Imagínate que tienes superpoderes para ver las cosas más pequeñas del universo. Lo primero que encontrarías sería el átomo, la partícula más pequeña de cualquier sustancia que no se puede descomponer químicamente.
Cada átomo es como una mini ciudad con un núcleo en el centro (formado por protones con carga positiva y neutrones sin carga) y electrones con carga negativa girando alrededor. Lo genial es que cada elemento tiene un número único de protones, como si fuera su huella digital.
Los científicos Bohr y Sommerfield nos ayudaron a entender que los electrones no andan perdidos por ahí, sino que viven en niveles energéticos específicos alrededor del núcleo. Es como si cada electrón tuviera su propio carril asignado en una pista de carreras circular o elíptica.
Dato curioso: El sodio (Na) tiene 11 protones, así que también tiene 11 electrones cuando está en equilibrio. ¡Es como un sistema perfectamente balanceado!

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Modelos Atómicos en Acción
Los modelos atómicos son como mapas que nos muestran dónde viven los electrones en diferentes elementos. El modelo de Bohr nos dice que los electrones están en niveles específicos, mientras que Sommerfield añadió que pueden moverse en órbitas circulares o elípticas.
Cuando hablamos del electrón, estamos hablando de una partícula súper pequeña con carga negativa que no se puede dividir más. Es uno de los bloques fundamentales de la materia, representado por el símbolo "e⁻".
Para elementos como el hidrógeno (H), que solo tiene un electrón, es fácil visualizar cómo funciona este sistema. Ese electrón único orbita alrededor del núcleo siguiendo las reglas que descubrieron estos científicos.
Tip de estudio: Dibuja los modelos atómicos con colores diferentes para cada nivel energético. Te ayudará a recordar cómo se distribuyen los electrones.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Electrones de Valencia y Formación de Iones
Los electrones de valencia son los electrones VIP del átomo porque viven en el nivel de energía más externo. Estos son los que realmente importan cuando los átomos quieren hacer amigos (formar enlaces químicos).
La capa de valencia es como la "zona de contacto" del átomo. El número de electrones en esta capa determina qué tan sociable será tu átomo y con quién se va a juntar. Es la clave para predecir el comportamiento químico.
Cuando un átomo gana o pierde electrones, se convierte en un ion. Los cationes son iones con carga positiva (perdieron electrones), mientras que los aniones tienen carga negativa (ganaron electrones). Es como si el átomo fuera una persona que puede tener más o menos dinero de lo normal.
Recuerda: Un átomo neutro tiene el mismo número de protones y electrones. ¡Cuando este equilibrio se rompe, nacen los iones!

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Enlaces Químicos: Cuando los Átomos se Unen
Los enlaces químicos son las fuerzas invisibles que mantienen unidos a los átomos, como el pegamento molecular que crea todo lo que existe. Sin estos enlaces, no existirían las moléculas ni los compuestos.
El enlace iónico se forma cuando un átomo cede electrones y otro los recibe, creando iones con cargas opuestas que se atraen. Es como el romance entre el sodio (Na⁺) y el cloro (Cl⁻) que forma la sal de mesa (NaCl).
En este tipo de enlace, el metal (como el sodio) pierde electrones y se vuelve catión, mientras que el no metal (como el cloro) gana esos electrones y se convierte en anión. La atracción electrostática entre cargas opuestas los mantiene unidos.
Visualízalo: Imagina que el sodio le regala un electrón al cloro. Ahora el sodio queda positivo y el cloro negativo, ¡y se atraen como imanes opuestos!

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Enlaces Covalentes: Compartir es Vivir
El enlace covalente funciona diferente: aquí los átomos comparten electrones en lugar de regalarlos. Es como dos amigos que comparten sus juguetes para que ambos puedan jugar.
En el enlace covalente no polar, los átomos comparten los electrones de manera equitativa. Esto pasa cuando se unen átomos iguales (como H₂) o con electronegatividades muy similares.
El átomo de hidrógeno es el más simple: un protón en el núcleo y un electrón girando alrededor. Cuando dos átomos de hidrógeno se juntan, comparten sus electrones formando H₂, donde cada átomo siente que tiene dos electrones.
Dato interesante: En la molécula H₂, cada átomo de hidrógeno contribuye con un electrón, y ambos comparten ese par equitativamente.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Enlaces Covalentes Polares y el Agua
Los enlaces covalentes polares se forman cuando los átomos no comparten los electrones de manera equitativa. Uno de los átomos "jala" más fuerte a los electrones, creando polos positivo y negativo.
El agua (H₂O) es el ejemplo perfecto de esto. El oxígeno es más "comelón" de electrones que el hidrógeno, así que atrae más hacia él los electrones compartidos. Esto hace que el oxígeno quede ligeramente negativo y los hidrógenos ligeramente positivos.
Este tipo de enlace explica por qué el agua tiene propiedades tan especiales. Los enlaces de hidrógeno se forman cuando el hidrógeno de una molécula se siente atraído hacia átomos electronegativos de otras moléculas.
Aplicación real: Las propiedades únicas del agua (como su punto de ebullición alto) se deben a estos enlaces polares y de hidrógeno.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Enlaces Especiales: Coordinado y Metálico
El enlace covalente coordinado es como un acto de generosidad extrema: un átomo aporta ambos electrones del par compartido, mientras el otro solo ofrece el espacio. Es menos común pero súper importante en ciertos compuestos.
El enlace metálico es exclusivo de los metales y funciona como una "sopa de electrones". Los átomos metálicos liberan sus electrones de valencia, creando un "mar de electrones" que se mueve libremente entre los cationes metálicos.
Este tipo de enlace explica por qué los metales brillan, conducen electricidad y calor, y son maleables. Los electrones libres pueden moverse fácilmente, transmitiendo energía y permitiendo que el metal se deforme sin romperse.
Conexión real: Cuando tocas algo metálico frío, los electrones libres transmiten rápidamente el calor de tu mano, por eso se siente más frío que otros materiales.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Herramientas para Entender los Enlaces
Las estructuras de Lewis son como diagramas que muestran cómo se distribuyen los electrones en las moléculas. Usas puntos para electrones solitarios y líneas para enlaces, creando un mapa visual de la molécula.
La regla del octeto dice que los átomos son más felices cuando tienen 8 electrones en su capa de valencia. Es como si cada átomo quisiera tener su "octet completo" para sentirse estable y seguro.
La electronegatividad mide qué tan "comelón" es un átomo de electrones. Los elementos más electronegativos (como el flúor) atraen fuertemente los electrones, mientras que otros (como el cesio) los ceden fácilmente.
Tip de examen: La electronegatividad aumenta hacia la derecha y hacia arriba en la tabla periódica. ¡El flúor es el más electrónegativo de todos!

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Propiedades Periódicas Clave
La afinidad electrónica es la energía que se libera cuando un átomo neutral atrapa un electrón extra. Es como medir qué tan "feliz" se pone un átomo al recibir un electrón adicional.
El radio iónico nos dice qué tan grande es un ion comparado con su átomo original. Los cationes son más pequeños (perdieron electrones) y los aniones son más grandes (ganaron electrones).
El radio atómico es simplemente el tamaño del átomo. Esta propiedad sigue patrones predecibles en la tabla periódica: aumenta hacia abajo y hacia la izquierda.
El número de oxidación indica cuántos electrones puede ganar, perder o compartir un átomo. Es como su "capacidad de negociación" en las reacciones químicas.
Regla práctica: Para encontrar números de oxidación, recuerda que la suma de todos los números de oxidación en un compuesto neutro debe ser cero.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Valencia: La Capacidad de Combinación
La valencia es el número de electrones que un elemento necesita ganar, perder o compartir para completar su capa de valencia. Es como conocer cuántos "asientos vacíos" tiene disponibles para hacer enlaces.
Por ejemplo, el aluminio (Al³⁺) tiene valencia +3 porque puede ceder 3 electrones. Esto significa que tiene 13 protones pero solo 10 electrones, dándole esa carga positiva característica.
Entender la valencia te ayuda a predecir qué tipos de compuestos puede formar cada elemento y en qué proporciones. Es una herramienta súper útil para balancear ecuaciones químicas y entender fórmulas.
Consejo final: Memoriza las valencias más comunes de los elementos que estudias frecuentemente. Te ahorrará mucho tiempo en los exámenes y problemas.
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
Contenidos más populares de Química
9química
química
Mapa metabólico
Mapa metabólico, glucólisis, gluconeogénesis, lípidos, vía de las pentosas, ciclo de krebs
Examen ecoems unam
Estudiar para el examen de ecoems 2026 unam
Quimica ECOEMS(Comipems)
resumen de los temas de quimica que se presentarán en el próximo examen de nivel media superior en la zona metropolitana de el valle de México
Método de Tanteo
Balanceo de ecuaciones químicas
química
propiedades de los elementos, compuestos, reacciones químicas y leyes de la química.
Quimica
Este quiz evalúa tus conocimientos sobre diversos temas de química, desde conceptos básicos hasta reacciones y compuestos.
LIPIDOS.
RESUMEN
Temario y Formulario de Quimica General
Vienen varios conceptos acerca de Quimica General, un apartado de formulas para usarlo de repaso y aplicarlo en ejercicios. Es un resumen de temas relacionados a Quimica General.
Contenidos más populares
9Jerarquía de operaciones
Te enseña la jerarquía de operaciones y también te ecplica que son y como las puedes hacer
química
química
Sistema óseo
Función, tipos, etcétera
Mapa metabólico
Mapa metabólico, glucólisis, gluconeogénesis, lípidos, vía de las pentosas, ciclo de krebs
Célula animal y vegetal
En resumen, este documento te habla sobre qué es, características, diferencias y similitudes de la célula animal y célula vegetal.💗
Matemáticas
matemáticas
Examen mate
matemáticas
Mapa mental - Sistema Nervioso
Mapa mental sobre el sistema nervioso
Historia ECOEMS (Comipems)
Breve resumen de los temas de historia universal del examen del examen de media superior ECOEMS del valle de México
¿No encuentras lo que buscas? Explora otros temas.
Reseñas de nuestros usuarios. Ellos obtuvieron todo lo bueno — y tú también lo harías.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.