La estructura atómica es la base de toda la química... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Knowunity AI
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
192
•
Actualizado Mar 23, 2026
•
Mauricio sinoe Pérez Carbajal
@mauriciosinoepr
La estructura atómica es la base de toda la química... Mostrar más







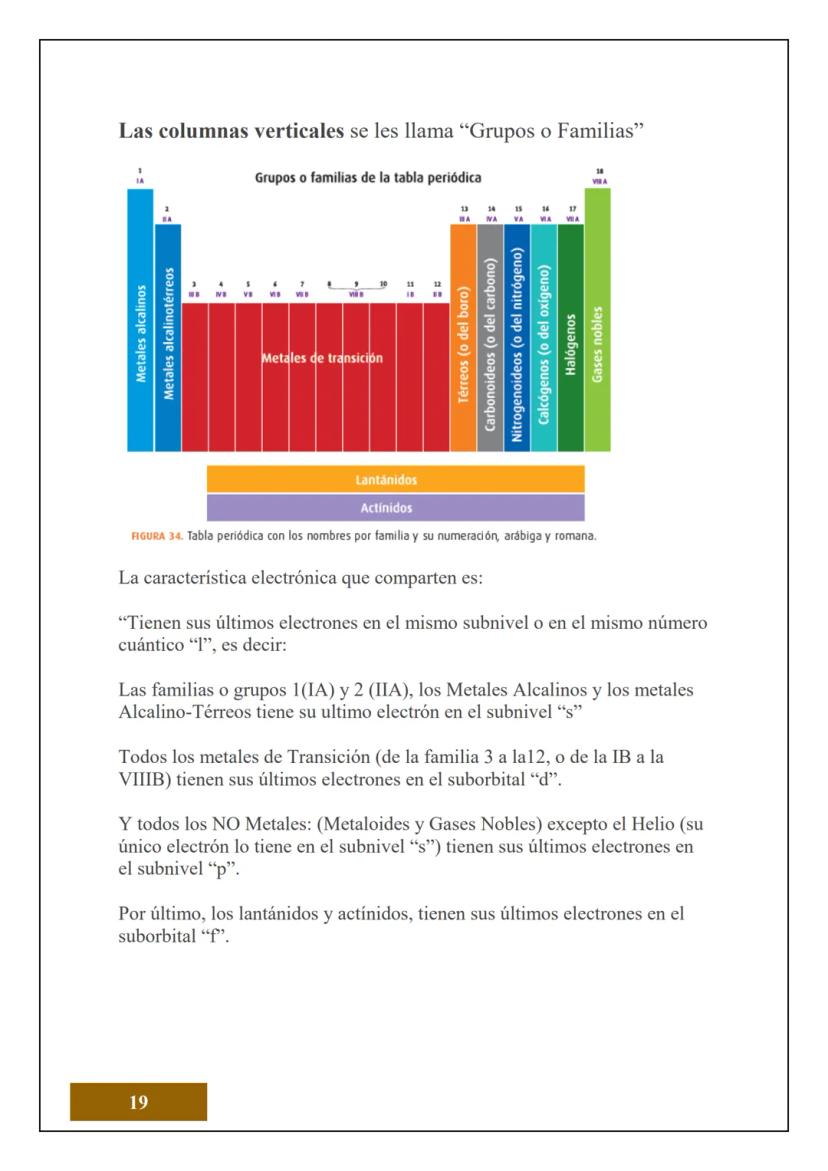
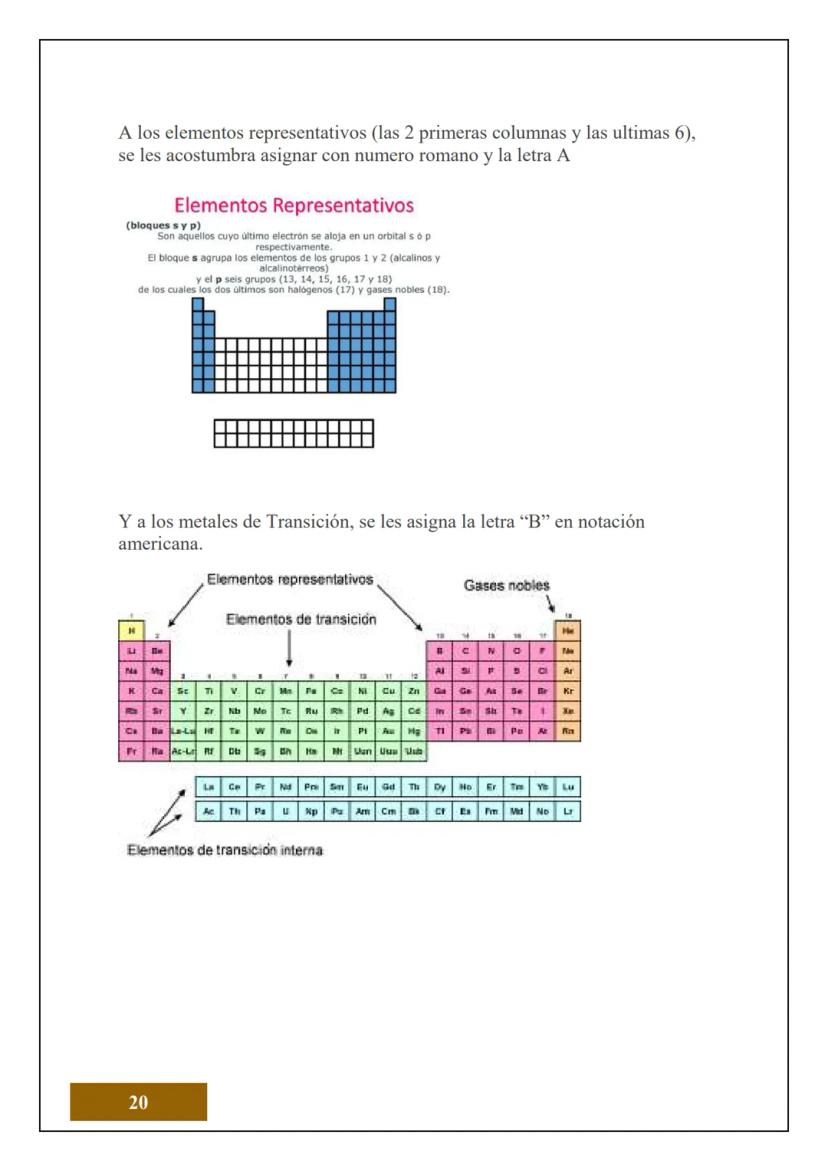






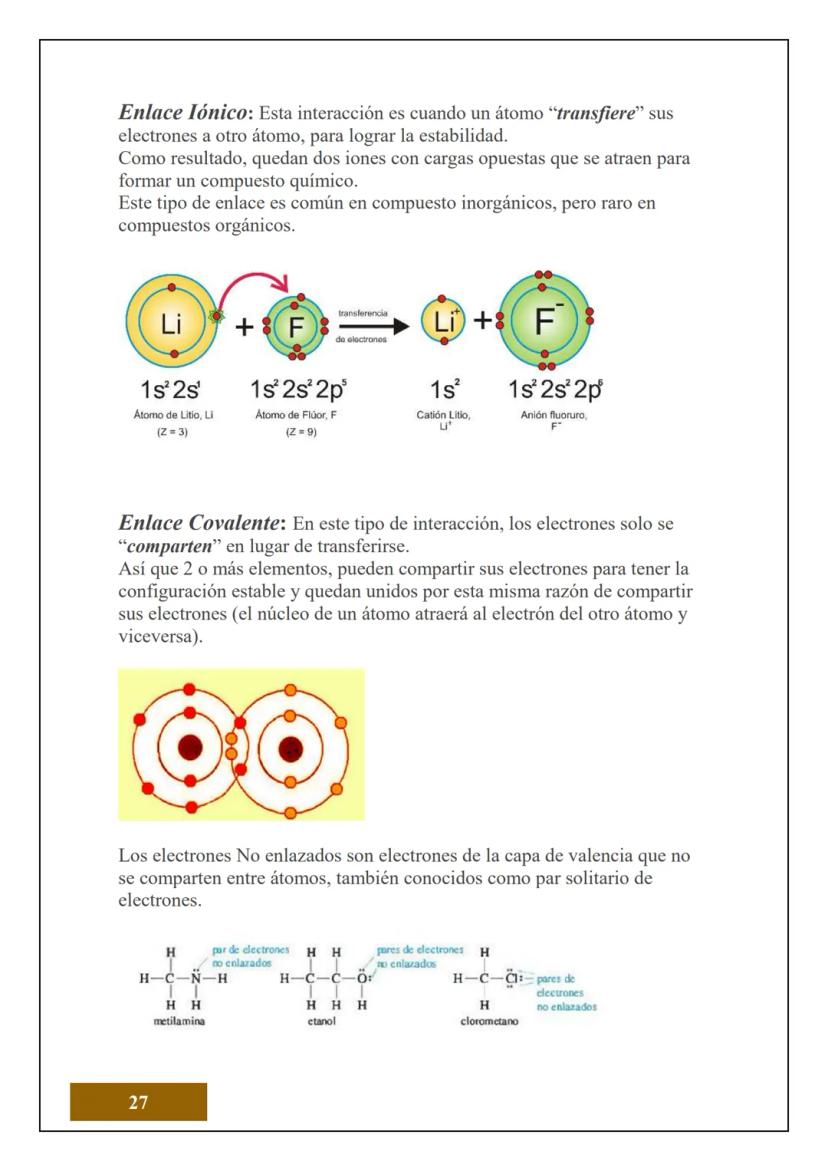


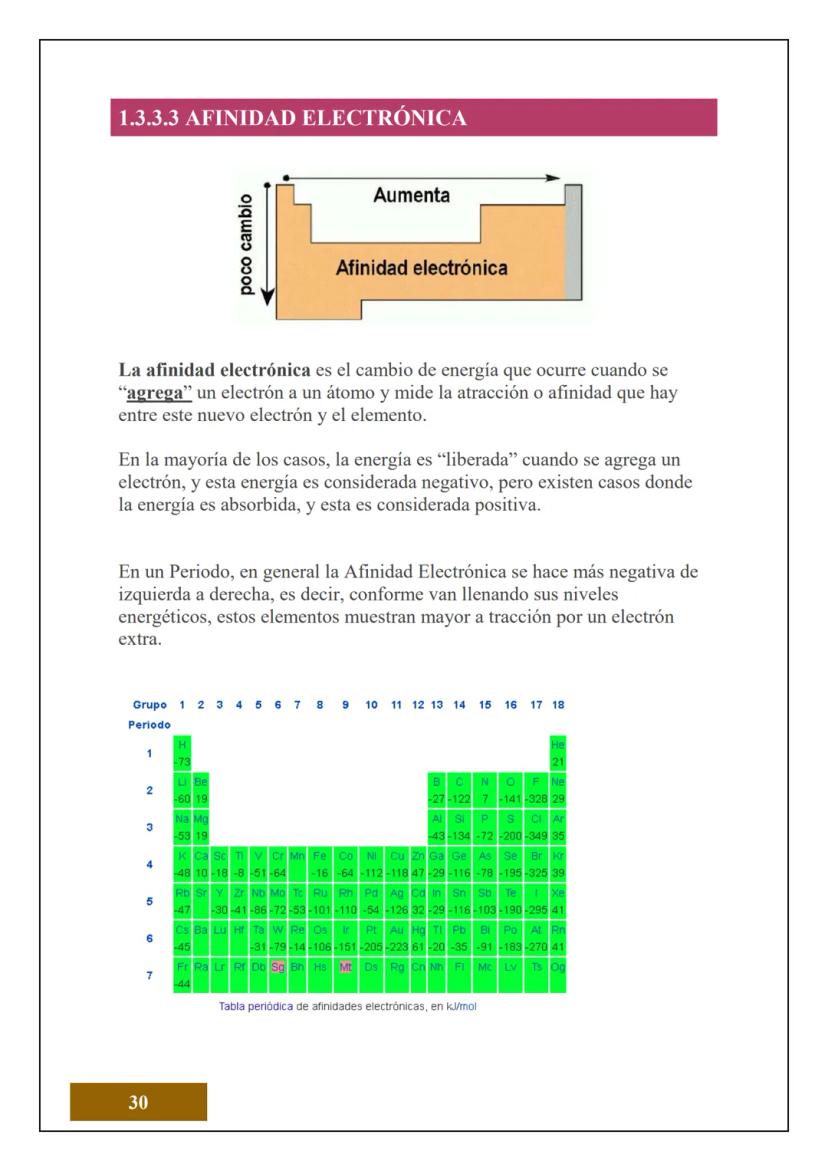








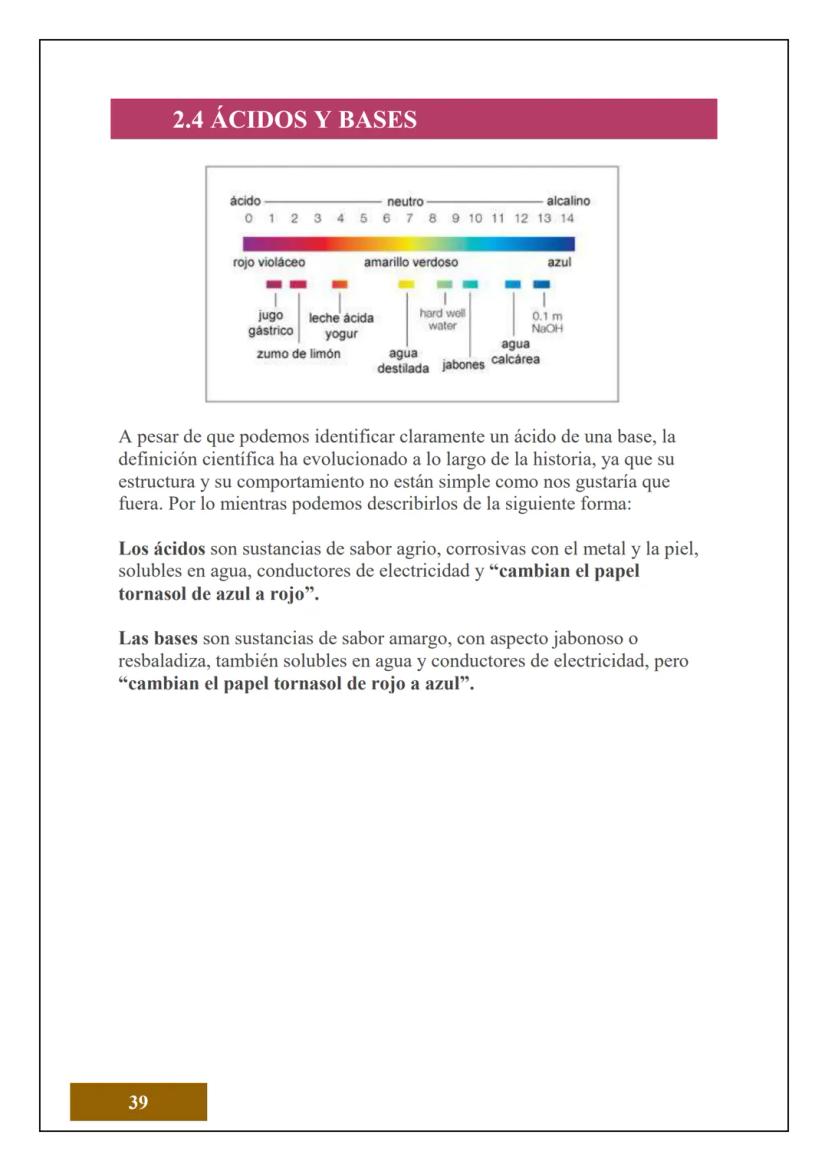


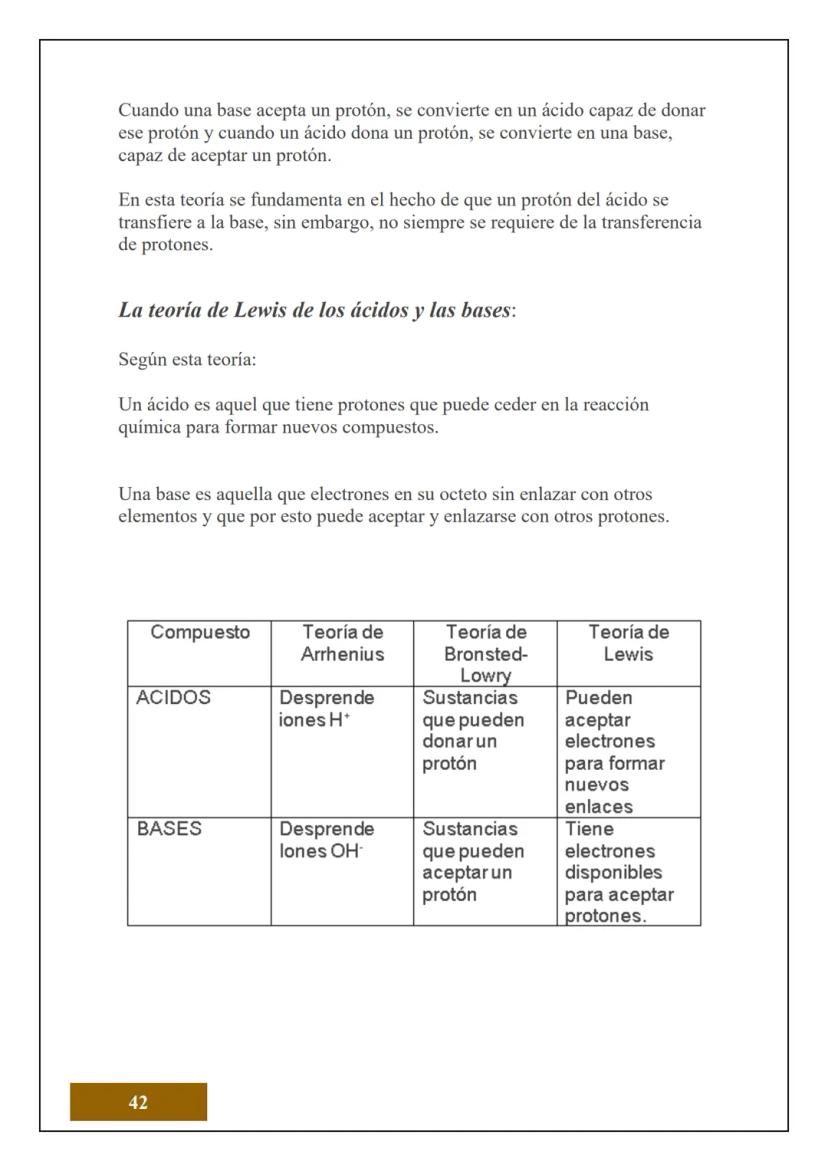





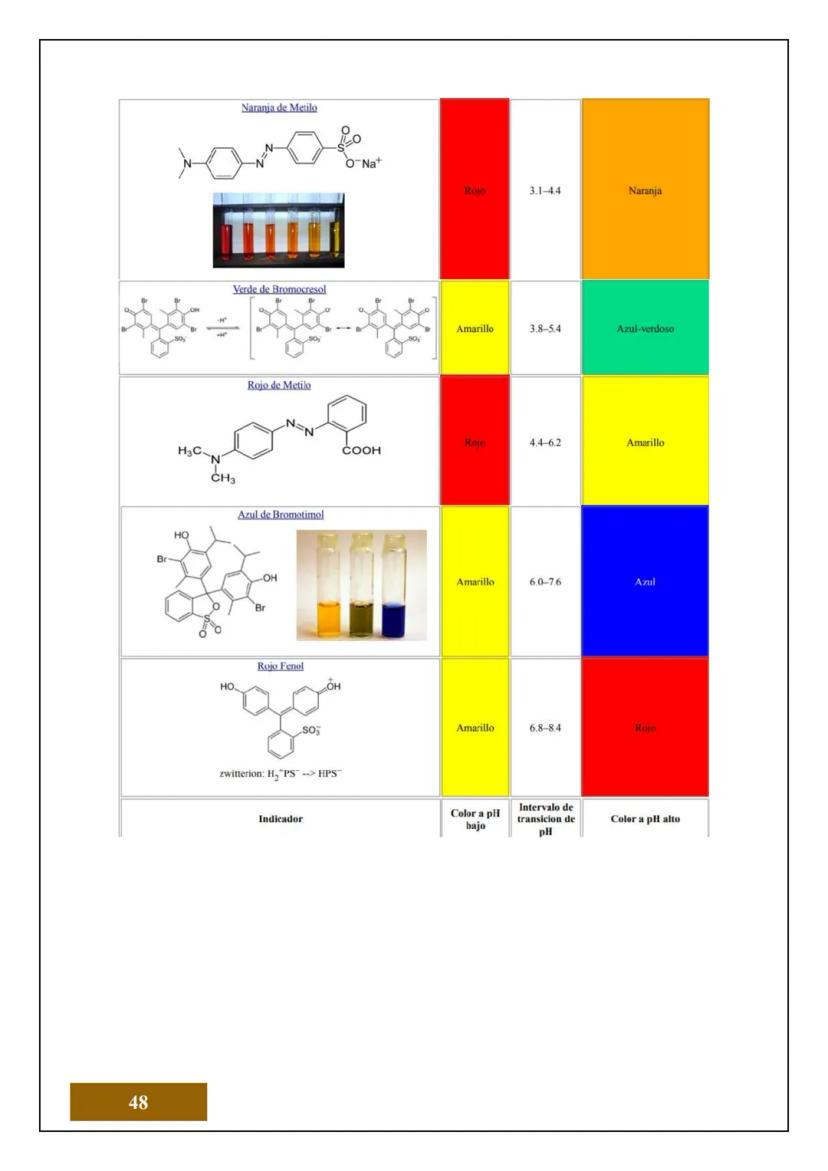
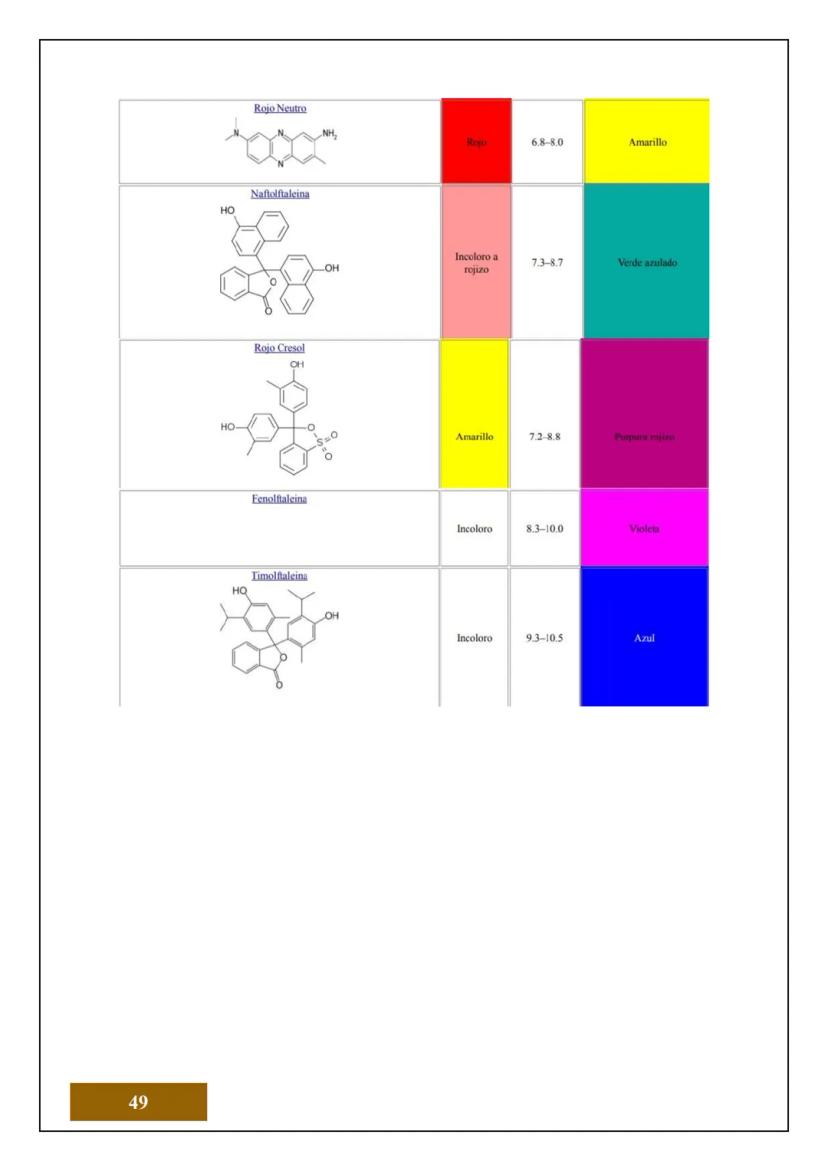



























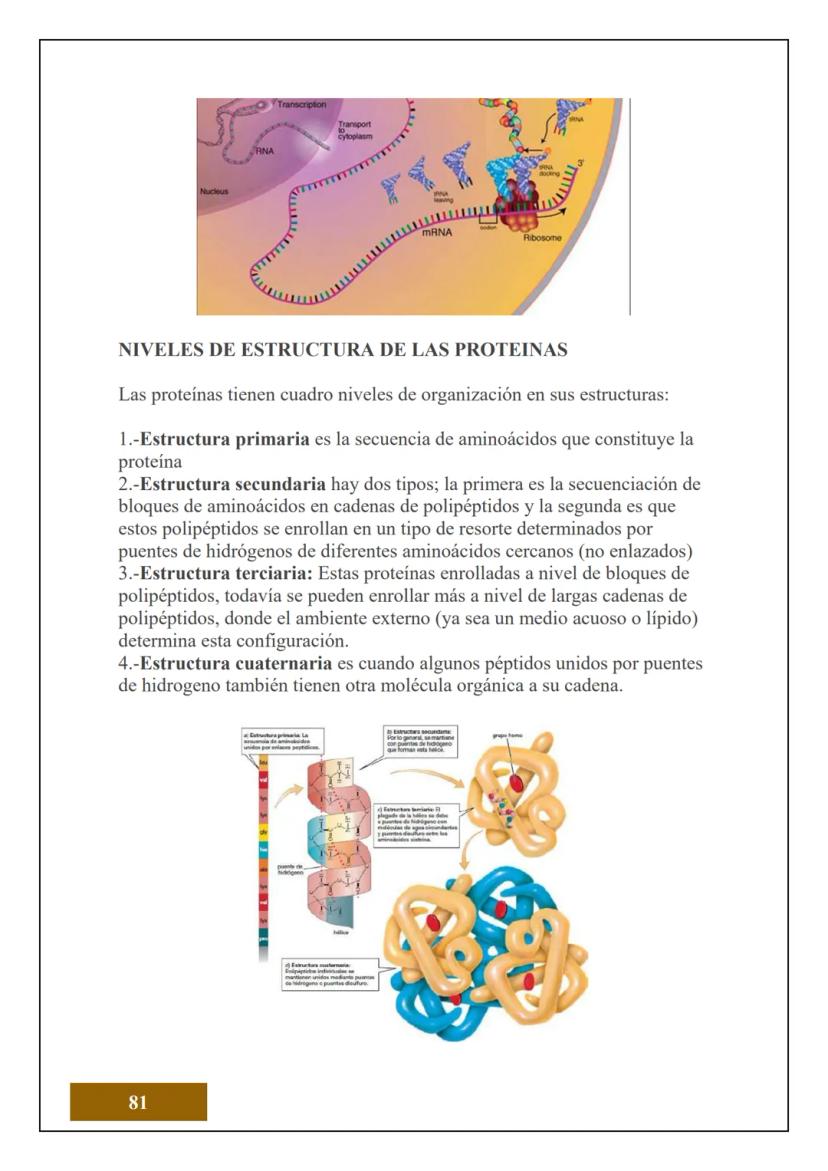
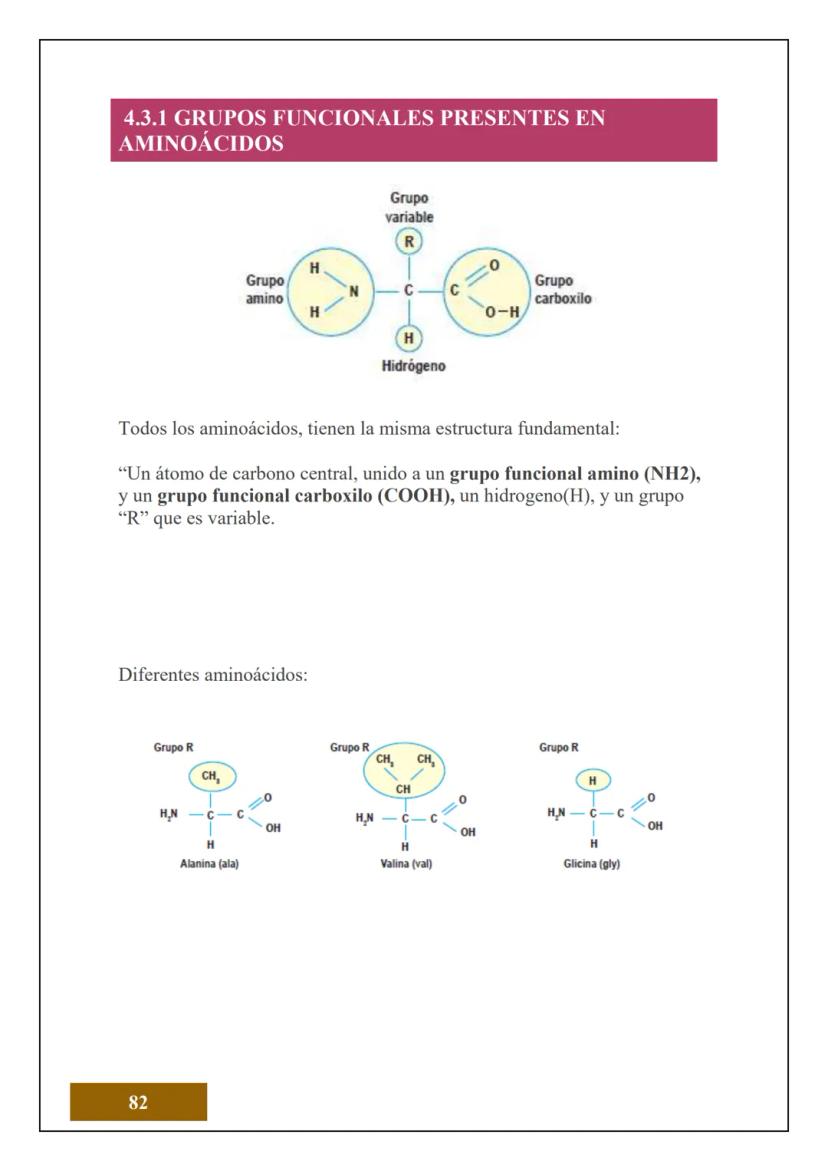
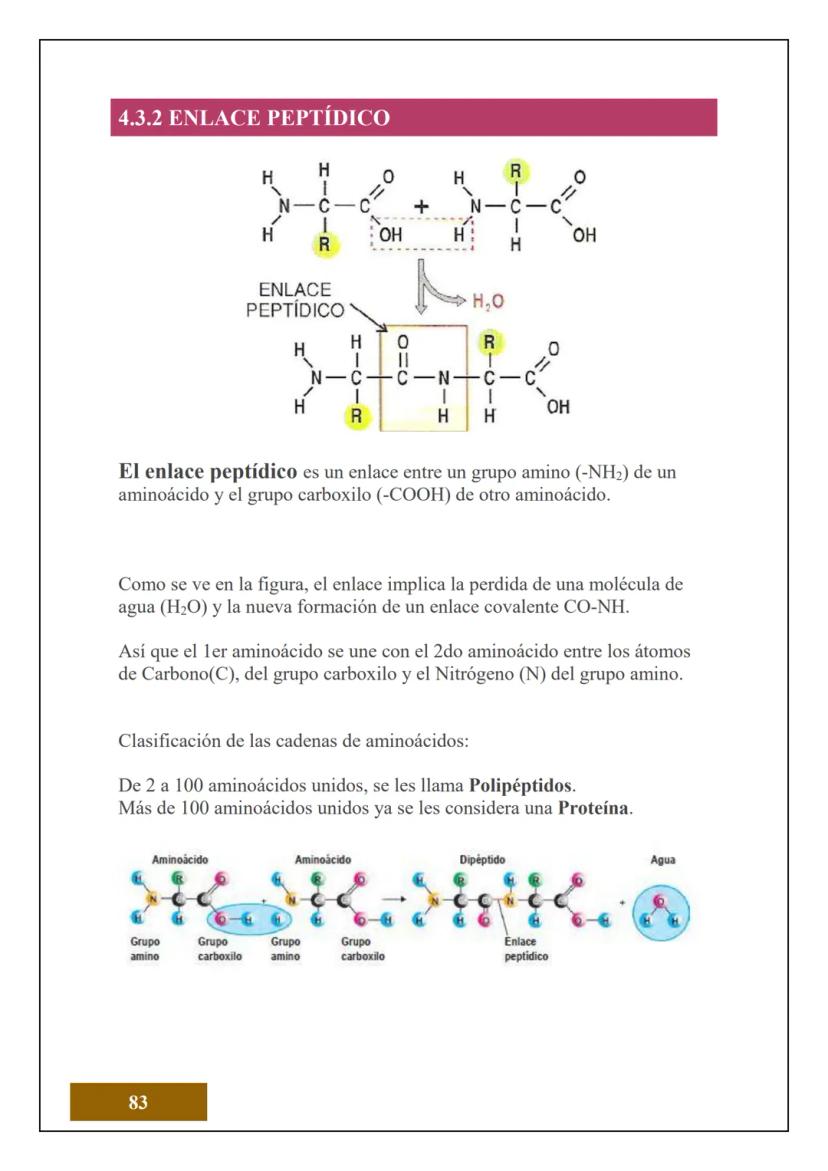







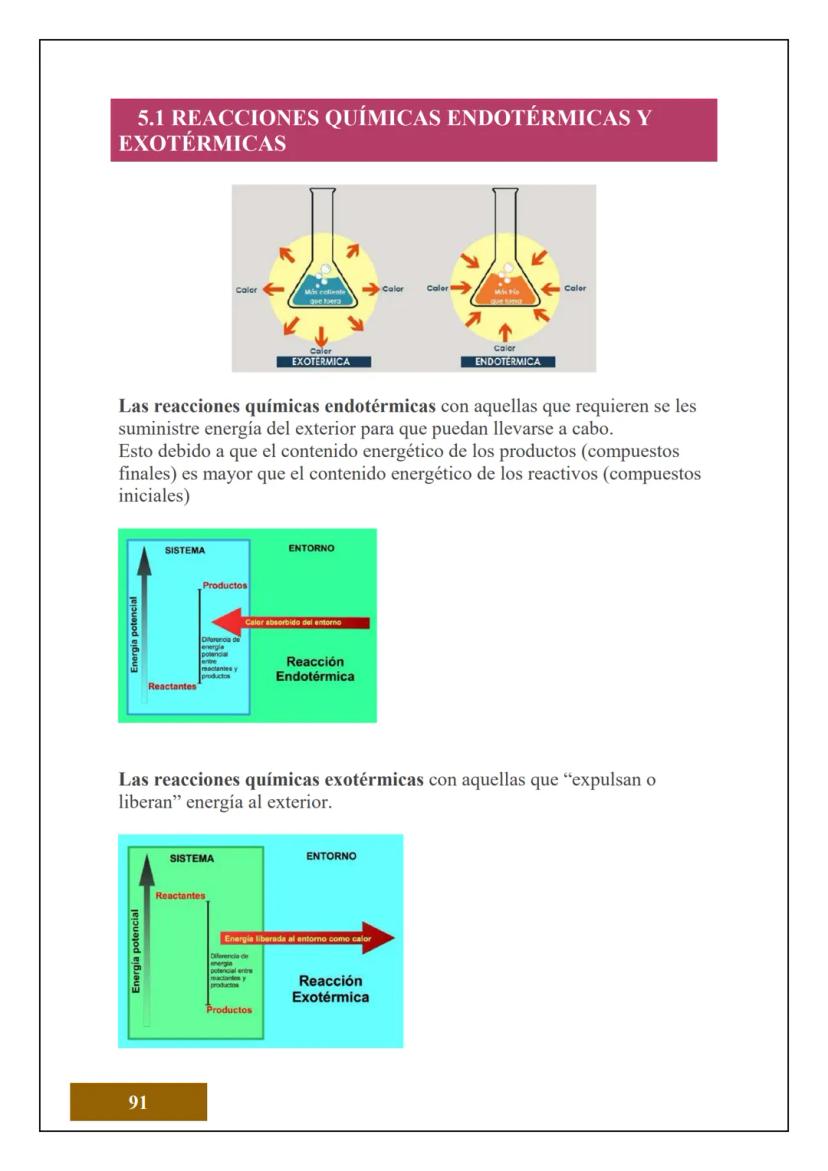









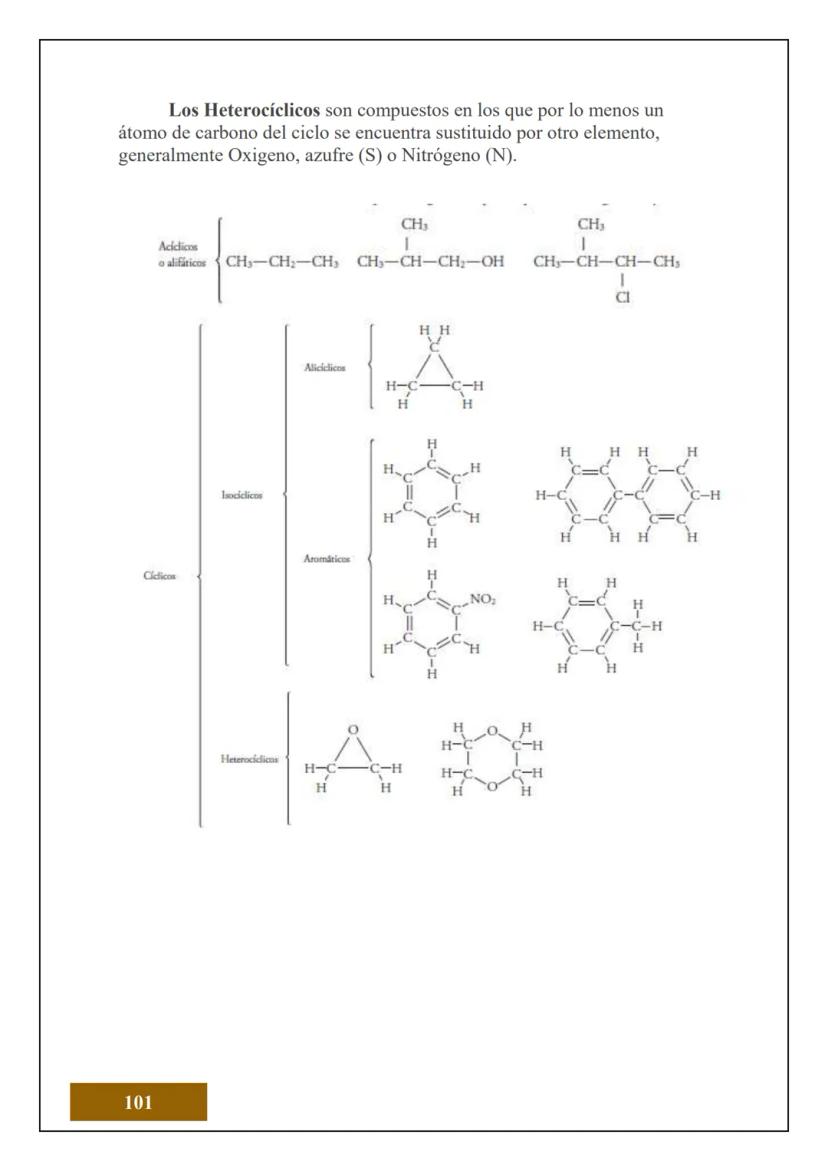

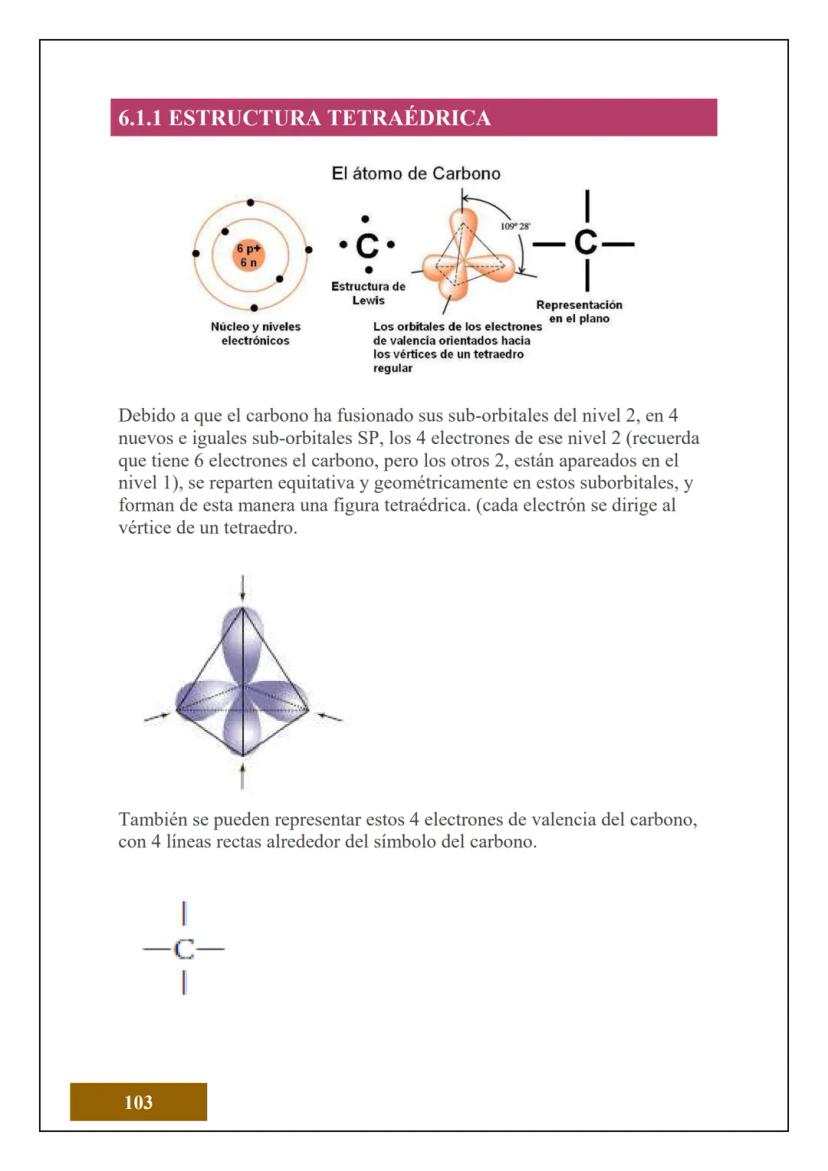



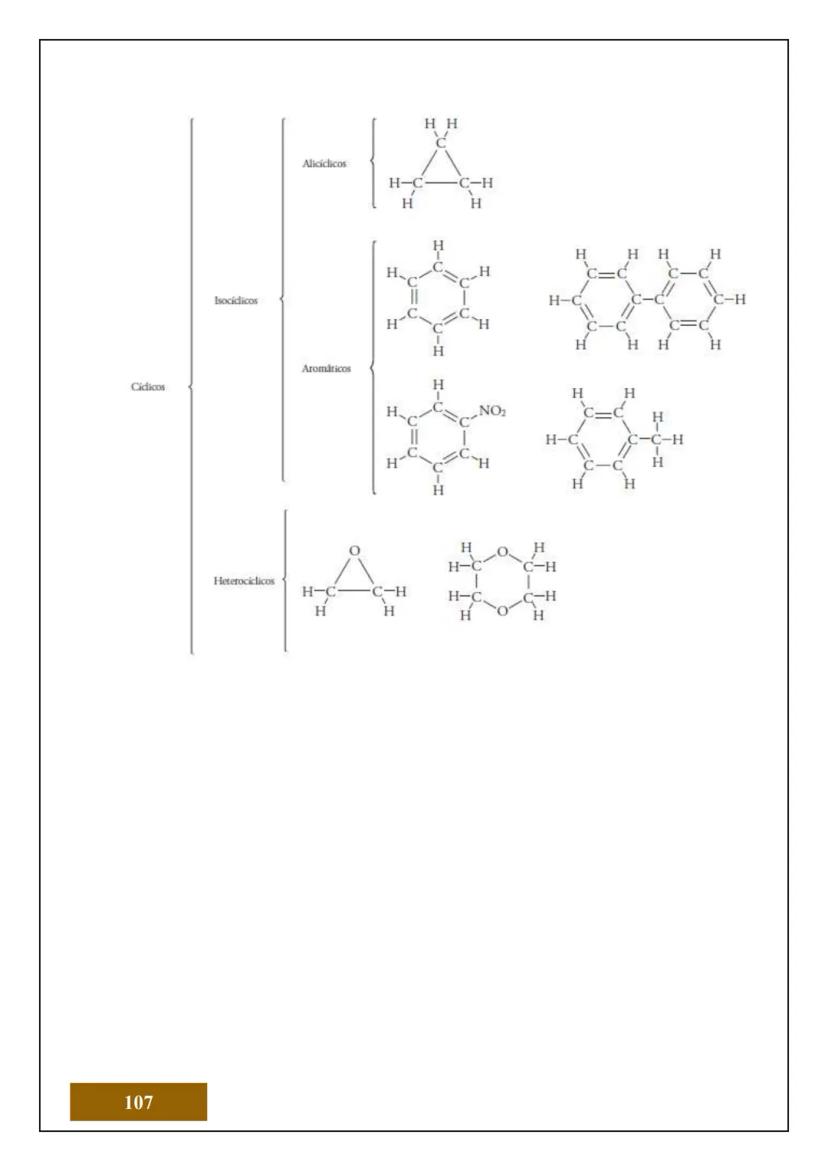

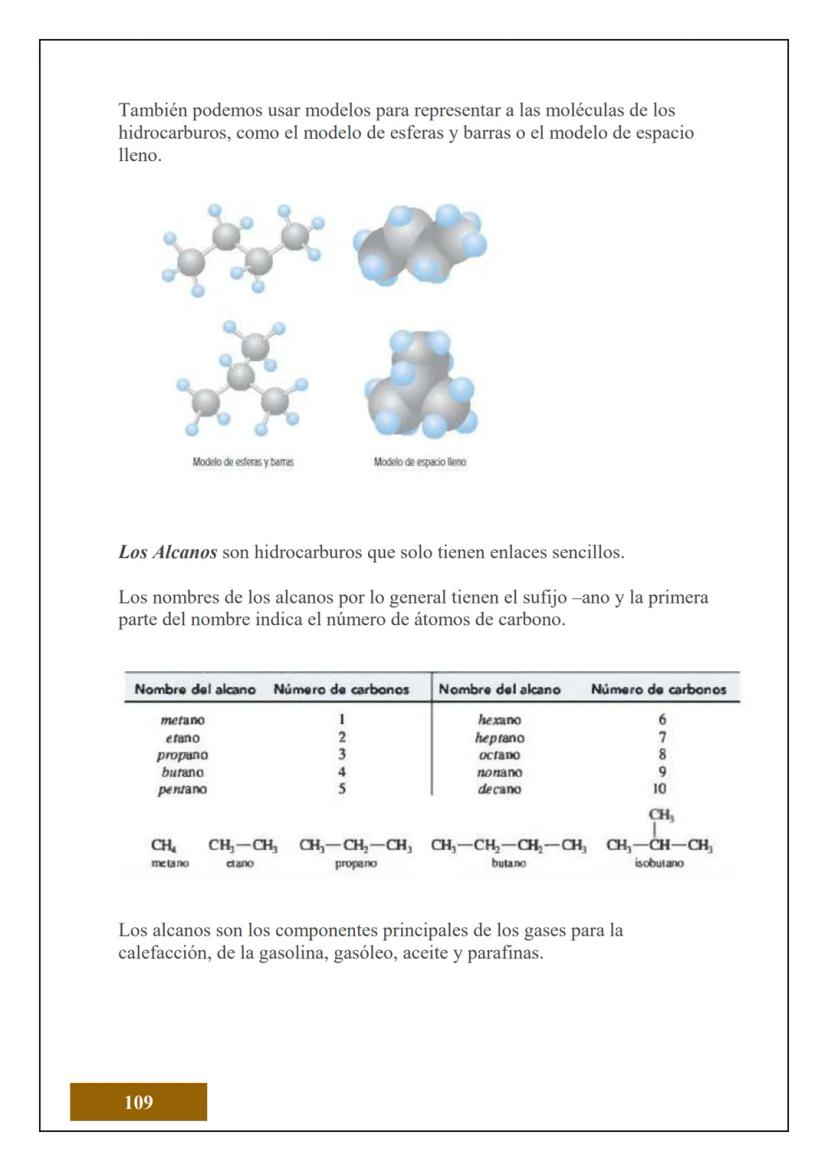
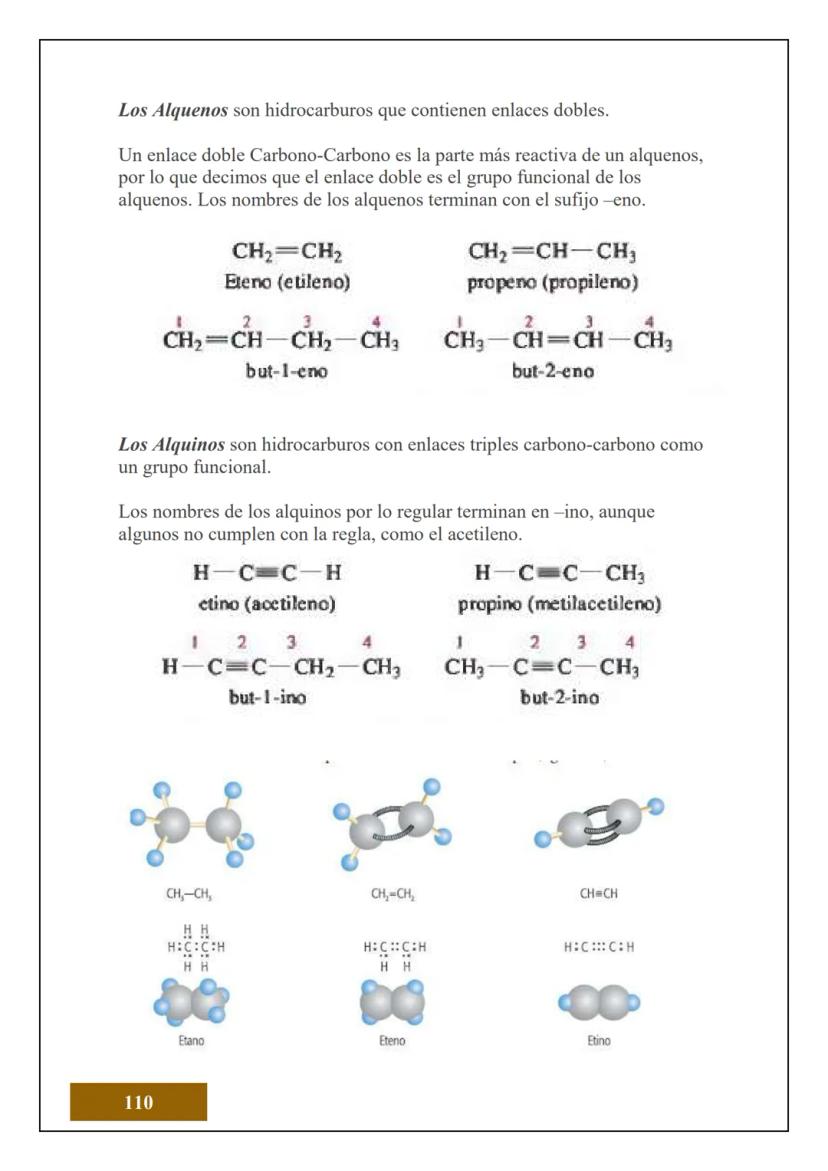
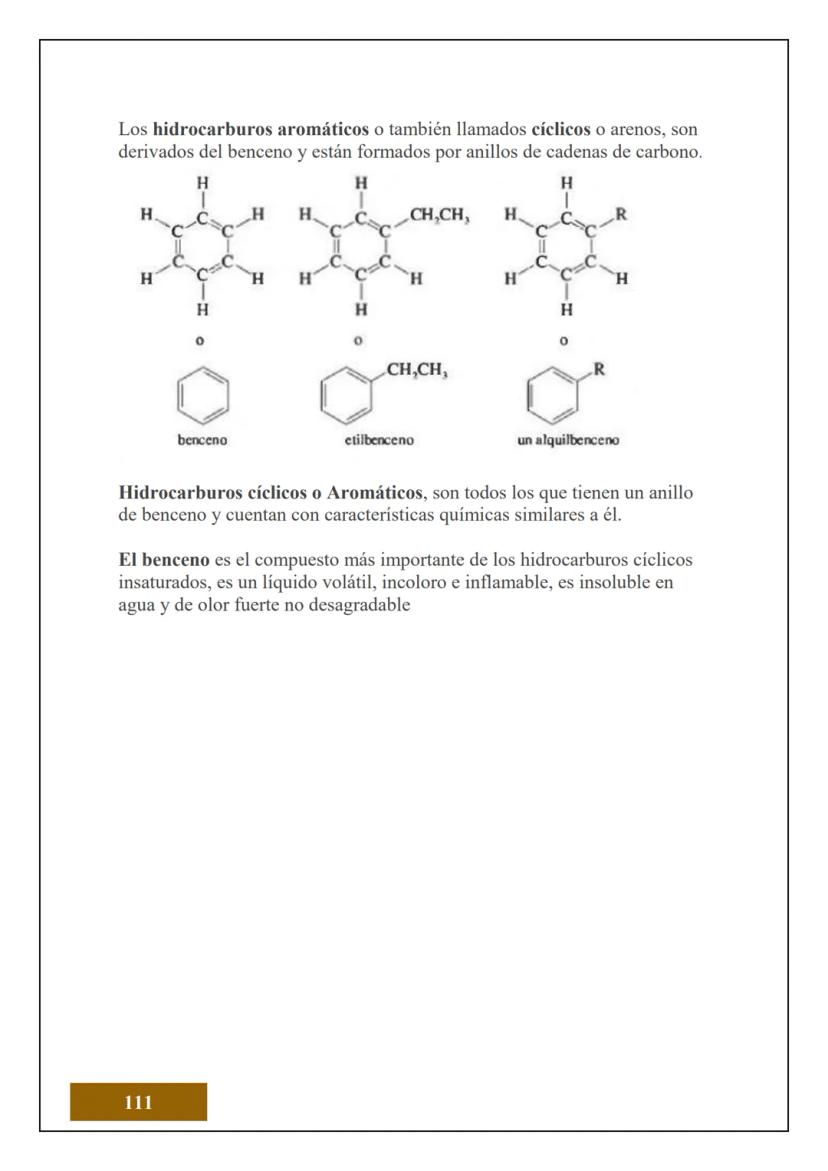
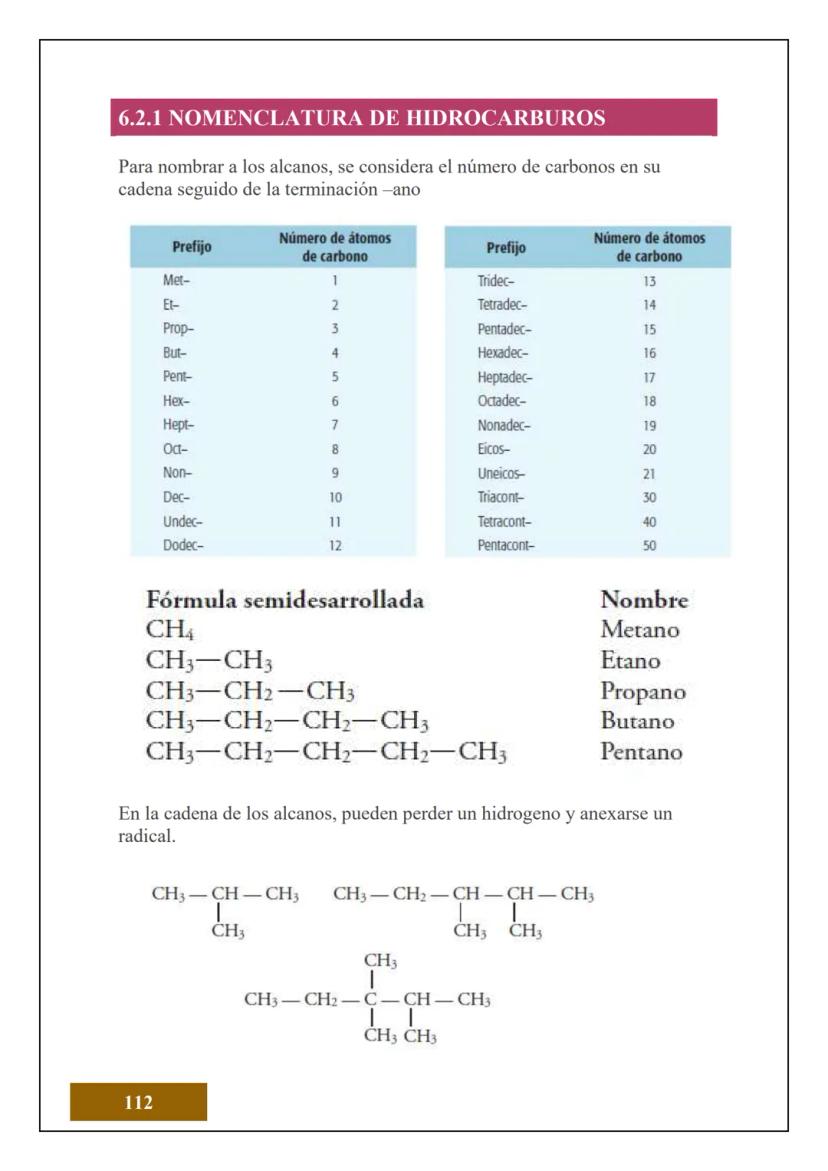

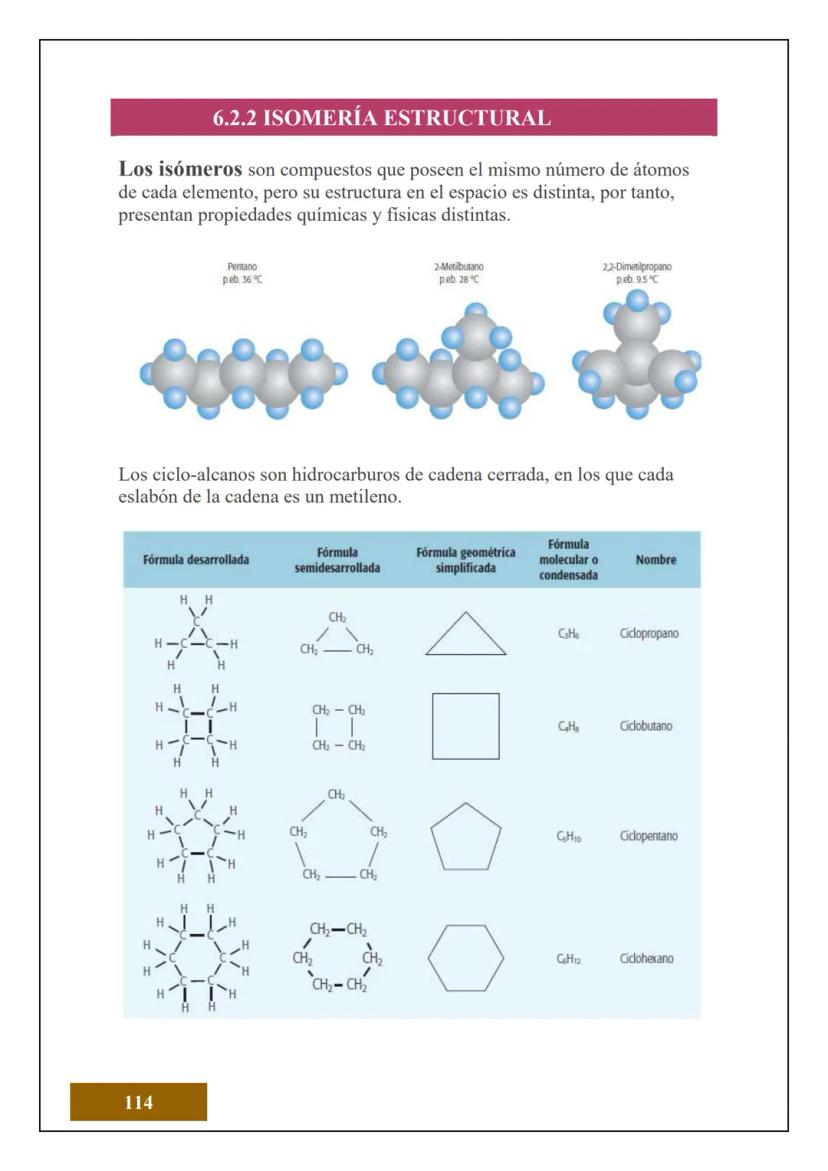
























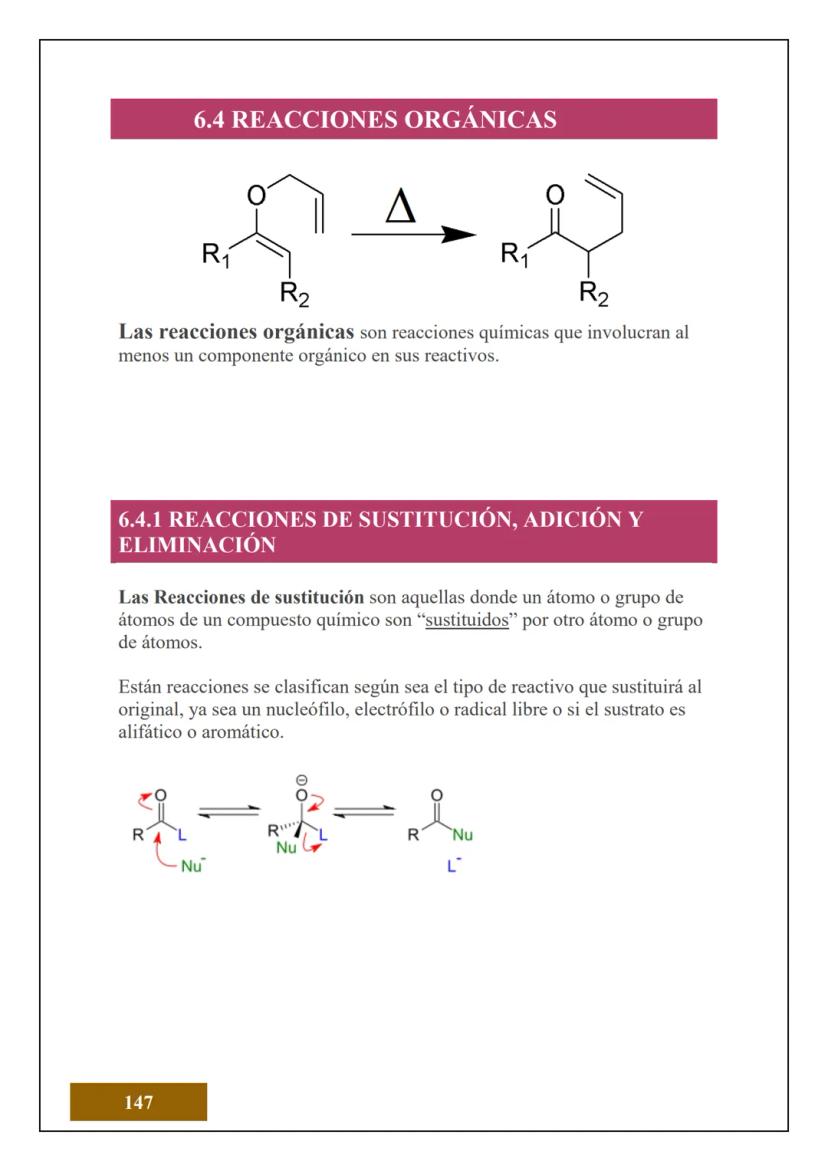



¿Sabías que todo lo que tocas está hecho de átomos? El átomo es la unidad más pequeña de la materia que conserva las propiedades de un elemento químico. Es como el "ladrillo" fundamental de todo lo que existe.
Cada átomo tiene una estructura súper organizada: en el centro está el núcleo (cargado positivamente) que contiene protones y neutrones (sin carga). Alrededor del núcleo giran los electrones , como planetas alrededor del sol.
Los protones pesan aproximadamente 1800 veces más que los electrones, por eso cuando hablamos del peso de un átomo, básicamente solo contamos protones y neutrones. Los electrones son súper livianos pero súper importantes: son los que participan en todas las reacciones químicas que estudiarás.
¡Dato curioso! Si un átomo fuera del tamaño de un estadio de fútbol, el núcleo sería como una canica en el centro.

El número atómico es súper fácil de entender: es simplemente cuántos protones tiene un elemento en su núcleo. Este número nunca cambia para un elemento específico (el carbono siempre tiene 6 protones).
La masa atómica es la suma de protones + neutrones en el núcleo. Como los electrones pesan casi nada comparado con estas partículas, no los contamos para la masa.
Los isótopos son una cosa genial: son átomos del mismo elemento (mismo número de protones) pero con diferente cantidad de neutrones. Por ejemplo, todos los carbonos tienen 6 protones, pero pueden tener 5, 6 o 7 neutrones.
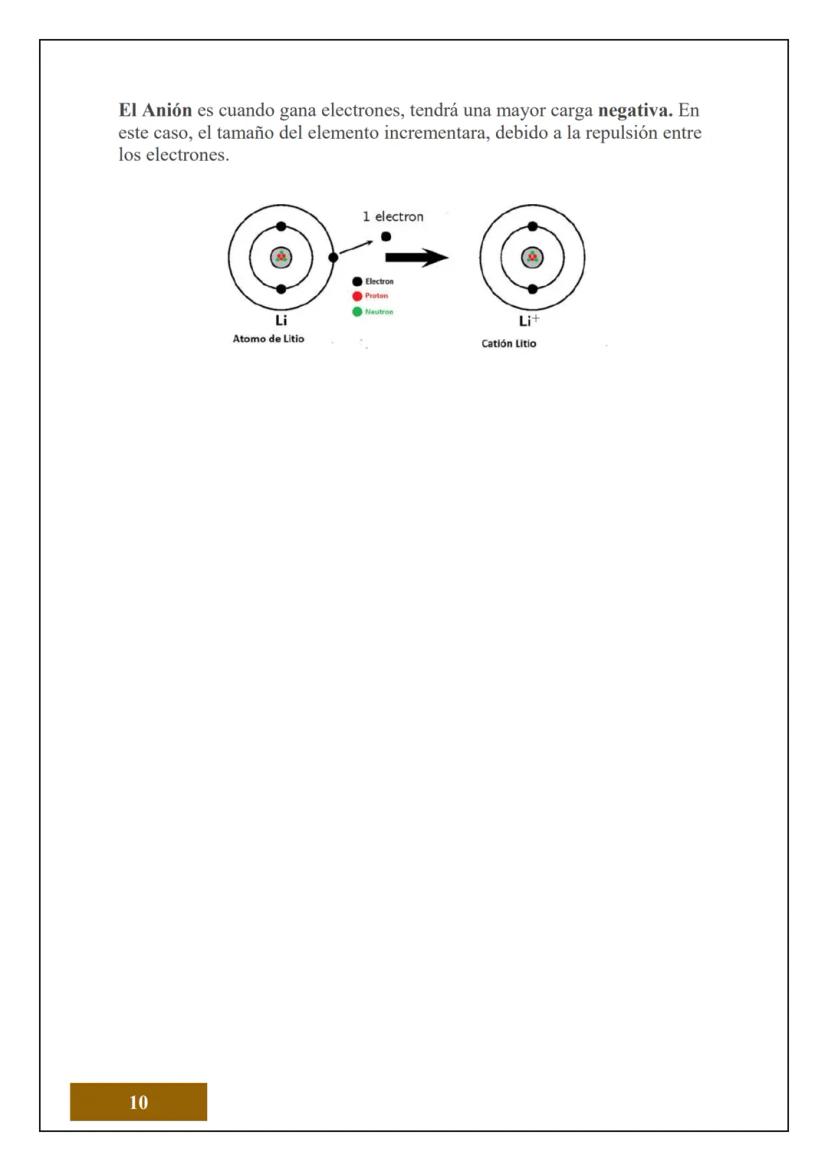
Un ion es cuando un átomo gana o pierde electrones. Si pierde electrones se vuelve catión (+) y se hace más pequeño. Si gana electrones se vuelve anión (-) y se agranda debido a la repulsión entre los electrones extra.
Para el examen: Recuerda que el número atómico = protones, y la masa atómica = protones + neutrones.
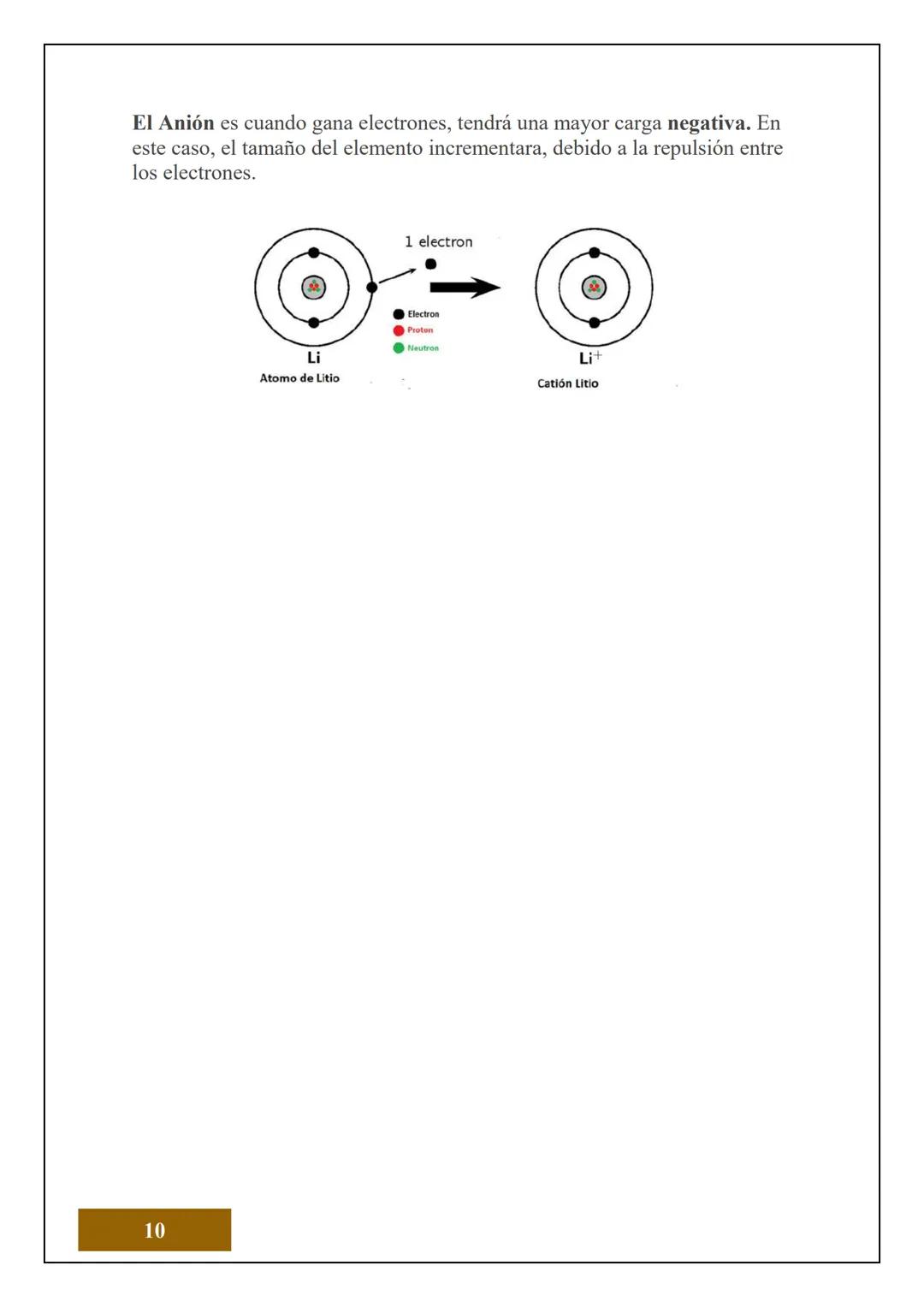
Cuando un átomo se convierte en anión (gana electrones), su tamaño aumenta. Esto pasa porque los electrones extra se repelen entre sí, "empujándose" y haciendo que el átomo se expanda.
Este concepto es clave para entender por qué algunos elementos forman ciertos tipos de enlaces químicos. Los aniones más grandes tienden a comportarse diferente que los cationes más pequeños.

Olvídate de la imagen clásica de electrones girando en círculos perfectos como planetas. Los orbitales atómicos son zonas del espacio donde hay alta probabilidad de encontrar un electrón, no rutas definidas.
La diferencia es crucial: las órbitas de Bohr eran círculos definidos, pero los orbitales son "nubes de probabilidad". Esto resuelve problemas que el modelo antiguo no podía explicar, como el principio de Heisenberg (no puedes saber exactamente dónde está un electrón y cuánta energía tiene al mismo tiempo).
Los orbitales se definen matemáticamente por la ecuación de Schrödinger. No necesitas resolver esta ecuación (¡es súper complicada!), pero sí entender que de ella salen los números cuánticos que describen exactamente dónde pueden estar los electrones.
Concepto clave: Los orbitales no son rutas, son zonas de probabilidad donde "probablemente" está el electrón.

Los números cuánticos son como la "dirección" de cada electrón en el átomo. Son cuatro números que te dicen exactamente dónde vive cada electrón.
n (número cuántico principal): Te dice qué tan lejos está del núcleo . A mayor n, mayor energía y más electrones caben.
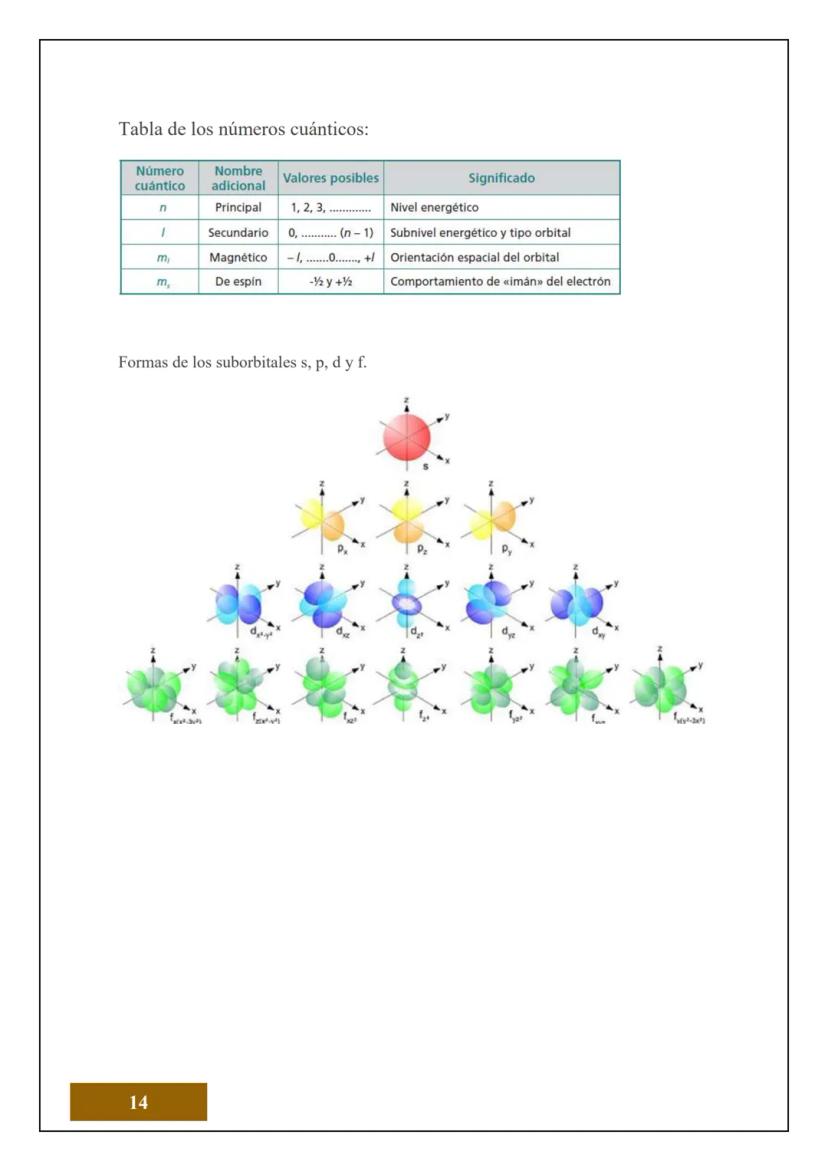
l (número cuántico secundario): Define la forma del orbital. l=0 es "s" (esférica), l=1 es "p" (forma de mancuerna), l=2 es "d", l=3 es "f". Puede valer desde 0 hasta n-1.
m (número cuántico magnético): Te dice la orientación espacial del orbital. Puede valer desde -l hasta +l. Por ejemplo, si l=2, entonces m puede ser -2, -1, 0, +1, +2.
s (spin): Es como si el electrón fuera una peonza que gira. Solo puede valer +1/2 o -1/2 (hacia arriba o hacia abajo).
Tip para memorizar: n=distancia, l=forma, m=orientación, s=giro del electrón.

El número cuántico magnético (m) determina cuántas orientaciones diferentes puede tener un orbital. Por ejemplo, el subnivel "p" tiene tres orientaciones: px, py, pz, correspondientes a m=-1, 0, +1.
El spin del electrón es fascinante: como el electrón tiene carga eléctrica y "gira", se comporta como un imán microscópico. Puede girar en dos direcciones (como las manecillas del reloj o al revés), lo que representa con +1/2 y -1/2.
Esta propiedad magnética del electrón explica por qué algunos materiales son magnéticos y otros no. Cuando los spines están desapareados, el material puede ser magnético.
Dato interesante: El spin electrónico es la base de tecnologías como la resonancia magnética y los discos duros de las computadoras.
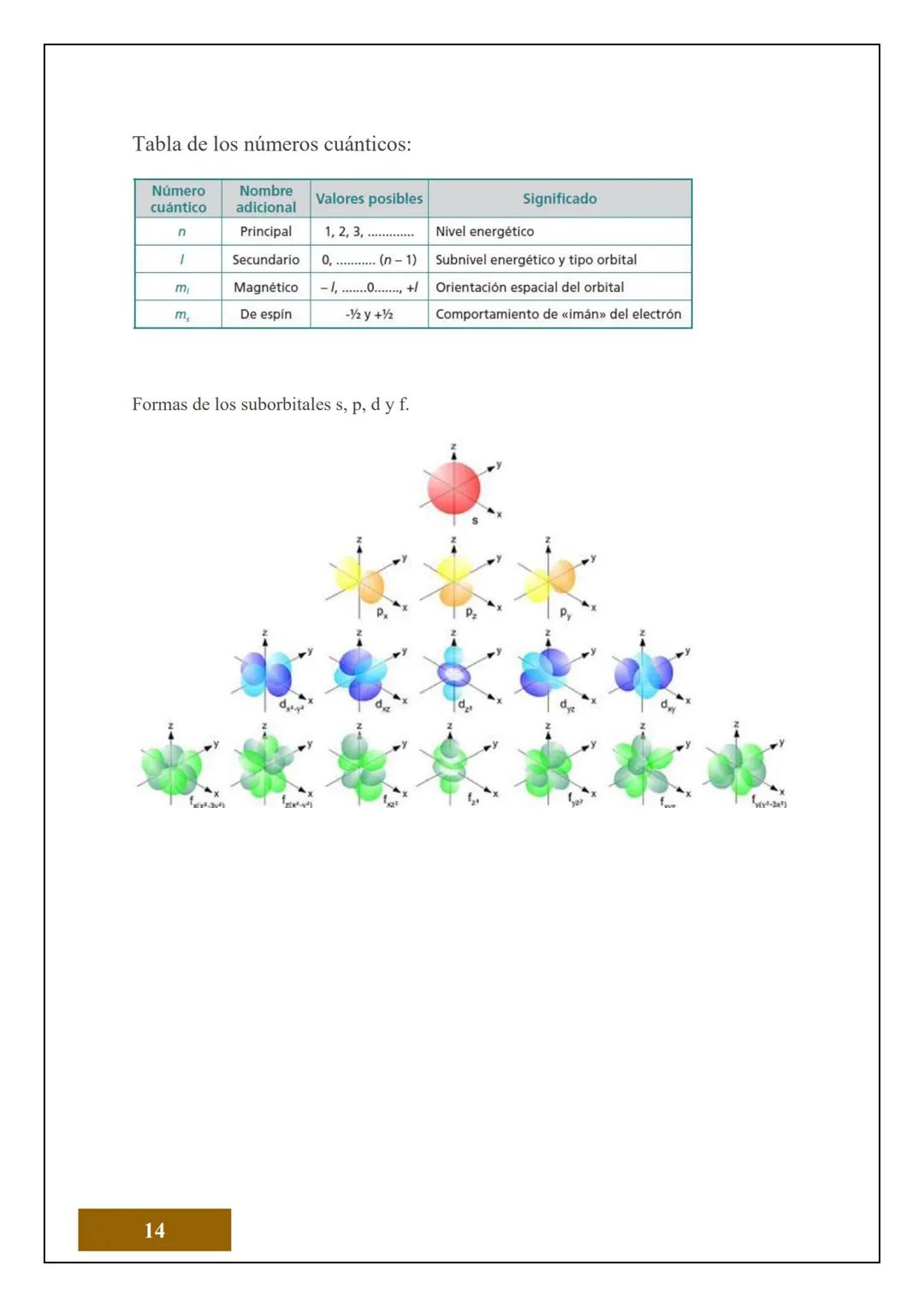
Los orbitales tienen formas geométricas específicas que puedes visualizar. Los orbitales s son esféricos, los p tienen forma de mancuerna, los d son más complejos con formas de trébol, y los f son aún más elaborados.
Cada tipo de orbital puede contener un número máximo de electrones: s=2, p=6, d=10, f=14. Esto se debe a que cada orbital individual puede tener máximo 2 electrones .
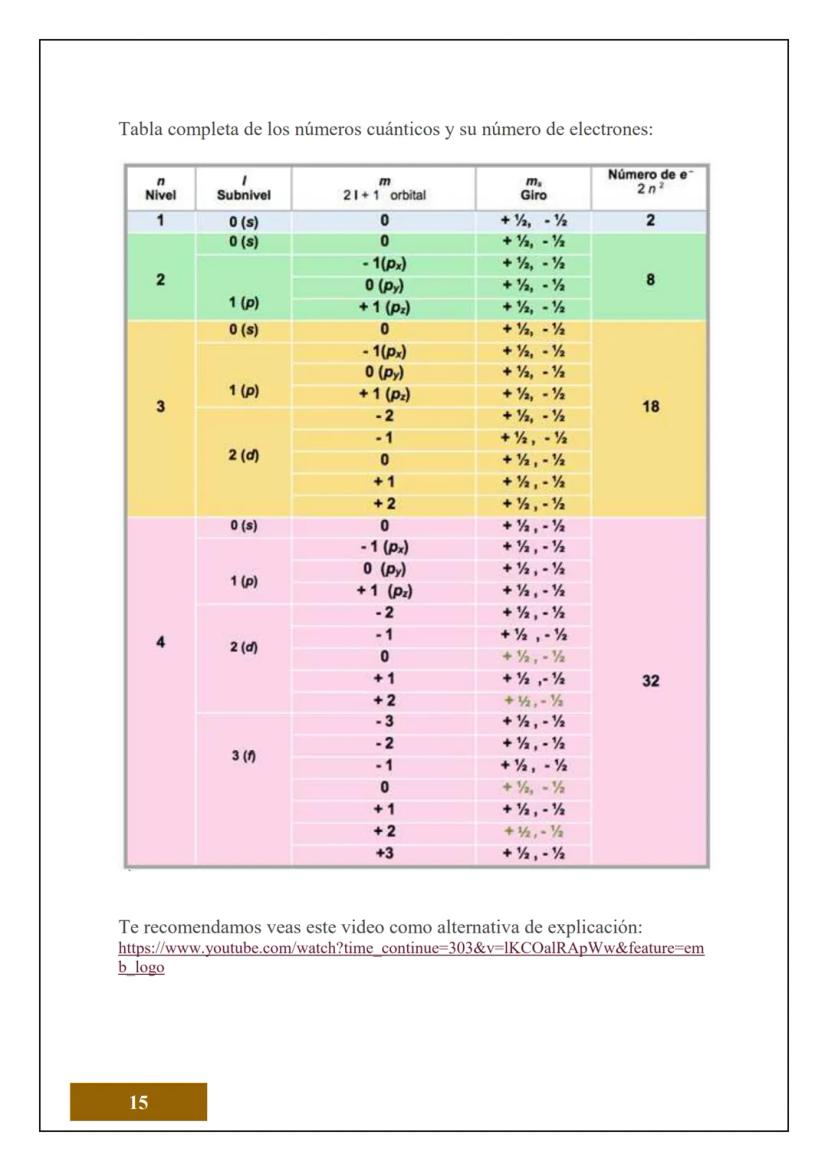
La tabla de números cuánticos te muestra todas las combinaciones posibles para cada nivel energético. Es como un mapa detallado de dónde puede "vivir" cada electrón en el átomo.
Para visualizar mejor: Busca modelos 3D de orbitales en internet, te ayudarán muchísimo a entender sus formas.
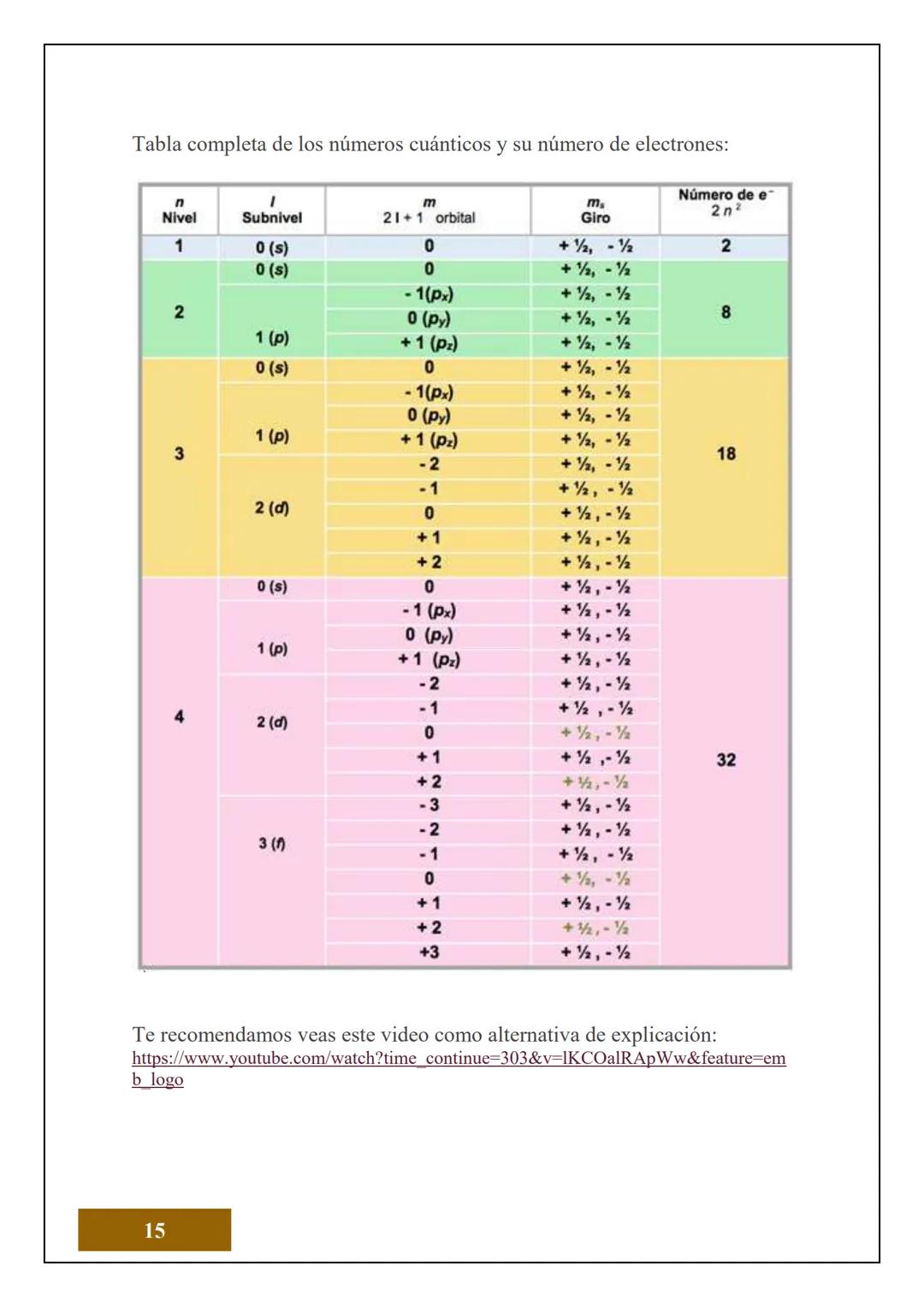
Esta tabla es tu guía maestra para entender cuántos electrones caben en cada nivel. La fórmula 2n² te dice el máximo de electrones por nivel: n=1 caben 2, n=2 caben 8, n=3 caben 18, n=4 caben 32.
Cada orbital individual puede tener máximo 2 electrones con spines opuestos. Por ejemplo, el subnivel p tiene 3 orbitales, entonces puede tener máximo 6 electrones (3 orbitales × 2 electrones).
La progresión es lógica: a medida que te alejas del núcleo, hay más espacio y más orbitales disponibles para los electrones. Es como los asientos en un estadio: las filas de atrás tienen más lugares.
Consejo de estudio: Memoriza la secuencia 2, 8, 18, 32 para los primeros cuatro niveles, te servirá muchísimo.

La configuración electrónica es como escribir la "dirección completa" de todos los electrones en un átomo. Para hacerlo correctamente, tienes que seguir cuatro reglas fundamentales que son como las leyes de tránsito para los electrones.
La regla de Aufbau dice que los electrones siempre van primero a los orbitales de menor energía, como agua que siempre busca el nivel más bajo. Es pura lógica: la naturaleza siempre prefiere la menor energía posible.
El principio de exclusión de Pauli establece que no puede haber dos electrones idénticos en un átomo. Si están en el mismo orbital, deben tener spines opuestos. Es como decir que en una misma habitación puede haber máximo 2 personas, pero una debe ser zurda y otra diestra.
La regla de Hund es súper práctica: cuando tienes varios orbitales de la misma energía (como los tres orbitales p), primero pones un electrón en cada uno, todos con el mismo spin. Después ya puedes aparearlos. Es como llenar primero todos los asientos individuales antes de que alguien se siente al lado de otro.
Analogía útil: Imagínate llenando un estacionamiento: primero ocupas los espacios más cercanos y baratos (menor energía), y evitas estacionarte junto a alguien hasta que no haya más remedio.
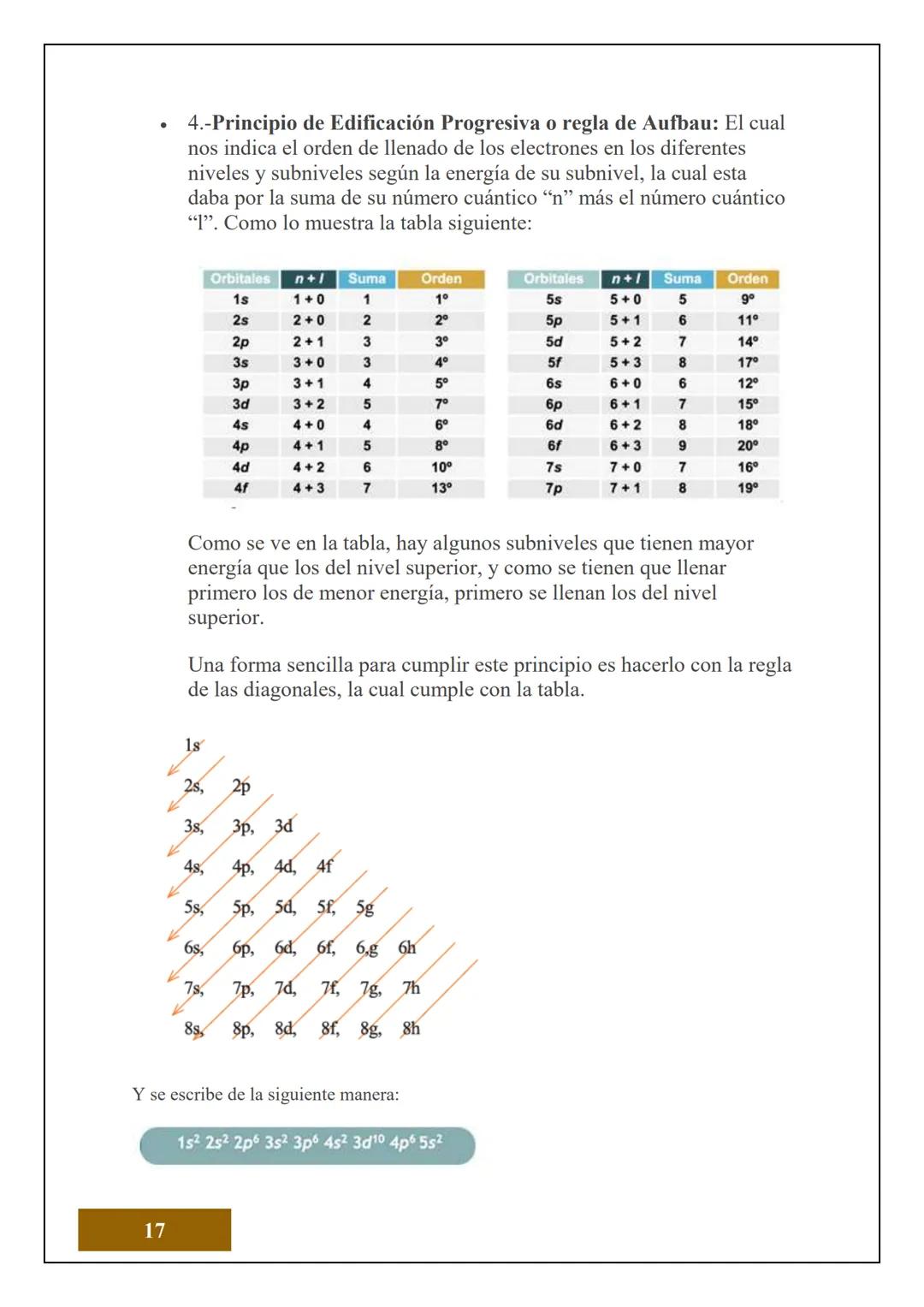
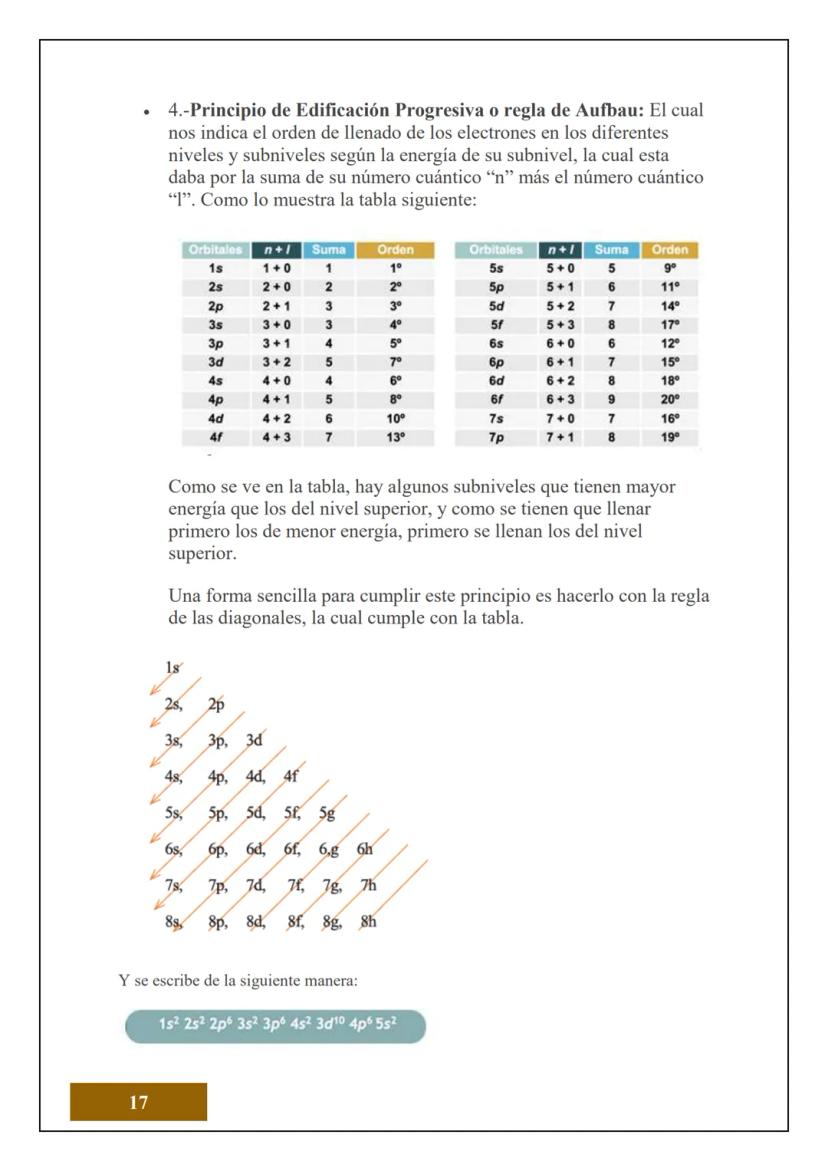
El principio de edificación progresiva te da el orden exacto para llenar los orbitales. La clave está en sumar n+l: el orbital con menor suma se llena primero. Por ejemplo, 4s (4+0=4) se llena antes que 3d (3+2=5), aunque 4s esté en un nivel superior.
La regla de las diagonales es un truco genial para recordar el orden correcto. Simplemente sigues las flechas diagonales: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p, y así sucesivamente.
Esta regla explica por qué algunos elementos tienen propiedades "raras". Por ejemplo, el calcio llena 4s antes que 3d, por eso se comporta diferente a lo que podrías esperar.
La configuración completa se escribe con exponentes que indican cuántos electrones hay en cada subnivel: 1s² 2s² 2p⁶ significa que 1s tiene 2 electrones, 2s tiene 2, y 2p tiene 6.
Tip de oro: Practica el orden de llenado hasta que lo sepas de memoria. Es la base para entender toda la tabla periódica y las propiedades de los elementos.





































































































Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener dificultades para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuario de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser muy difícil reunir toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis notas y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuario de Android
Siempre estaba estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a manejar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZZES Y FLASHCARDS SON SÚPER ÚTILES Y AMO Knowunity AI. TAMBIÉN ES LITERALMENTE COMO CHATGPT PERO MÁS INTELIGENTE!! ME AYUDÓ CON MIS PROBLEMAS DE RÍMEL TAMBIÉN!! Y CON MIS MATERIAS REALES OBVIO! 😍😁😲🤑💗✨🎀😮
Sarah L
usuario de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros – me siento mucho más seguro cuando me preparo para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener dificultades para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuario de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser muy difícil reunir toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis notas y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuario de Android
Siempre estaba estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a manejar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZZES Y FLASHCARDS SON SÚPER ÚTILES Y AMO Knowunity AI. TAMBIÉN ES LITERALMENTE COMO CHATGPT PERO MÁS INTELIGENTE!! ME AYUDÓ CON MIS PROBLEMAS DE RÍMEL TAMBIÉN!! Y CON MIS MATERIAS REALES OBVIO! 😍😁😲🤑💗✨🎀😮
Sarah L
usuario de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros – me siento mucho más seguro cuando me preparo para los exámenes.
Paul T
usuario de iOS
Mauricio sinoe Pérez Carbajal
@mauriciosinoepr
La estructura atómica es la base de toda la química que vas a estudiar este año. Imagínate que pudieras ver dentro de cualquier material y descubrir los "ladrillos" microscópicos que lo forman: eso son los átomos y sus partes.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
¿Sabías que todo lo que tocas está hecho de átomos? El átomo es la unidad más pequeña de la materia que conserva las propiedades de un elemento químico. Es como el "ladrillo" fundamental de todo lo que existe.
Cada átomo tiene una estructura súper organizada: en el centro está el núcleo (cargado positivamente) que contiene protones y neutrones (sin carga). Alrededor del núcleo giran los electrones , como planetas alrededor del sol.
Los protones pesan aproximadamente 1800 veces más que los electrones, por eso cuando hablamos del peso de un átomo, básicamente solo contamos protones y neutrones. Los electrones son súper livianos pero súper importantes: son los que participan en todas las reacciones químicas que estudiarás.
¡Dato curioso! Si un átomo fuera del tamaño de un estadio de fútbol, el núcleo sería como una canica en el centro.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El número atómico es súper fácil de entender: es simplemente cuántos protones tiene un elemento en su núcleo. Este número nunca cambia para un elemento específico (el carbono siempre tiene 6 protones).
La masa atómica es la suma de protones + neutrones en el núcleo. Como los electrones pesan casi nada comparado con estas partículas, no los contamos para la masa.
Los isótopos son una cosa genial: son átomos del mismo elemento (mismo número de protones) pero con diferente cantidad de neutrones. Por ejemplo, todos los carbonos tienen 6 protones, pero pueden tener 5, 6 o 7 neutrones.
Un ion es cuando un átomo gana o pierde electrones. Si pierde electrones se vuelve catión (+) y se hace más pequeño. Si gana electrones se vuelve anión (-) y se agranda debido a la repulsión entre los electrones extra.
Para el examen: Recuerda que el número atómico = protones, y la masa atómica = protones + neutrones.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Cuando un átomo se convierte en anión (gana electrones), su tamaño aumenta. Esto pasa porque los electrones extra se repelen entre sí, "empujándose" y haciendo que el átomo se expanda.
Este concepto es clave para entender por qué algunos elementos forman ciertos tipos de enlaces químicos. Los aniones más grandes tienden a comportarse diferente que los cationes más pequeños.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Olvídate de la imagen clásica de electrones girando en círculos perfectos como planetas. Los orbitales atómicos son zonas del espacio donde hay alta probabilidad de encontrar un electrón, no rutas definidas.
La diferencia es crucial: las órbitas de Bohr eran círculos definidos, pero los orbitales son "nubes de probabilidad". Esto resuelve problemas que el modelo antiguo no podía explicar, como el principio de Heisenberg (no puedes saber exactamente dónde está un electrón y cuánta energía tiene al mismo tiempo).
Los orbitales se definen matemáticamente por la ecuación de Schrödinger. No necesitas resolver esta ecuación (¡es súper complicada!), pero sí entender que de ella salen los números cuánticos que describen exactamente dónde pueden estar los electrones.
Concepto clave: Los orbitales no son rutas, son zonas de probabilidad donde "probablemente" está el electrón.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los números cuánticos son como la "dirección" de cada electrón en el átomo. Son cuatro números que te dicen exactamente dónde vive cada electrón.
n (número cuántico principal): Te dice qué tan lejos está del núcleo . A mayor n, mayor energía y más electrones caben.
l (número cuántico secundario): Define la forma del orbital. l=0 es "s" (esférica), l=1 es "p" (forma de mancuerna), l=2 es "d", l=3 es "f". Puede valer desde 0 hasta n-1.
m (número cuántico magnético): Te dice la orientación espacial del orbital. Puede valer desde -l hasta +l. Por ejemplo, si l=2, entonces m puede ser -2, -1, 0, +1, +2.
s (spin): Es como si el electrón fuera una peonza que gira. Solo puede valer +1/2 o -1/2 (hacia arriba o hacia abajo).
Tip para memorizar: n=distancia, l=forma, m=orientación, s=giro del electrón.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El número cuántico magnético (m) determina cuántas orientaciones diferentes puede tener un orbital. Por ejemplo, el subnivel "p" tiene tres orientaciones: px, py, pz, correspondientes a m=-1, 0, +1.
El spin del electrón es fascinante: como el electrón tiene carga eléctrica y "gira", se comporta como un imán microscópico. Puede girar en dos direcciones (como las manecillas del reloj o al revés), lo que representa con +1/2 y -1/2.
Esta propiedad magnética del electrón explica por qué algunos materiales son magnéticos y otros no. Cuando los spines están desapareados, el material puede ser magnético.
Dato interesante: El spin electrónico es la base de tecnologías como la resonancia magnética y los discos duros de las computadoras.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los orbitales tienen formas geométricas específicas que puedes visualizar. Los orbitales s son esféricos, los p tienen forma de mancuerna, los d son más complejos con formas de trébol, y los f son aún más elaborados.
Cada tipo de orbital puede contener un número máximo de electrones: s=2, p=6, d=10, f=14. Esto se debe a que cada orbital individual puede tener máximo 2 electrones .
La tabla de números cuánticos te muestra todas las combinaciones posibles para cada nivel energético. Es como un mapa detallado de dónde puede "vivir" cada electrón en el átomo.
Para visualizar mejor: Busca modelos 3D de orbitales en internet, te ayudarán muchísimo a entender sus formas.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Esta tabla es tu guía maestra para entender cuántos electrones caben en cada nivel. La fórmula 2n² te dice el máximo de electrones por nivel: n=1 caben 2, n=2 caben 8, n=3 caben 18, n=4 caben 32.
Cada orbital individual puede tener máximo 2 electrones con spines opuestos. Por ejemplo, el subnivel p tiene 3 orbitales, entonces puede tener máximo 6 electrones (3 orbitales × 2 electrones).
La progresión es lógica: a medida que te alejas del núcleo, hay más espacio y más orbitales disponibles para los electrones. Es como los asientos en un estadio: las filas de atrás tienen más lugares.
Consejo de estudio: Memoriza la secuencia 2, 8, 18, 32 para los primeros cuatro niveles, te servirá muchísimo.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La configuración electrónica es como escribir la "dirección completa" de todos los electrones en un átomo. Para hacerlo correctamente, tienes que seguir cuatro reglas fundamentales que son como las leyes de tránsito para los electrones.
La regla de Aufbau dice que los electrones siempre van primero a los orbitales de menor energía, como agua que siempre busca el nivel más bajo. Es pura lógica: la naturaleza siempre prefiere la menor energía posible.
El principio de exclusión de Pauli establece que no puede haber dos electrones idénticos en un átomo. Si están en el mismo orbital, deben tener spines opuestos. Es como decir que en una misma habitación puede haber máximo 2 personas, pero una debe ser zurda y otra diestra.
La regla de Hund es súper práctica: cuando tienes varios orbitales de la misma energía (como los tres orbitales p), primero pones un electrón en cada uno, todos con el mismo spin. Después ya puedes aparearlos. Es como llenar primero todos los asientos individuales antes de que alguien se siente al lado de otro.
Analogía útil: Imagínate llenando un estacionamiento: primero ocupas los espacios más cercanos y baratos (menor energía), y evitas estacionarte junto a alguien hasta que no haya más remedio.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El principio de edificación progresiva te da el orden exacto para llenar los orbitales. La clave está en sumar n+l: el orbital con menor suma se llena primero. Por ejemplo, 4s (4+0=4) se llena antes que 3d (3+2=5), aunque 4s esté en un nivel superior.
La regla de las diagonales es un truco genial para recordar el orden correcto. Simplemente sigues las flechas diagonales: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p, y así sucesivamente.
Esta regla explica por qué algunos elementos tienen propiedades "raras". Por ejemplo, el calcio llena 4s antes que 3d, por eso se comporta diferente a lo que podrías esperar.
La configuración completa se escribe con exponentes que indican cuántos electrones hay en cada subnivel: 1s² 2s² 2p⁶ significa que 1s tiene 2 electrones, 2s tiene 2, y 2p tiene 6.
Tip de oro: Practica el orden de llenado hasta que lo sepas de memoria. Es la base para entender toda la tabla periódica y las propiedades de los elementos.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
4
Herramientas Inteligentes NUEVO
Convierte estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Tarjetas de Estudio Interactivas ✓ Examen Completo de Práctica ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener dificultades para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuario de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser muy difícil reunir toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis notas y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuario de Android
Siempre estaba estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a manejar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZZES Y FLASHCARDS SON SÚPER ÚTILES Y AMO Knowunity AI. TAMBIÉN ES LITERALMENTE COMO CHATGPT PERO MÁS INTELIGENTE!! ME AYUDÓ CON MIS PROBLEMAS DE RÍMEL TAMBIÉN!! Y CON MIS MATERIAS REALES OBVIO! 😍😁😲🤑💗✨🎀😮
Sarah L
usuario de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros – me siento mucho más seguro cuando me preparo para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener dificultades para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuario de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser muy difícil reunir toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis notas y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuario de Android
Siempre estaba estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a manejar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZZES Y FLASHCARDS SON SÚPER ÚTILES Y AMO Knowunity AI. TAMBIÉN ES LITERALMENTE COMO CHATGPT PERO MÁS INTELIGENTE!! ME AYUDÓ CON MIS PROBLEMAS DE RÍMEL TAMBIÉN!! Y CON MIS MATERIAS REALES OBVIO! 😍😁😲🤑💗✨🎀😮
Sarah L
usuario de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros – me siento mucho más seguro cuando me preparo para los exámenes.
Paul T
usuario de iOS