Los enlaces químicos son las fuerzas que mantienen unidos a... Mostrar más
Tipos de Enlaces Químicos: Guía Sencilla

























Tema 3: Enlaces Químicos

¿Cómo se forman los compuestos?
Cuando dos átomos se unen, algo muy interesante pasa: transfieren o comparten electrones. Es como si los átomos hicieran un intercambio para volverse más estables y felices.
Existen diferentes tipos de enlaces químicos dependiendo de cómo los átomos manejen sus electrones. Los principales son el iónico, covalente y metálico. También hay fuerzas más débiles llamadas intermoleculares que actúan entre moléculas.
Los electrones que participan en estos enlaces se llaman electrones de valencia. Son los que están en la capa más externa del átomo, listos para la acción. Son como los jugadores estrella que determinan cómo se va a comportar cada elemento.
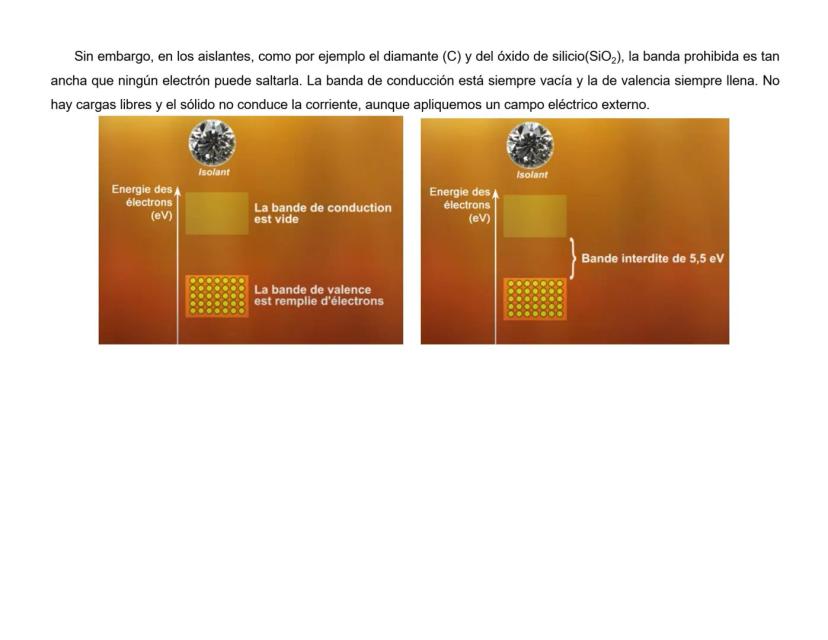
¡Dato curioso! Los enlaces químicos son de naturaleza eléctrica, por eso algunos materiales conducen electricidad y otros no.
Tipos de Enlaces Químicos
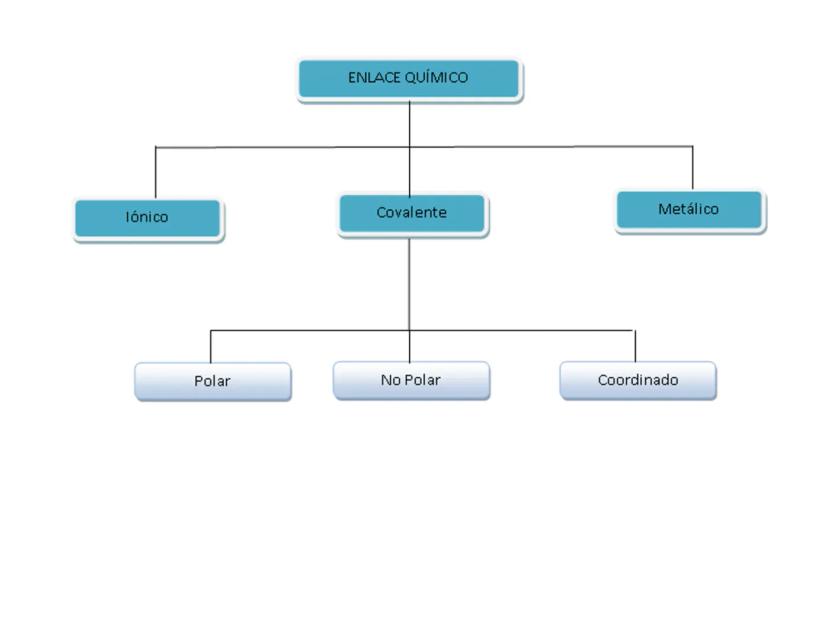
Los enlaces químicos se clasifican en varios tipos principales que debes dominar para tus exámenes:
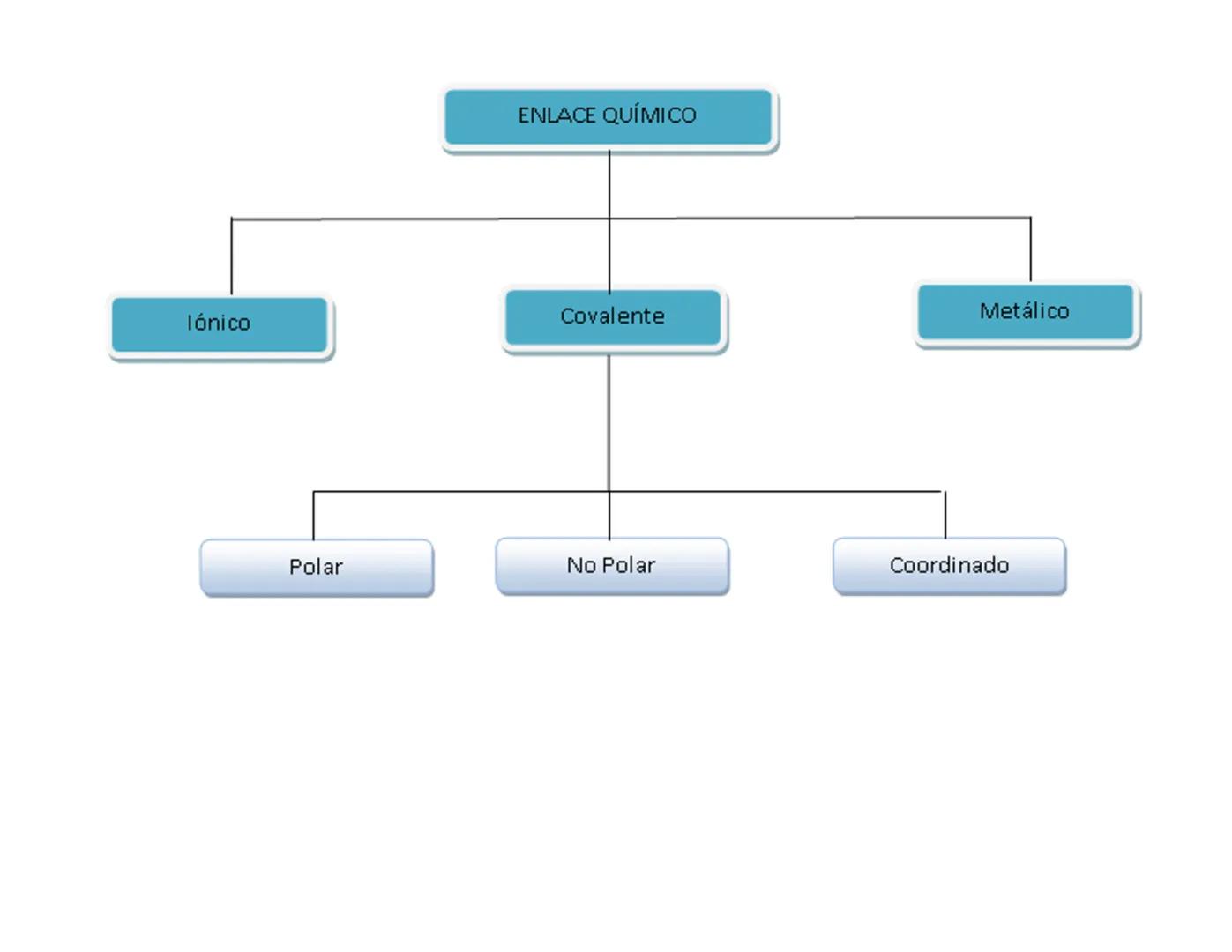
Enlace Iónico: Se forma entre metales y no metales Enlace Covalente: Tiene dos variantes importantes
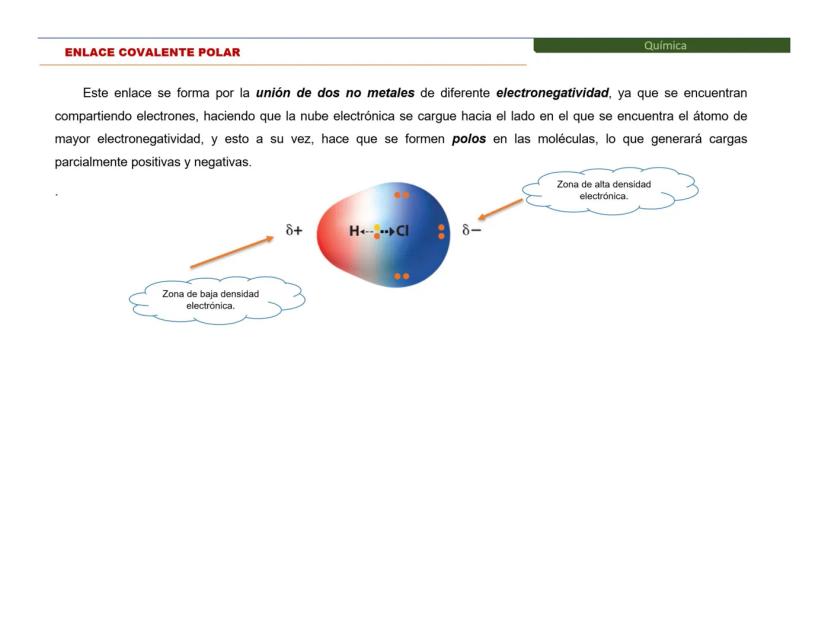
- Polar: Los electrones se comparten de manera desigual
- No Polar: Los electrones se comparten equitativamente
También están el enlace metálico (entre metales) y el coordinado (un tipo especial de covalente).
Tip de estudio: Memoriza esta clasificación porque aparece en casi todos los exámenes de química.
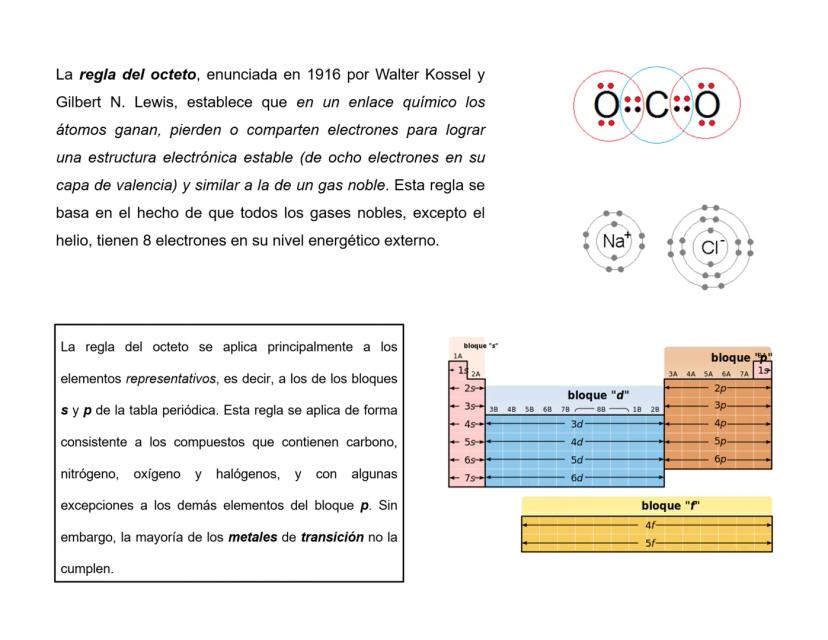
Limitaciones de la Regla del Octeto
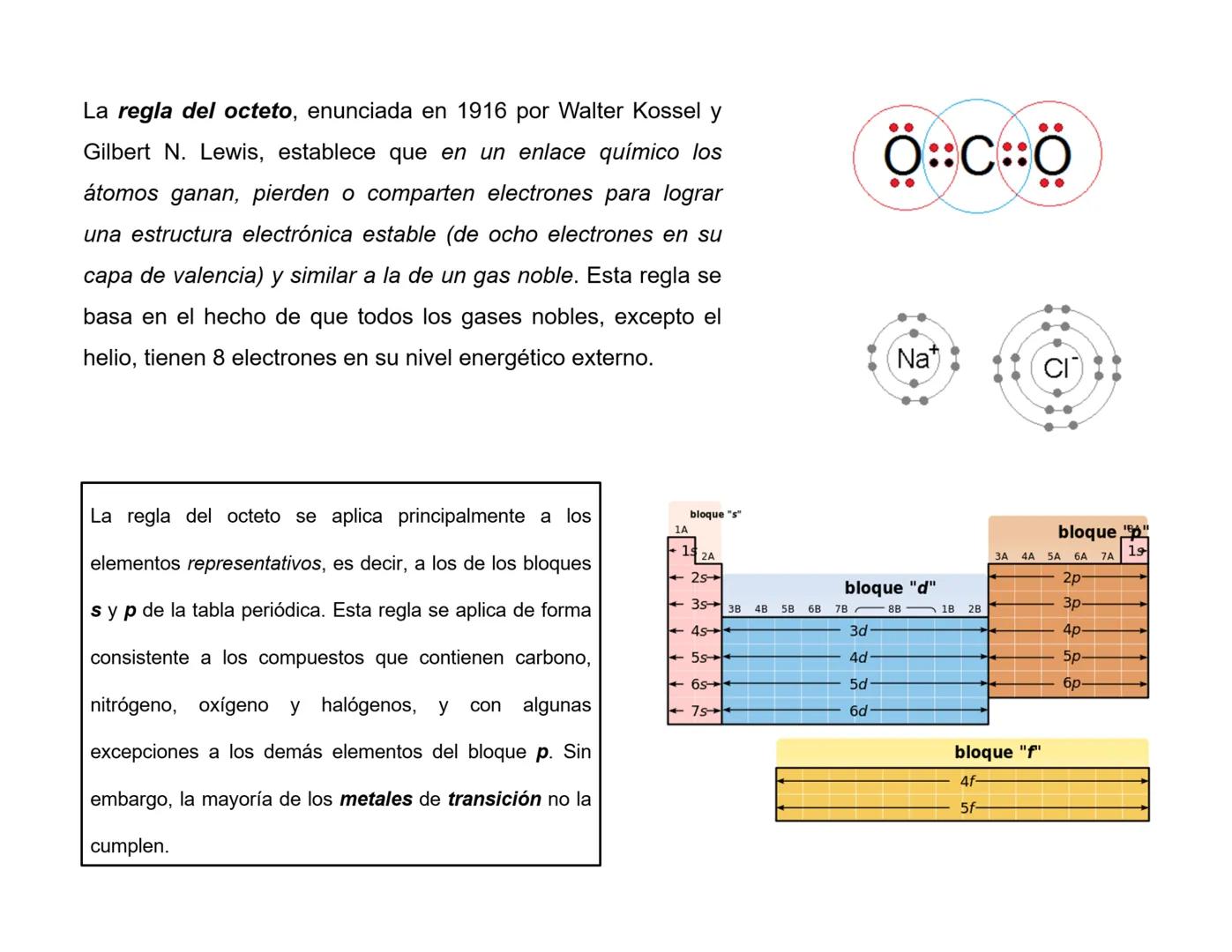
No todos los átomos siguen la famosa regla del octeto (tener 8 electrones en su capa externa). Algunos son rebeldes y tienen sus propias reglas.
Hay tres casos donde la regla se rompe: cuando tienes un número impar de electrones (como el NO con 7 electrones), cuando hay muy pocos electrones (átomos deficientes), o cuando hay demasiados electrones (octeto expandido).
Los átomos con octeto expandido se llaman hipervalentes. Suena complicado, pero solo significa que pueden manejar más de 8 electrones sin problema.
Para recordar: La regla del octeto es útil, pero como toda regla, tiene sus excepciones importantes.

Ejemplos de Excepciones
Aquí tienes ejemplos concretos de cuándo la regla del octeto no funciona:
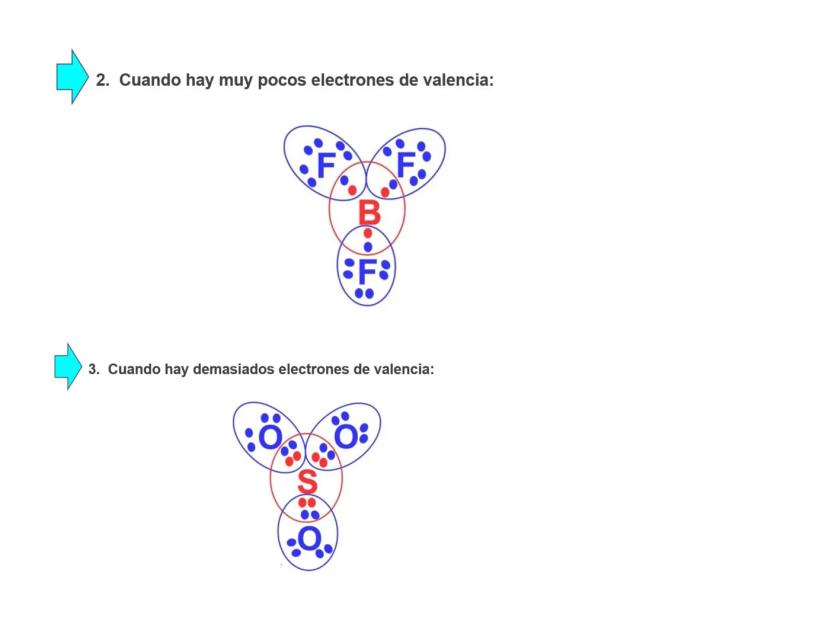
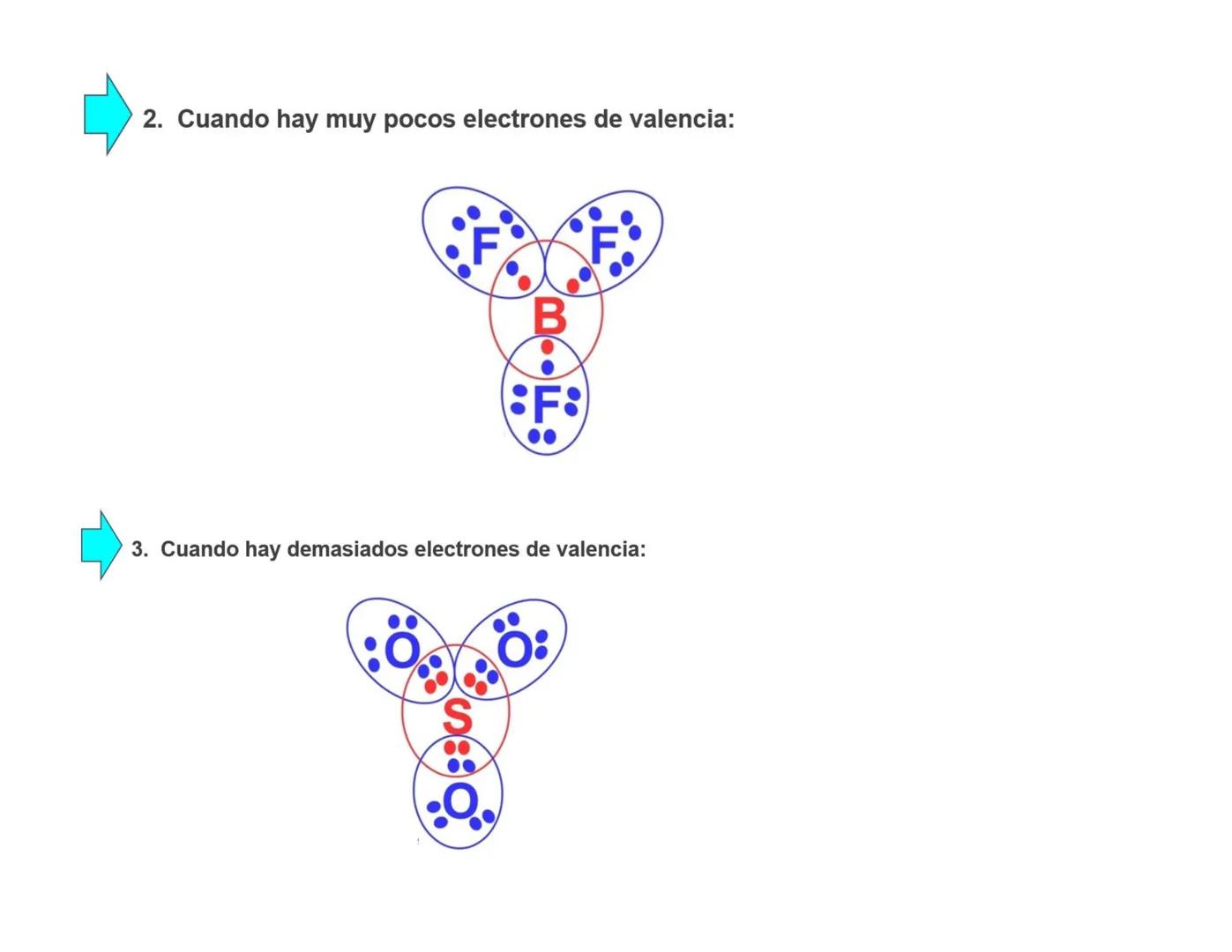
Muy pocos electrones: El boro (B) en BF₃ solo tiene 6 electrones alrededor. Es como si fuera un átomo que no logra completar su "colección" de electrones.
Demasiados electrones: El azufre (S) puede tener más de 8 electrones en algunos compuestos. Es un átomo "ambicioso" que puede manejar electrones extra sin problemas.
Consejo: No te frustres si al principio estas excepciones te confunden. Con práctica, identificarlas se vuelve automático.
Enlace Covalente: Lo Básico
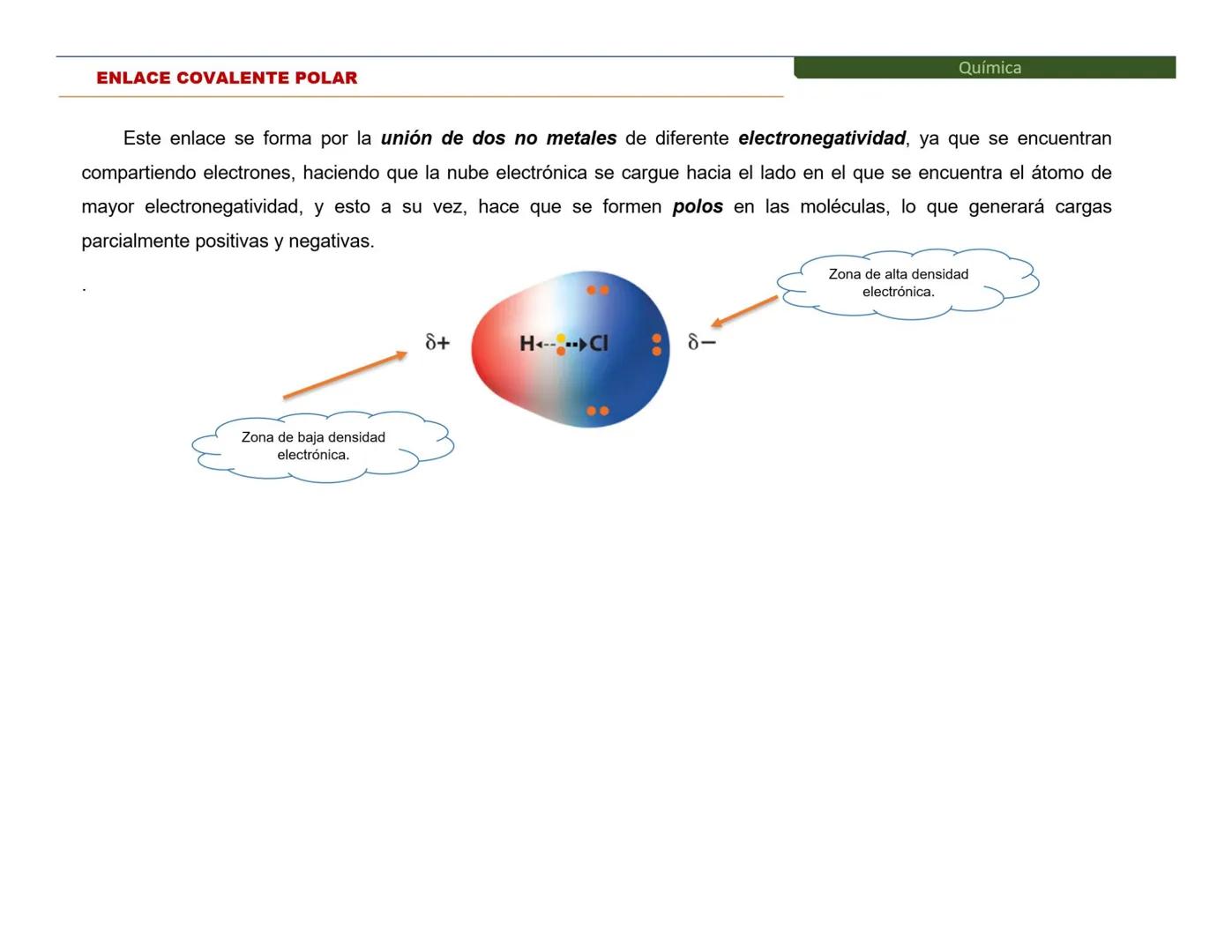
El enlace covalente es el favorito de los no metales. En lugar de robar o regalar electrones como en el iónico, aquí los átomos comparten electrones como buenos amigos.
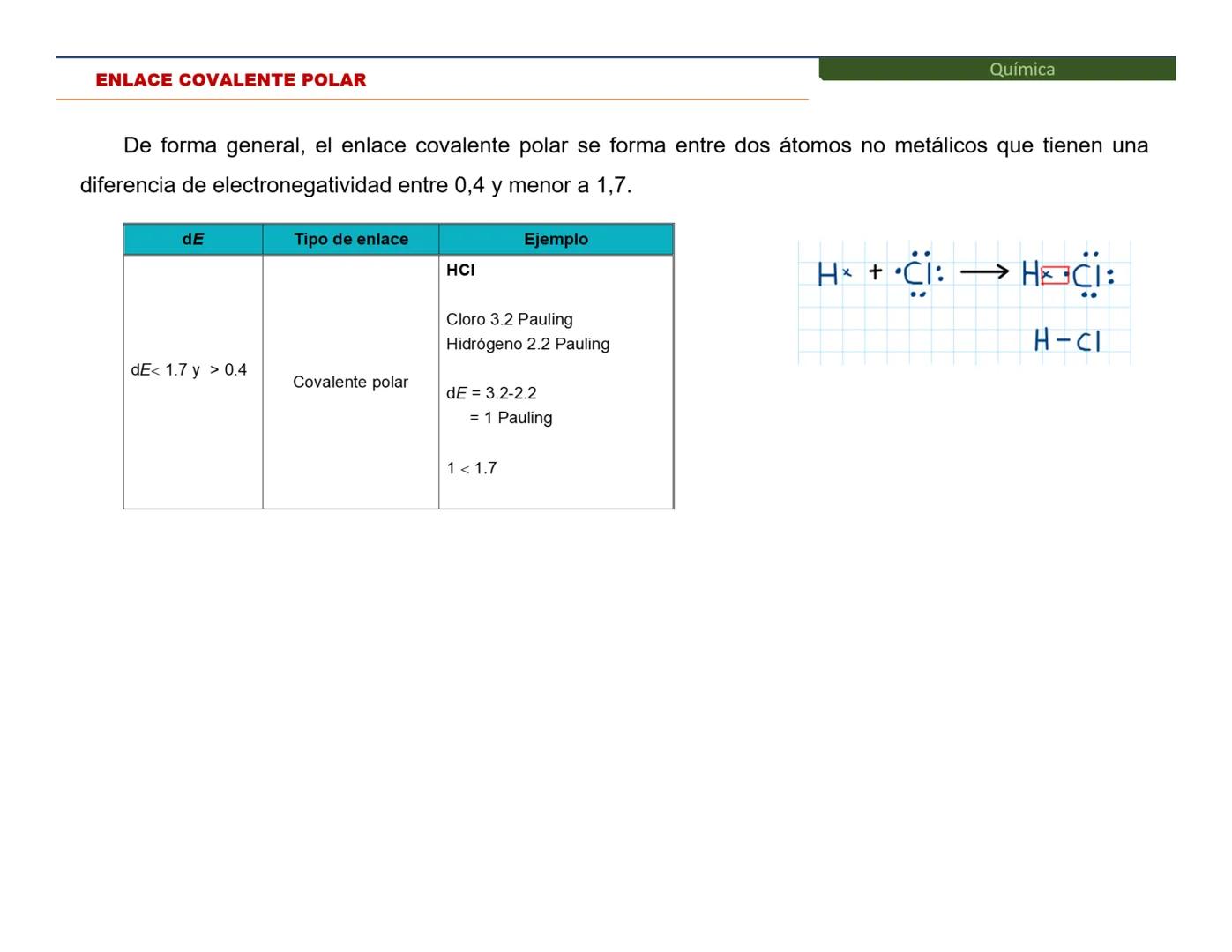
Puedes identificar un enlace covalente cuando la diferencia de electronegatividades es menor a 1.7. Los átomos pueden compartir uno, dos o tres pares de electrones, formando enlaces sencillos, dobles o triples.
Lo genial es que forman moléculas en lugar de cristales. Piensa en el agua (H₂O) o el metano (CH₄): son pequeñas unidades independientes que pueden moverse libremente.
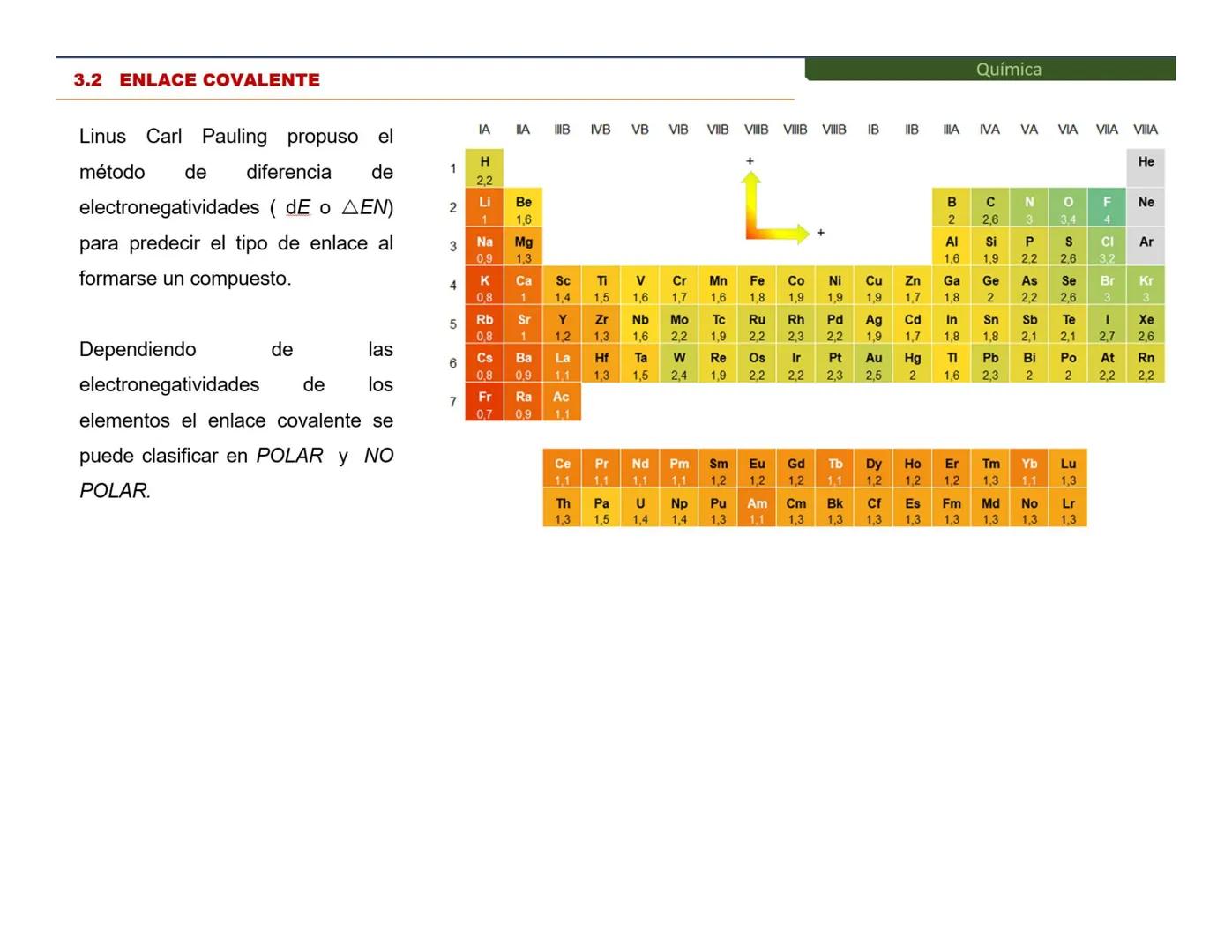
El químico Linus Pauling desarrolló el método de diferencias de electronegatividad para predecir qué tipo de enlace se formará entre dos elementos.
Dato importante: En los enlaces covalentes, los átomos NO ganan ni pierden electrones, solo los comparten.

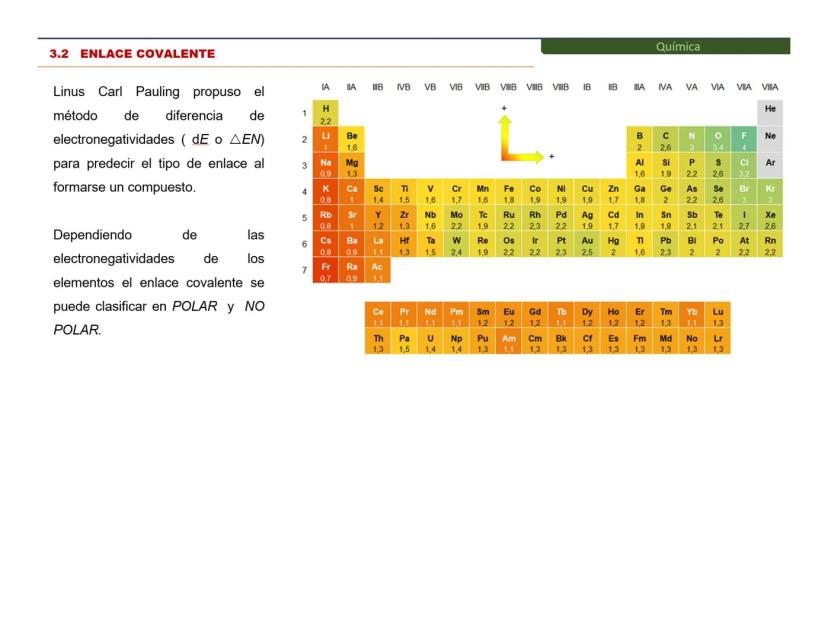
Tabla de Electronegatividades
Esta tabla de electronegatividades de Pauling es tu herramienta secreta para predecir enlaces. Cada elemento tiene un valor que indica qué tan "egoísta" es con los electrones.
Para usar la tabla, simplemente resta las electronegatividades de los dos elementos que se van a enlazar. La diferencia de electronegatividades (ΔEN) te dirá qué tipo de enlace esperar.
Los elementos más electronegativos (como el flúor con 4.0) son los más "codiciosos" de electrones. Los menos electronegativos (como el francio con 0.7) son más "generosos".
Truco: Memoriza que el flúor es el más electronegativo y los metales alcalinos son los menos electronegativos.
Enlace Covalente No Polar
El enlace covalente no polar se forma cuando dos átomos idénticos se unen, como Cl₂ o O₂. Es el enlace más "justo" porque ambos átomos tienen exactamente la misma fuerza para atraer electrones.
La diferencia de electronegatividad es cero (o menor a 0.4). Es como dos personas de la misma fuerza jalando una cuerda: nadie gana, así que comparten por igual.
Un ejemplo perfecto es el cloro gaseoso (Cl₂): ambos átomos de cloro tienen electronegatividad de 3.2, entonces 3.2 - 3.2 = 0.
Para recordar: Si ΔEN < 0.4, tienes un enlace covalente no polar.

Tipos de Enlaces Covalentes No Polares
Los átomos pueden compartir diferentes cantidades de electrones, creando enlaces de distinta "fuerza":
Enlaces sencillos: Comparten un par de electrones . Es como darse la mano.
Enlaces dobles: Comparten dos pares de electrones . Es como darse ambas manos.
Enlaces triples: Comparten tres pares de electrones (N≡N). Es el abrazo más fuerte posible entre átomos.
Dato curioso: Mientras más pares de electrones compartan, más fuerte y corto será el enlace.

Propiedades del Enlace Covalente No Polar
Las moléculas con enlaces covalentes no polares tienen características muy específicas que debes conocer:
Son malos conductores de calor y electricidad porque no tienen cargas libres. Tienen baja solubilidad en agua porque "lo similar disuelve lo similar" y el agua es polar.
Generalmente son gases a temperatura ambiente (como O₂, N₂, Cl₂), aunque algunos pueden ser líquidos o sólidos. Sus puntos de fusión y ebullición son bajos porque las fuerzas entre moléculas son débiles.
Presentan actividad química mediana - ni muy reactivos ni totalmente inertes. Las moléculas formadas son típicamente diatómicas (dos átomos iguales).
Para exámenes: Estas propiedades aparecen frecuentemente en preguntas de opción múltiple.

















Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
Contenidos más populares de Química
9química
química
Mapa metabólico
Mapa metabólico, glucólisis, gluconeogénesis, lípidos, vía de las pentosas, ciclo de krebs
Examen ecoems unam
Estudiar para el examen de ecoems 2026 unam
Quimica ECOEMS(Comipems)
resumen de los temas de quimica que se presentarán en el próximo examen de nivel media superior en la zona metropolitana de el valle de México
Método de Tanteo
Balanceo de ecuaciones químicas
química
propiedades de los elementos, compuestos, reacciones químicas y leyes de la química.
Quimica
Este quiz evalúa tus conocimientos sobre diversos temas de química, desde conceptos básicos hasta reacciones y compuestos.
LIPIDOS.
RESUMEN
Temario y Formulario de Quimica General
Vienen varios conceptos acerca de Quimica General, un apartado de formulas para usarlo de repaso y aplicarlo en ejercicios. Es un resumen de temas relacionados a Quimica General.
Contenidos más populares
9Jerarquía de operaciones
Te enseña la jerarquía de operaciones y también te ecplica que son y como las puedes hacer
química
química
Sistema óseo
Función, tipos, etcétera
Mapa metabólico
Mapa metabólico, glucólisis, gluconeogénesis, lípidos, vía de las pentosas, ciclo de krebs
Célula animal y vegetal
En resumen, este documento te habla sobre qué es, características, diferencias y similitudes de la célula animal y célula vegetal.💗
Matemáticas
matemáticas
Examen mate
matemáticas
Mapa mental - Sistema Nervioso
Mapa mental sobre el sistema nervioso
Historia ECOEMS (Comipems)
Breve resumen de los temas de historia universal del examen del examen de media superior ECOEMS del valle de México
¿No encuentras lo que buscas? Explora otros temas.
Reseñas de nuestros usuarios. Ellos obtuvieron todo lo bueno — y tú también lo harías.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Tipos de Enlaces Químicos: Guía Sencilla
Los enlaces químicos son las fuerzas que mantienen unidos a los átomos para formar compuestos. Imagínate que son como el "pegamento" invisible que permite que los elementos se combinen y creen todas las sustancias que conoces, desde el agua hasta... Mostrar más

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Tema 3: Enlaces Químicos

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
¿Cómo se forman los compuestos?
Cuando dos átomos se unen, algo muy interesante pasa: transfieren o comparten electrones. Es como si los átomos hicieran un intercambio para volverse más estables y felices.
Existen diferentes tipos de enlaces químicos dependiendo de cómo los átomos manejen sus electrones. Los principales son el iónico, covalente y metálico. También hay fuerzas más débiles llamadas intermoleculares que actúan entre moléculas.
Los electrones que participan en estos enlaces se llaman electrones de valencia. Son los que están en la capa más externa del átomo, listos para la acción. Son como los jugadores estrella que determinan cómo se va a comportar cada elemento.
¡Dato curioso! Los enlaces químicos son de naturaleza eléctrica, por eso algunos materiales conducen electricidad y otros no.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Tipos de Enlaces Químicos
Los enlaces químicos se clasifican en varios tipos principales que debes dominar para tus exámenes:
Enlace Iónico: Se forma entre metales y no metales Enlace Covalente: Tiene dos variantes importantes
- Polar: Los electrones se comparten de manera desigual
- No Polar: Los electrones se comparten equitativamente
También están el enlace metálico (entre metales) y el coordinado (un tipo especial de covalente).
Tip de estudio: Memoriza esta clasificación porque aparece en casi todos los exámenes de química.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Limitaciones de la Regla del Octeto
No todos los átomos siguen la famosa regla del octeto (tener 8 electrones en su capa externa). Algunos son rebeldes y tienen sus propias reglas.
Hay tres casos donde la regla se rompe: cuando tienes un número impar de electrones (como el NO con 7 electrones), cuando hay muy pocos electrones (átomos deficientes), o cuando hay demasiados electrones (octeto expandido).
Los átomos con octeto expandido se llaman hipervalentes. Suena complicado, pero solo significa que pueden manejar más de 8 electrones sin problema.
Para recordar: La regla del octeto es útil, pero como toda regla, tiene sus excepciones importantes.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Ejemplos de Excepciones
Aquí tienes ejemplos concretos de cuándo la regla del octeto no funciona:
Muy pocos electrones: El boro (B) en BF₃ solo tiene 6 electrones alrededor. Es como si fuera un átomo que no logra completar su "colección" de electrones.
Demasiados electrones: El azufre (S) puede tener más de 8 electrones en algunos compuestos. Es un átomo "ambicioso" que puede manejar electrones extra sin problemas.
Consejo: No te frustres si al principio estas excepciones te confunden. Con práctica, identificarlas se vuelve automático.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Enlace Covalente: Lo Básico
El enlace covalente es el favorito de los no metales. En lugar de robar o regalar electrones como en el iónico, aquí los átomos comparten electrones como buenos amigos.
Puedes identificar un enlace covalente cuando la diferencia de electronegatividades es menor a 1.7. Los átomos pueden compartir uno, dos o tres pares de electrones, formando enlaces sencillos, dobles o triples.
Lo genial es que forman moléculas en lugar de cristales. Piensa en el agua (H₂O) o el metano (CH₄): son pequeñas unidades independientes que pueden moverse libremente.
El químico Linus Pauling desarrolló el método de diferencias de electronegatividad para predecir qué tipo de enlace se formará entre dos elementos.
Dato importante: En los enlaces covalentes, los átomos NO ganan ni pierden electrones, solo los comparten.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Tabla de Electronegatividades
Esta tabla de electronegatividades de Pauling es tu herramienta secreta para predecir enlaces. Cada elemento tiene un valor que indica qué tan "egoísta" es con los electrones.
Para usar la tabla, simplemente resta las electronegatividades de los dos elementos que se van a enlazar. La diferencia de electronegatividades (ΔEN) te dirá qué tipo de enlace esperar.
Los elementos más electronegativos (como el flúor con 4.0) son los más "codiciosos" de electrones. Los menos electronegativos (como el francio con 0.7) son más "generosos".
Truco: Memoriza que el flúor es el más electronegativo y los metales alcalinos son los menos electronegativos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Enlace Covalente No Polar
El enlace covalente no polar se forma cuando dos átomos idénticos se unen, como Cl₂ o O₂. Es el enlace más "justo" porque ambos átomos tienen exactamente la misma fuerza para atraer electrones.
La diferencia de electronegatividad es cero (o menor a 0.4). Es como dos personas de la misma fuerza jalando una cuerda: nadie gana, así que comparten por igual.
Un ejemplo perfecto es el cloro gaseoso (Cl₂): ambos átomos de cloro tienen electronegatividad de 3.2, entonces 3.2 - 3.2 = 0.
Para recordar: Si ΔEN < 0.4, tienes un enlace covalente no polar.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Tipos de Enlaces Covalentes No Polares
Los átomos pueden compartir diferentes cantidades de electrones, creando enlaces de distinta "fuerza":
Enlaces sencillos: Comparten un par de electrones . Es como darse la mano.
Enlaces dobles: Comparten dos pares de electrones . Es como darse ambas manos.
Enlaces triples: Comparten tres pares de electrones (N≡N). Es el abrazo más fuerte posible entre átomos.
Dato curioso: Mientras más pares de electrones compartan, más fuerte y corto será el enlace.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Propiedades del Enlace Covalente No Polar
Las moléculas con enlaces covalentes no polares tienen características muy específicas que debes conocer:
Son malos conductores de calor y electricidad porque no tienen cargas libres. Tienen baja solubilidad en agua porque "lo similar disuelve lo similar" y el agua es polar.
Generalmente son gases a temperatura ambiente (como O₂, N₂, Cl₂), aunque algunos pueden ser líquidos o sólidos. Sus puntos de fusión y ebullición son bajos porque las fuerzas entre moléculas son débiles.
Presentan actividad química mediana - ni muy reactivos ni totalmente inertes. Las moléculas formadas son típicamente diatómicas (dos átomos iguales).
Para exámenes: Estas propiedades aparecen frecuentemente en preguntas de opción múltiple.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
Contenidos más populares de Química
9química
química
Mapa metabólico
Mapa metabólico, glucólisis, gluconeogénesis, lípidos, vía de las pentosas, ciclo de krebs
Examen ecoems unam
Estudiar para el examen de ecoems 2026 unam
Quimica ECOEMS(Comipems)
resumen de los temas de quimica que se presentarán en el próximo examen de nivel media superior en la zona metropolitana de el valle de México
Método de Tanteo
Balanceo de ecuaciones químicas
química
propiedades de los elementos, compuestos, reacciones químicas y leyes de la química.
Quimica
Este quiz evalúa tus conocimientos sobre diversos temas de química, desde conceptos básicos hasta reacciones y compuestos.
LIPIDOS.
RESUMEN
Temario y Formulario de Quimica General
Vienen varios conceptos acerca de Quimica General, un apartado de formulas para usarlo de repaso y aplicarlo en ejercicios. Es un resumen de temas relacionados a Quimica General.
Contenidos más populares
9Jerarquía de operaciones
Te enseña la jerarquía de operaciones y también te ecplica que son y como las puedes hacer
química
química
Sistema óseo
Función, tipos, etcétera
Mapa metabólico
Mapa metabólico, glucólisis, gluconeogénesis, lípidos, vía de las pentosas, ciclo de krebs
Célula animal y vegetal
En resumen, este documento te habla sobre qué es, características, diferencias y similitudes de la célula animal y célula vegetal.💗
Matemáticas
matemáticas
Examen mate
matemáticas
Mapa mental - Sistema Nervioso
Mapa mental sobre el sistema nervioso
Historia ECOEMS (Comipems)
Breve resumen de los temas de historia universal del examen del examen de media superior ECOEMS del valle de México
¿No encuentras lo que buscas? Explora otros temas.
Reseñas de nuestros usuarios. Ellos obtuvieron todo lo bueno — y tú también lo harías.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.