¿Sabías que toda la química se basa en entender cómo... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Knowunity AI
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
58
•
Actualizado May 23, 2026
•
Jazmin Rangel
@jazminran_tzia9
¿Sabías que toda la química se basa en entender cómo... Mostrar más
















El número atómico es básicamente la "identificación" de cada elemento - es el número de protones en el núcleo y se representa con la letra "Z". Piensa en esto como el ADN de cada átomo.
Los isótopos son como gemelos del mismo elemento que solo difieren en el número de neutrones. Esto significa que tienen el mismo número atómico pero diferente masa atómica.
La masa atómica se calcula sumando protones + neutrones. Es súper importante para resolver problemas en química, así que memoriza esta fórmula simple.
💡 Tip clave: El número atómico nunca cambia para un elemento, pero los neutrones sí pueden variar creando isótopos.

Los metales están del lado izquierdo de la tabla periódica porque ceden electrones fácilmente - tienen solo 1, 2 o 3 electrones en su capa externa. Son brillantes, conducen electricidad y calor, y son maleables.
Los no metales se ubican a la derecha porque tienen 6 o 7 electrones en su última capa y prefieren "robar" electrones de otros elementos. Los gases nobles (grupo 18) no interactúan porque ya tienen su capa completa.
Los semimetales son elementos "indecisos" - a veces actúan como metales y otras veces no, dependiendo de las condiciones.
Los períodos representan el número de niveles energéticos que tienen los átomos. Mientras más abajo en la tabla, más niveles energéticos.
💡 Dato curioso: El hidrógeno es la excepción rara - está con los metales pero es un gas, no un metal.

Los enlaces iónicos se forman cuando los átomos se vuelven iones con cargas opuestas. Es como el magnetismo - los opuestos se atraen y crean enlaces súper fuertes.
Los cationes son iones positivos (perdieron electrones) y los aniones son iones negativos (ganaron electrones). Los aniones siempre terminan en "-uro" como cloruro o sulfuro.
La transferencia de electrones ocurre cuando un átomo pierde electrones y otro los gana completamente. El sodio y cloro son el ejemplo clásico de esto.
Los enlaces covalentes se forman cuando los átomos comparten electrones en lugar de transferirlos. Estos son más comunes en los seres vivos que los enlaces iónicos.
💡 Recuerda: Iónico = transferencia completa, Covalente = compartir electrones.

Las reacciones exotérmicas liberan calor - el recipiente se siente caliente al tocarlo. Las reacciones endotérmicas absorben calor - el recipiente se siente frío.
La Ley de conservación de la materia dice que los átomos no se crean ni destruyen, solo se reorganizan. Lo mismo pasa con la Ley de conservación de la energía.
Las ecuaciones químicas son el lenguaje que usan los químicos para describir qué sucede en una reacción. Te permiten predecir productos y calcular proporciones exactas.
La termoquímica estudia cómo el calor se relaciona con las reacciones químicas. Es fundamental para entender por qué algunas reacciones necesitan calor y otras lo producen.
💡 Concepto clave: En cualquier reacción, la cantidad total de materia y energía antes = después, solo cambia de forma.

Las reacciones de síntesis o combinación siguen el patrón A + B → AB. Dos o más sustancias se unen para formar una sola más compleja.
Ejemplos típicos incluyen: metal + oxígeno = óxido metálico, o no metal + oxígeno = óxido no metálico. También óxido + agua puede formar hidróxidos o ácidos.
Las reacciones de descomposición hacen exactamente lo opuesto: AB → A + B. Un compuesto complejo se rompe en sustancias más simples.
Muchas descomposiciones necesitan calor para ocurrir. Los compuestos con oxígeno son especialmente propensos a descomponerse cuando se calientan.
💡 Tip para exámenes: Síntesis = construir (juntar), Descomposición = demoler (separar).

En la sustitución simple, un elemento "echa fuera" a otro de un compuesto. El patrón es AB + C → A + CB.
Tienes que identificar qué elementos pueden intercambiarse: los que forman cationes sustituyen cationes, y los que forman aniones sustituyen aniones.
Un elemento puro reacciona con un compuesto acuoso para producir un nuevo compuesto acuoso y un elemento puro diferente.
El truco está en predecir si la reacción realmente ocurrirá - depende de la serie de actividad de los metales.
💡 Visualiza esto: Es como un baile donde los elementos cambian de pareja, pero solo si el "nuevo" es más activo que el que está.

La sustitución doble es como un intercambio de parejas: AX + BZ → AZ + BX. Los cationes intercambian aniones entre dos compuestos.
Estas reacciones solo ocurren si se cumple una condición específica: formación de precipitado, obtención de agua/gas, o desprendimiento de calor.
Los tipos principales incluyen neutralización , formación de precipitados insolubles, y formación de gases.
Las reacciones ácido-base siempre producen sal + agua + calor. Los precipitados se indican con (s) y los gases con una flecha hacia arriba ↑.
💡 Regla de oro: Si no se forma precipitado, gas, agua o hay cambio de calor, la reacción de doble sustitución NO ocurre.

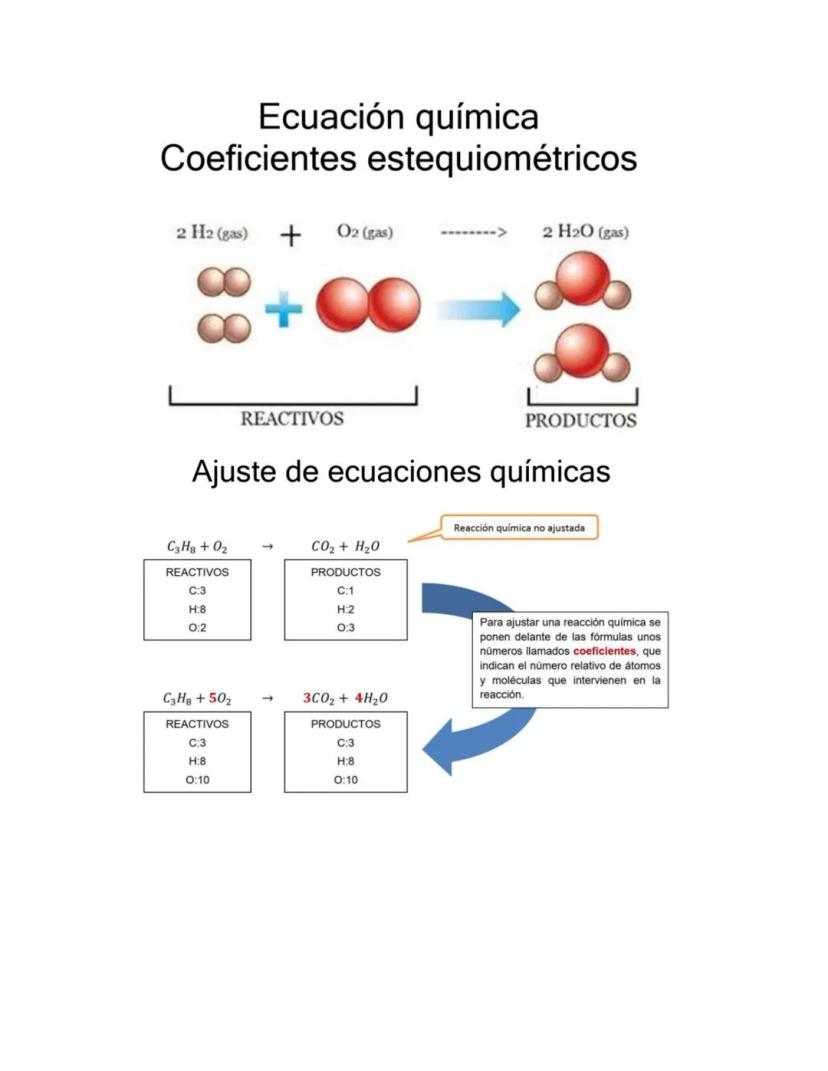
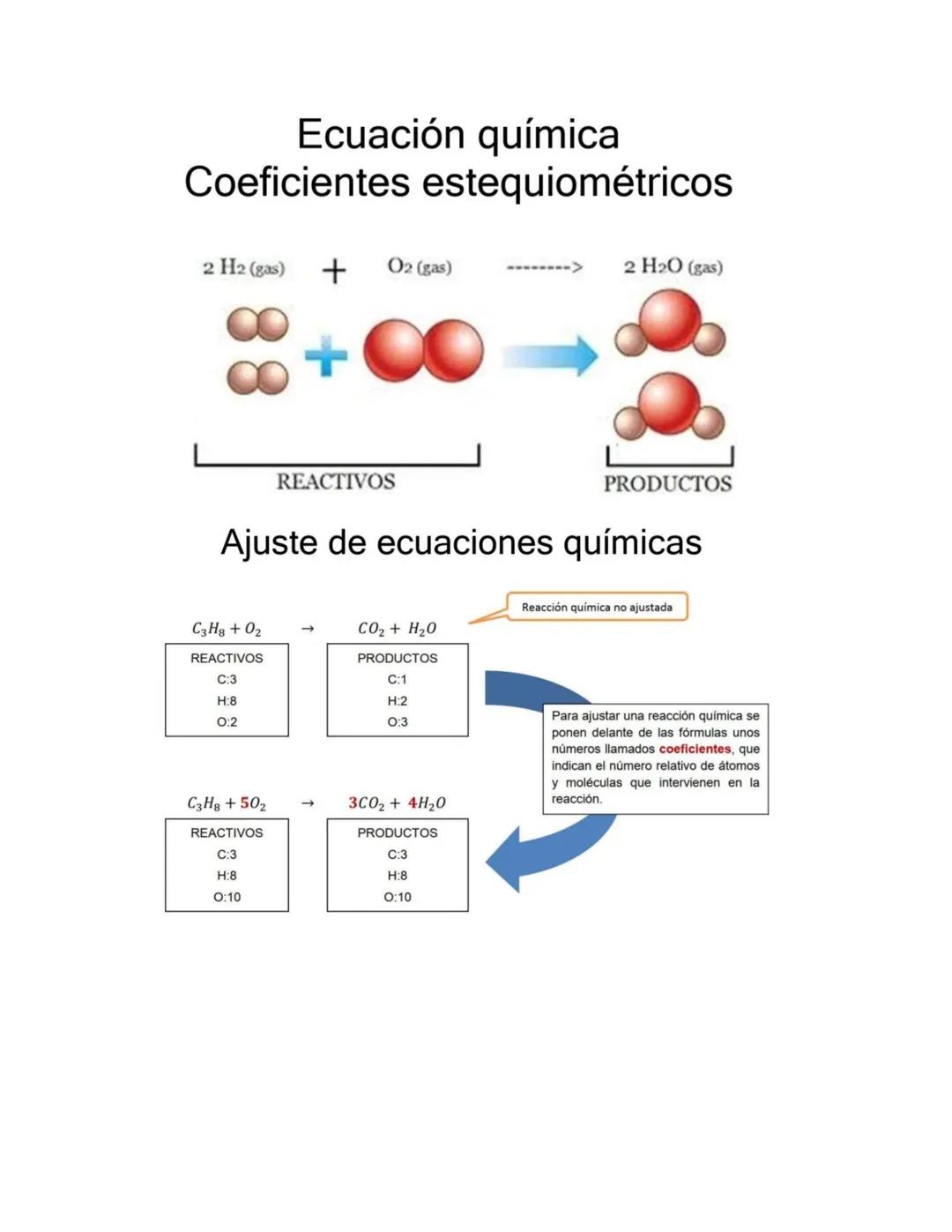
El balanceo por tanteo es el método básico para igualar átomos en ambos lados de la ecuación. Esto verifica la Ley de Conservación de la Materia.
El orden correcto es: primero balancear metales, luego no metales, y al final oxígeno e hidrógeno. Los coeficientes van al frente de cada compuesto.
Multiplica los coeficientes por los subíndices para contar átomos totales. Si los números no coinciden en ambos lados, ajusta los coeficientes.
Siempre verifica tu respuesta final contando nuevamente todos los átomos de cada elemento en reactivos y productos.
💡 Estrategia efectiva: Empieza con el compuesto más complejo y deja los elementos puros para el final del balanceo.

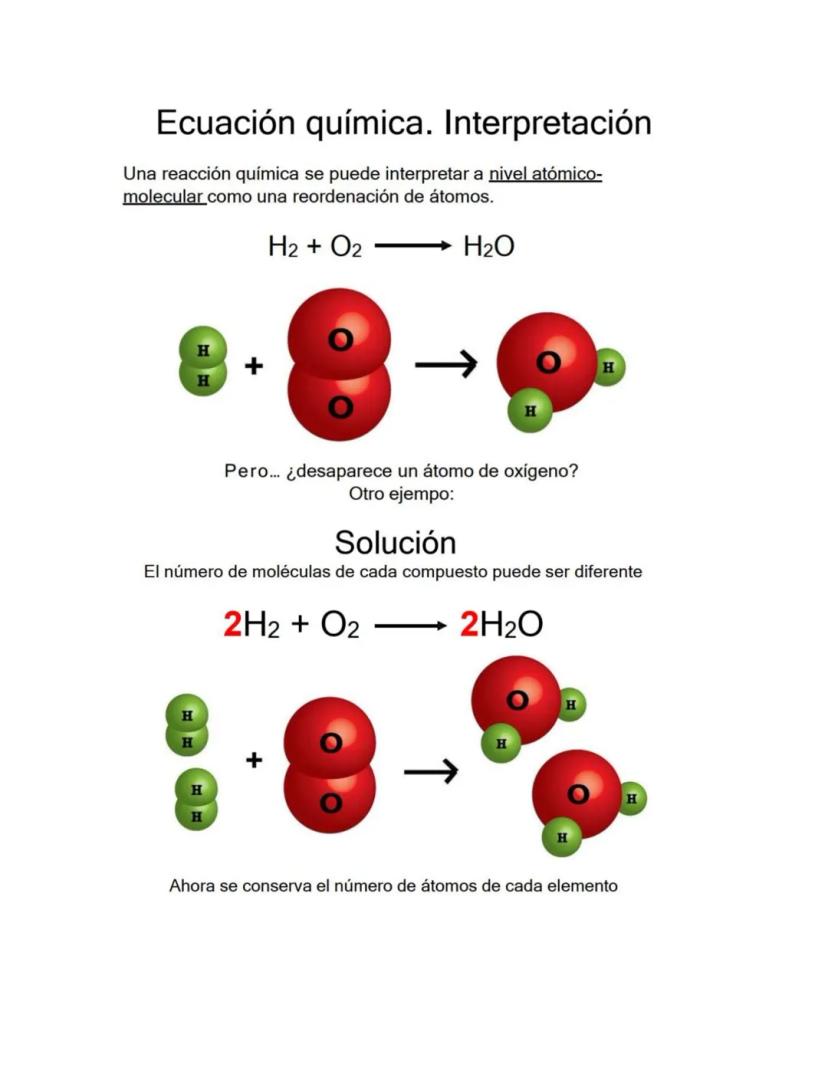
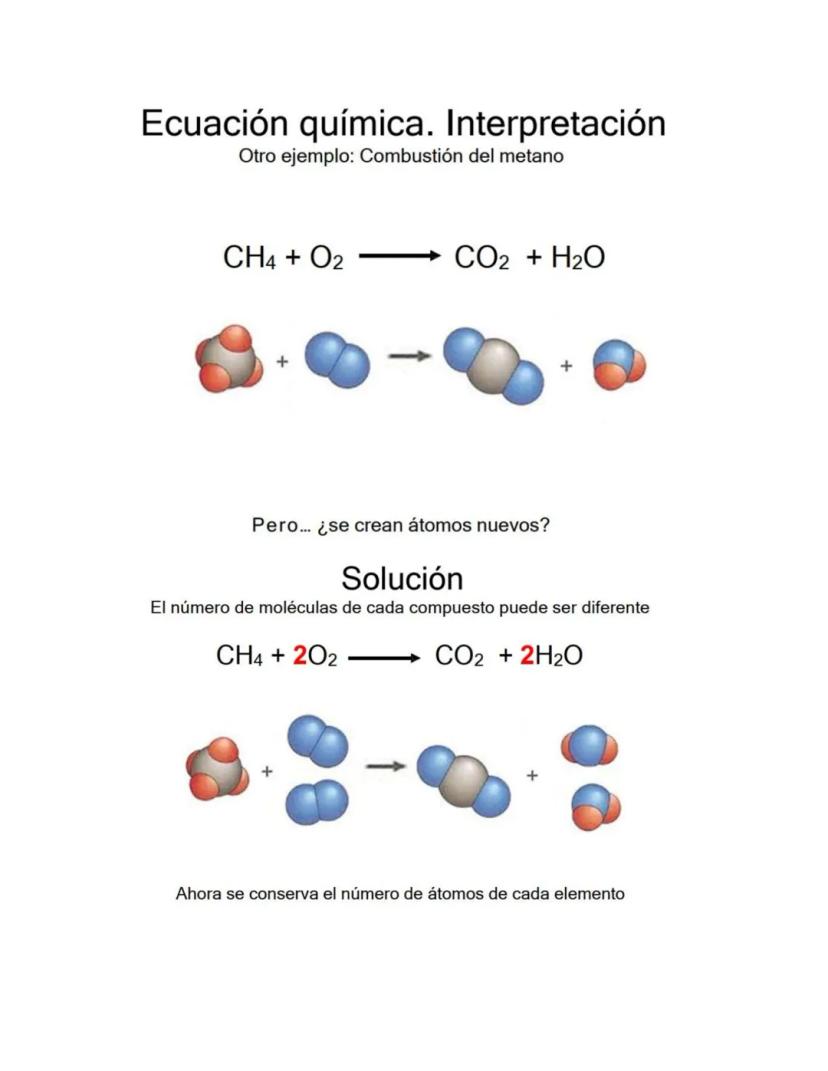
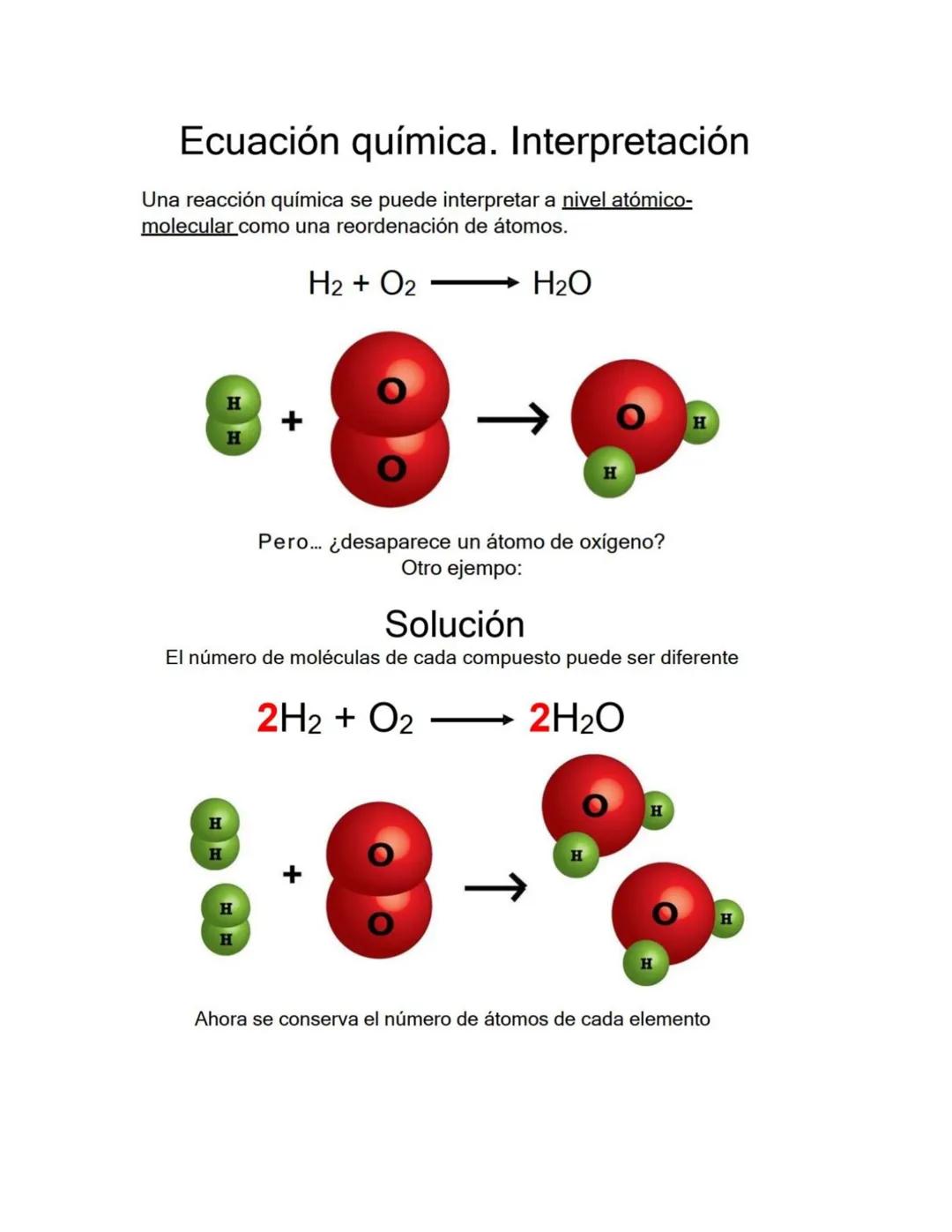
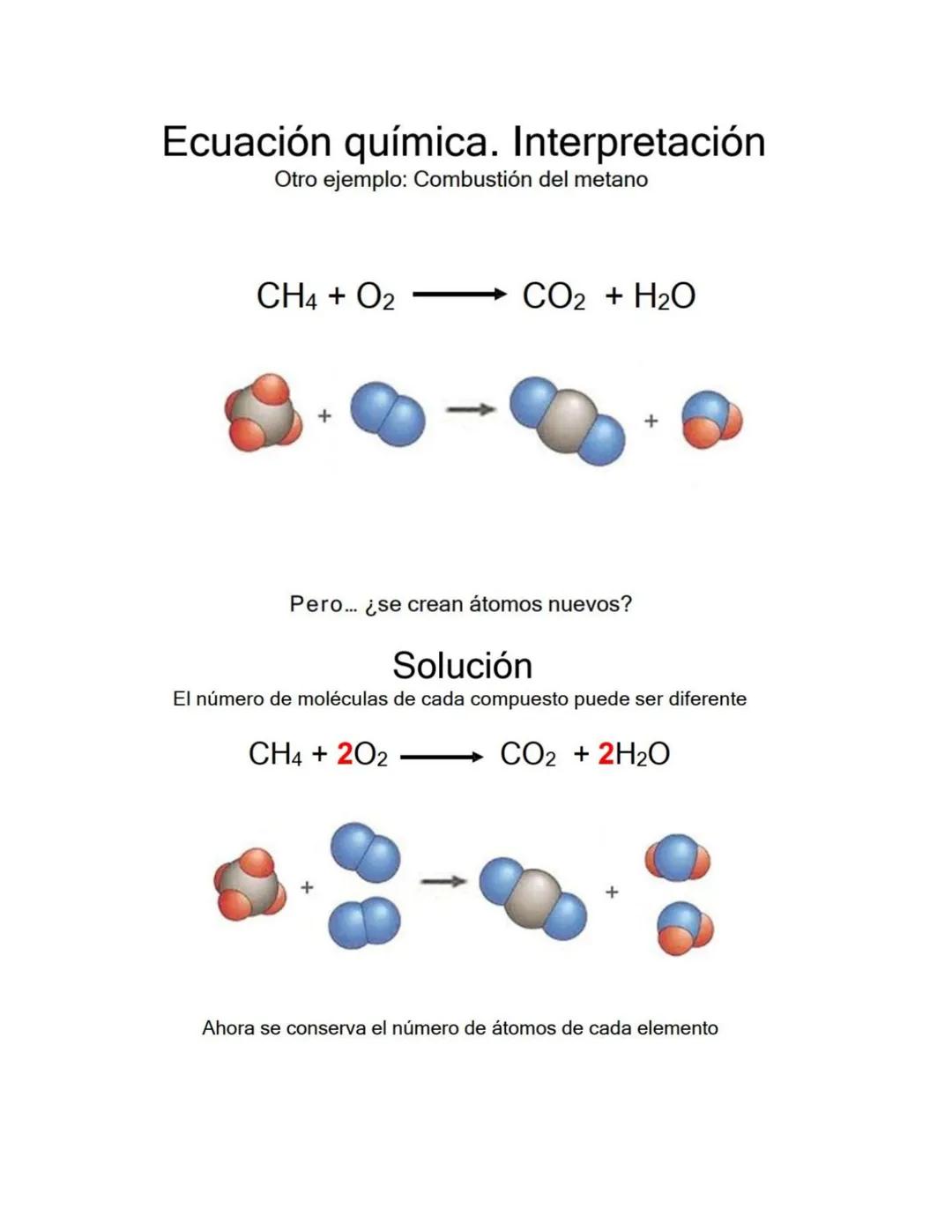
Durante una reacción química, los enlaces entre átomos se rompen y los átomos se reorganizan formando nuevos enlaces. Los átomos son los mismos, pero las conexiones cambian completamente.
Esta reorganización crea sustancias con propiedades totalmente diferentes a las originales. Es como desarmar un LEGO y construir algo nuevo con las mismas piezas.
Pueden participar uno o más reactivos para formar uno o más productos. La clave es que siempre hay el mismo número total de cada tipo de átomo antes y después.
El balanceo te permite visualizar exactamente cómo se reorganizan los átomos y en qué proporciones.
💡 Concepto fundamental: Los átomos son eternos - solo cambian de "vecinos" en las reacciones químicas.
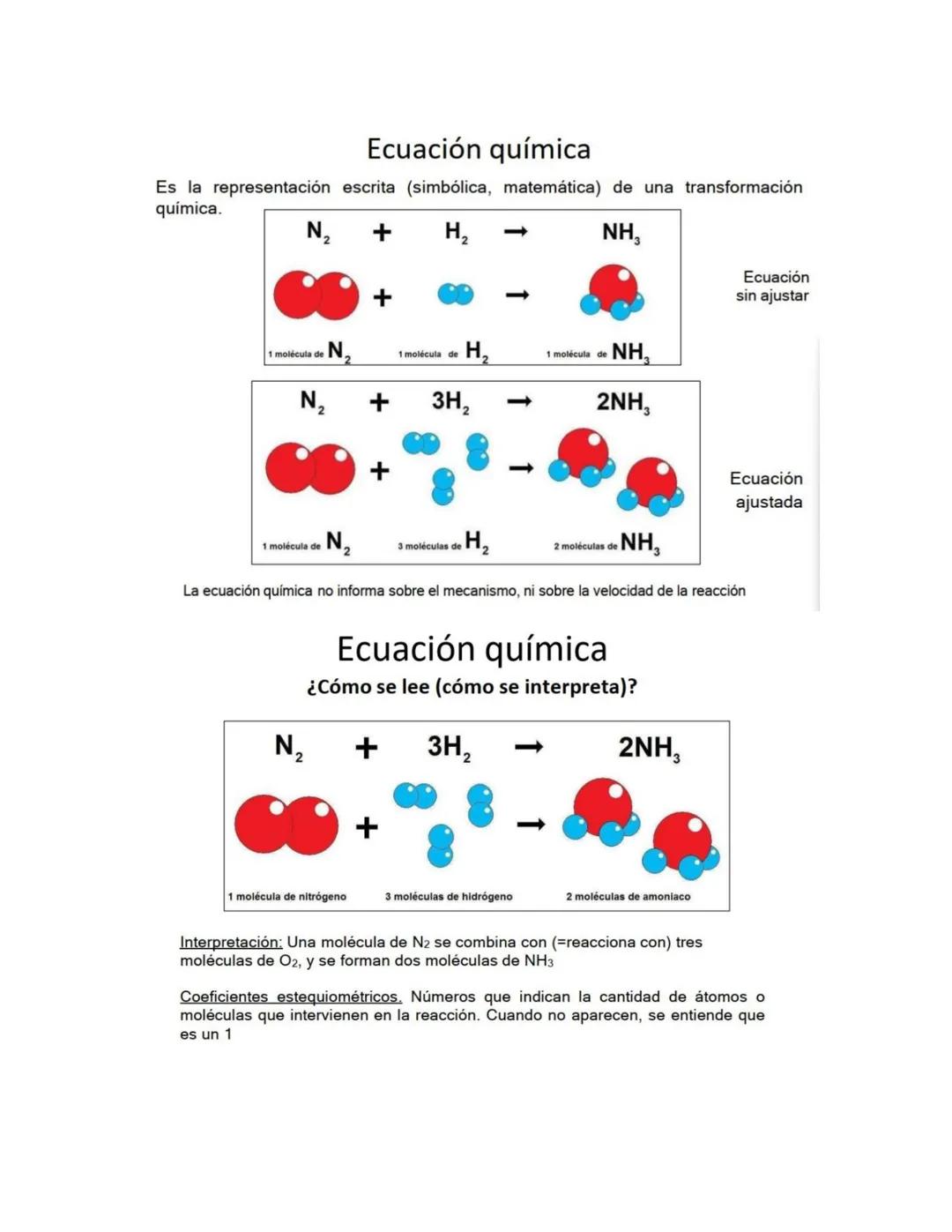
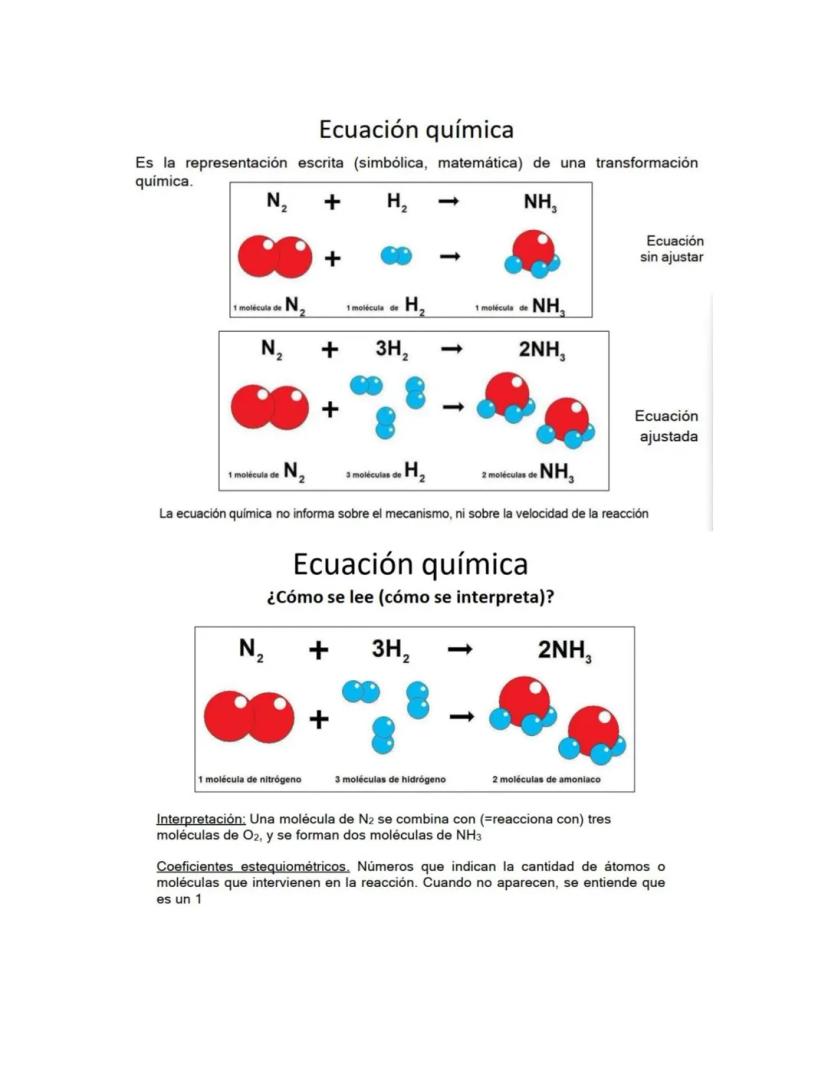
Una ecuación química es la representación matemática de una transformación química. Los números que aparecen son los coeficientes estequiométricos.
La ecuación N₂ + 3H₂ → 2NH₃ se lee: "una molécula de nitrógeno reacciona con tres moléculas de hidrógeno para formar dos moléculas de amoniaco".
Los coeficientes te dicen las proporciones exactas en que reaccionan las sustancias. Cuando no aparece número, se entiende que es 1.
Las ecuaciones no te dicen qué tan rápido ocurre la reacción ni los pasos intermedios - solo los materiales iniciales y finales.
💡 Para dominar esto: Practica leyendo ecuaciones en voz alta hasta que sea automático interpretar los coeficientes.






Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener dificultades para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuario de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser muy difícil reunir toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis notas y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuario de Android
Siempre estaba estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a manejar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZZES Y FLASHCARDS SON SÚPER ÚTILES Y AMO Knowunity AI. TAMBIÉN ES LITERALMENTE COMO CHATGPT PERO MÁS INTELIGENTE!! ME AYUDÓ CON MIS PROBLEMAS DE RÍMEL TAMBIÉN!! Y CON MIS MATERIAS REALES OBVIO! 😍😁😲🤑💗✨🎀😮
Sarah L
usuario de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros – me siento mucho más seguro cuando me preparo para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener dificultades para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuario de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser muy difícil reunir toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis notas y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuario de Android
Siempre estaba estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a manejar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZZES Y FLASHCARDS SON SÚPER ÚTILES Y AMO Knowunity AI. TAMBIÉN ES LITERALMENTE COMO CHATGPT PERO MÁS INTELIGENTE!! ME AYUDÓ CON MIS PROBLEMAS DE RÍMEL TAMBIÉN!! Y CON MIS MATERIAS REALES OBVIO! 😍😁😲🤑💗✨🎀😮
Sarah L
usuario de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros – me siento mucho más seguro cuando me preparo para los exámenes.
Paul T
usuario de iOS
Jazmin Rangel
@jazminran_tzia9
¿Sabías que toda la química se basa en entender cómo los átomos se comportan y se combinan? Desde el número de protones en el núcleo hasta las reacciones que ocurren en tu cuerpo, todo sigue patrones específicos que puedes dominar... Mostrar más

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El número atómico es básicamente la "identificación" de cada elemento - es el número de protones en el núcleo y se representa con la letra "Z". Piensa en esto como el ADN de cada átomo.
Los isótopos son como gemelos del mismo elemento que solo difieren en el número de neutrones. Esto significa que tienen el mismo número atómico pero diferente masa atómica.
La masa atómica se calcula sumando protones + neutrones. Es súper importante para resolver problemas en química, así que memoriza esta fórmula simple.
💡 Tip clave: El número atómico nunca cambia para un elemento, pero los neutrones sí pueden variar creando isótopos.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los metales están del lado izquierdo de la tabla periódica porque ceden electrones fácilmente - tienen solo 1, 2 o 3 electrones en su capa externa. Son brillantes, conducen electricidad y calor, y son maleables.
Los no metales se ubican a la derecha porque tienen 6 o 7 electrones en su última capa y prefieren "robar" electrones de otros elementos. Los gases nobles (grupo 18) no interactúan porque ya tienen su capa completa.
Los semimetales son elementos "indecisos" - a veces actúan como metales y otras veces no, dependiendo de las condiciones.
Los períodos representan el número de niveles energéticos que tienen los átomos. Mientras más abajo en la tabla, más niveles energéticos.
💡 Dato curioso: El hidrógeno es la excepción rara - está con los metales pero es un gas, no un metal.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los enlaces iónicos se forman cuando los átomos se vuelven iones con cargas opuestas. Es como el magnetismo - los opuestos se atraen y crean enlaces súper fuertes.
Los cationes son iones positivos (perdieron electrones) y los aniones son iones negativos (ganaron electrones). Los aniones siempre terminan en "-uro" como cloruro o sulfuro.
La transferencia de electrones ocurre cuando un átomo pierde electrones y otro los gana completamente. El sodio y cloro son el ejemplo clásico de esto.
Los enlaces covalentes se forman cuando los átomos comparten electrones en lugar de transferirlos. Estos son más comunes en los seres vivos que los enlaces iónicos.
💡 Recuerda: Iónico = transferencia completa, Covalente = compartir electrones.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las reacciones exotérmicas liberan calor - el recipiente se siente caliente al tocarlo. Las reacciones endotérmicas absorben calor - el recipiente se siente frío.
La Ley de conservación de la materia dice que los átomos no se crean ni destruyen, solo se reorganizan. Lo mismo pasa con la Ley de conservación de la energía.
Las ecuaciones químicas son el lenguaje que usan los químicos para describir qué sucede en una reacción. Te permiten predecir productos y calcular proporciones exactas.
La termoquímica estudia cómo el calor se relaciona con las reacciones químicas. Es fundamental para entender por qué algunas reacciones necesitan calor y otras lo producen.
💡 Concepto clave: En cualquier reacción, la cantidad total de materia y energía antes = después, solo cambia de forma.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Las reacciones de síntesis o combinación siguen el patrón A + B → AB. Dos o más sustancias se unen para formar una sola más compleja.
Ejemplos típicos incluyen: metal + oxígeno = óxido metálico, o no metal + oxígeno = óxido no metálico. También óxido + agua puede formar hidróxidos o ácidos.
Las reacciones de descomposición hacen exactamente lo opuesto: AB → A + B. Un compuesto complejo se rompe en sustancias más simples.
Muchas descomposiciones necesitan calor para ocurrir. Los compuestos con oxígeno son especialmente propensos a descomponerse cuando se calientan.
💡 Tip para exámenes: Síntesis = construir (juntar), Descomposición = demoler (separar).

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
En la sustitución simple, un elemento "echa fuera" a otro de un compuesto. El patrón es AB + C → A + CB.
Tienes que identificar qué elementos pueden intercambiarse: los que forman cationes sustituyen cationes, y los que forman aniones sustituyen aniones.
Un elemento puro reacciona con un compuesto acuoso para producir un nuevo compuesto acuoso y un elemento puro diferente.
El truco está en predecir si la reacción realmente ocurrirá - depende de la serie de actividad de los metales.
💡 Visualiza esto: Es como un baile donde los elementos cambian de pareja, pero solo si el "nuevo" es más activo que el que está.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La sustitución doble es como un intercambio de parejas: AX + BZ → AZ + BX. Los cationes intercambian aniones entre dos compuestos.
Estas reacciones solo ocurren si se cumple una condición específica: formación de precipitado, obtención de agua/gas, o desprendimiento de calor.
Los tipos principales incluyen neutralización , formación de precipitados insolubles, y formación de gases.
Las reacciones ácido-base siempre producen sal + agua + calor. Los precipitados se indican con (s) y los gases con una flecha hacia arriba ↑.
💡 Regla de oro: Si no se forma precipitado, gas, agua o hay cambio de calor, la reacción de doble sustitución NO ocurre.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El balanceo por tanteo es el método básico para igualar átomos en ambos lados de la ecuación. Esto verifica la Ley de Conservación de la Materia.
El orden correcto es: primero balancear metales, luego no metales, y al final oxígeno e hidrógeno. Los coeficientes van al frente de cada compuesto.
Multiplica los coeficientes por los subíndices para contar átomos totales. Si los números no coinciden en ambos lados, ajusta los coeficientes.
Siempre verifica tu respuesta final contando nuevamente todos los átomos de cada elemento en reactivos y productos.
💡 Estrategia efectiva: Empieza con el compuesto más complejo y deja los elementos puros para el final del balanceo.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Durante una reacción química, los enlaces entre átomos se rompen y los átomos se reorganizan formando nuevos enlaces. Los átomos son los mismos, pero las conexiones cambian completamente.
Esta reorganización crea sustancias con propiedades totalmente diferentes a las originales. Es como desarmar un LEGO y construir algo nuevo con las mismas piezas.
Pueden participar uno o más reactivos para formar uno o más productos. La clave es que siempre hay el mismo número total de cada tipo de átomo antes y después.
El balanceo te permite visualizar exactamente cómo se reorganizan los átomos y en qué proporciones.
💡 Concepto fundamental: Los átomos son eternos - solo cambian de "vecinos" en las reacciones químicas.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Una ecuación química es la representación matemática de una transformación química. Los números que aparecen son los coeficientes estequiométricos.
La ecuación N₂ + 3H₂ → 2NH₃ se lee: "una molécula de nitrógeno reacciona con tres moléculas de hidrógeno para formar dos moléculas de amoniaco".
Los coeficientes te dicen las proporciones exactas en que reaccionan las sustancias. Cuando no aparece número, se entiende que es 1.
Las ecuaciones no te dicen qué tan rápido ocurre la reacción ni los pasos intermedios - solo los materiales iniciales y finales.
💡 Para dominar esto: Practica leyendo ecuaciones en voz alta hasta que sea automático interpretar los coeficientes.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
1
Herramientas Inteligentes NUEVO
Convierte estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Tarjetas de Estudio Interactivas ✓ Examen Completo de Práctica ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener dificultades para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuario de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser muy difícil reunir toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis notas y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuario de Android
Siempre estaba estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a manejar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZZES Y FLASHCARDS SON SÚPER ÚTILES Y AMO Knowunity AI. TAMBIÉN ES LITERALMENTE COMO CHATGPT PERO MÁS INTELIGENTE!! ME AYUDÓ CON MIS PROBLEMAS DE RÍMEL TAMBIÉN!! Y CON MIS MATERIAS REALES OBVIO! 😍😁😲🤑💗✨🎀😮
Sarah L
usuario de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros – me siento mucho más seguro cuando me preparo para los exámenes.
Paul T
usuario de iOS
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Solía tener dificultades para completar mis tareas a tiempo hasta que descubrí Knowunity, que no solo facilita subir mi propio contenido sino que también proporciona excelentes resúmenes que hacen mi trabajo más rápido y eficiente.
Thomas R
usuario de iOS
Siempre era un desafío encontrar toda la información importante para mis tareas – desde que comencé a usar Knowunity, puedo simplemente subir mi contenido y beneficiarme de los resúmenes de otros, lo que me ayuda mucho con la organización.
Lisa M
usuario de Android
A menudo sentía que no tenía suficiente visión general al estudiar, pero desde que comencé a usar Knowunity, eso ya no es un problema – subo mi contenido y siempre encuentro resúmenes útiles en la plataforma, lo que hace mi aprendizaje mucho más fácil.
David K
usuario de iOS
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Solía ser muy difícil reunir toda la información para mis presentaciones. Pero desde que comencé a usar Knowunity, solo subo mis notas y encuentro increíbles resúmenes de otros – ¡hace mi estudio mucho más eficiente!
Julia S
usuario de Android
Siempre estaba estresado con todo el material de estudio, pero desde que comencé a usar Knowunity, subo mis cosas y reviso los geniales resúmenes de otros – realmente me ayuda a manejar todo mejor y es mucho menos estresante.
Marco B
usuario de iOS
LOS QUIZZES Y FLASHCARDS SON SÚPER ÚTILES Y AMO Knowunity AI. TAMBIÉN ES LITERALMENTE COMO CHATGPT PERO MÁS INTELIGENTE!! ME AYUDÓ CON MIS PROBLEMAS DE RÍMEL TAMBIÉN!! Y CON MIS MATERIAS REALES OBVIO! 😍😁😲🤑💗✨🎀😮
Sarah L
usuario de Android
Antes pasaba horas buscando en Google materiales escolares, pero ahora solo subo mis cosas a Knowunity y reviso los útiles resúmenes de otros – me siento mucho más seguro cuando me preparo para los exámenes.
Paul T
usuario de iOS